近期帕金森病相关研究进展
来源:本站原创 2019-05-20 22:33
2019年5月21日 讯 /生物谷BIOON/ --本期为大家带来的是帕金森症领域的最新研究进展,希望读者朋友们能够喜欢。1. Cell Res:意外发现!维生素B12或许可以治疗遗传性帕金森!DOI: 10.1038/s41422-019-0153-8巴斯克科学基金会的研究员、Biofisika研究所(CSIC-UPV/EHU)主任Iban Ubarretxena参与的一项研究发现了一种可能被开
2019年5月21日 讯 /生物谷BIOON/ --本期为大家带来的是帕金森症领域的最新研究进展,希望读者朋友们能够喜欢。
1. Cell Res:意外发现!维生素B12或许可以治疗遗传性帕金森!
DOI: 10.1038/s41422-019-0153-8
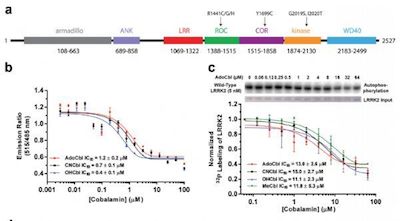
巴斯克科学基金会的研究员、Biofisika研究所(CSIC-UPV/EHU)主任Iban Ubarretxena参与的一项研究发现了一种可能被开发用于对抗帕金森疾病的新型抑制剂,相关研究成果于近日发表在《Cell Research》上。
帕金森是最常见的慢性神经退行性运动障碍,影响着全球1%的70岁以上的人群。目前为止没有药物可以治疗这种疾病,而现有的治疗方法仅仅在于处理其症状,但是不能延缓其进展。虽然帕金森病的大多数病例是散发性的,但这种疾病的遗传变异主要与编码LRRK2酶的基因突变有关。
2004年一个国际研究团队发现了这个酶的一种突变和病人患这种疾病之间的关系。LRRK2酶又叫做Dardarina,在巴斯克语中的意思是“震颤”,已经成为了开发对抗遗传性帕金森最有吸引力的治疗靶标。与LRRK2相关的神经毒性和致病效应主要是由于致病突变增加了其激酶活性,这促使国际上竞相开发LRRK2的抑制剂。目前,确实存在LRRK2激酶活性特异性的强效抑制剂,但是其中许多药物会产生不良副作用或产生非常不明确的临床结果。
这项最新研究由Iban Ubarretxena领导,他和国际团队合作发现了维生素B12的一种活化成分AdoCbl在培养的细胞和脑组织中可以有效抑制LRRK2的激酶活性。它还可以显著降低一系列帕金森动物模型中LRRK2突变体的神经毒性。该研究表明维生素B12可能是一类LRRK2激酶活性的新型调节剂。
“这想研究迈出了一大步,因为它在动物模型中是一个神经保护性的维生素,而且代表着一类全新的抑制剂。因此我们可以以它为基础开发出治疗与LRRK2突变相关的遗传性帕金森的新疗法。”
2. J Clin Onco:化疗药物对帕金森患者产生积极治疗效果
DOI: 10.1200/JCO.18.02158
根据美国癌症协会的数据,前列腺癌是2018年美国男性癌症相关死亡的第二大常见原因。目前,高危局限性前列腺癌的治疗标准是放疗的组合( RT)和长期(24-36个月)雄激素抑制(AS)。研究人员推测,将辅助多西紫杉醇(一种细胞毒性化疗药物)添加到护理标准RT和长期AS治疗可能会改善患有局部高风险前列腺癌的男性的总体生存率和临床结果。
多西紫杉醇为基础的化疗改善了去势抵抗和去势敏感的前列腺癌患者的总体生存率,患者通常耐受良好,并且可能能够靶向激素抵抗细胞,从而补充AS靶向激素敏感细胞的能力。因此,NRG肿瘤学临床试验NRG-RTOG 0521旨在比较使用和不使用多西紫杉醇的化疗的护理标准,并确定添加多西紫杉醇是否能改善OS,无病生存(DFS)和远处转移率( DM)用于患有高风险非转移性前列腺癌的男性。该研究的结果最近发表在Journal of Clinical Oncology上。
多中心III期试验NRG-RTOG 0521将男性随机分配到两个可能的治疗组之一。两个治疗组均接受8周AS,然后接受RT并行AS,然后进行辅助AS治疗24个月。护理标准加化疗组在完成RT后28天开始接受另外6个剂量的多西他赛和泼尼松同时给予AS。
“随机分组后4年,细胞毒性化疗对雄激素抑制和放疗的增加使总生存率从89%提高到93%。无病生存率和远处转移率也有所改善,”医学博士Seth A. Rosenthal表示: “这些都是有希望的结果。试验结果表明多西紫杉醇化疗长期加入标准治疗对于患有高风险非转移性前列腺癌的男性,雄激素抑制疗法和RT是一种可行的治疗选择。医生应该考虑与选择适合化疗的患者讨论这一选择“
3. J Par Dis:干细胞疗法有助于缓解帕金森症
DOI: 10.3233/JPD-181488

根据最近一项研究,细胞替代疗法可能在将来减轻帕金森病(PD)的运动症状方面发挥越来越大的作用。在最近发表在《Journal of Parkinson's Disease》杂志上的文章中,作者讨论了新开发的干细胞技术如何用于治疗疾病,以及干细胞治疗的巨大希望和重大挑战。
今天最常见的PD治疗是通过多巴胺调节增强脑中黑质纹状体通路的活性,从而增加纹状体多巴胺水平并改善与该疾病相关的运动损伤。然而,这种治疗长期来看具有显著的局限性和副作用。相比之下,干细胞技术显示出治疗PD的希望,并且可能在未来几十年中至少减轻运动症状中起到越来越大的作用。
作者分析了新开发的干细胞技术如何用于治疗PD,以及临床研究人员如何迅速将这项技术转化为早期临床试验。在过去,PD中的大多数移植研究使用来自流产胚胎的人类细胞。虽然这种方式植入的细胞可以存活并保持活性长达多年,但存在科学和伦理问题:胎儿细胞供应有限、个体差异很大,难以控制质量。只有一些患者受益,一些患者则会出现副作用。
干细胞技术的最新进展意味着可以确保质量,一致性,活性和安全性,并且可以在实验室中生长基本上无限量的产生多巴胺的神经细胞用于移植。这种方法现在正迅速进入临床试验的初步测试。随着多种人胚胎干细胞系的可用性,以及从患者自身血液或皮肤细胞产生诱导多能细胞或神经元细胞的可能性,起始材料的选择也得到了扩展。最初使用多能干细胞作为供体组织的系统临床移植试验于2018年在日本启动。
“这种PD大脑修复方法肯定具有巨大的潜力,未来二十年也可能会看到干细胞工程在针对特定患者或患者群体量身定制的干细胞方面取得更大进展,”医学博士Patrik Brundin评论道。 “与此同时,还需要跨越生物、实践领域和商业障碍才能真正成为常规治疗。”
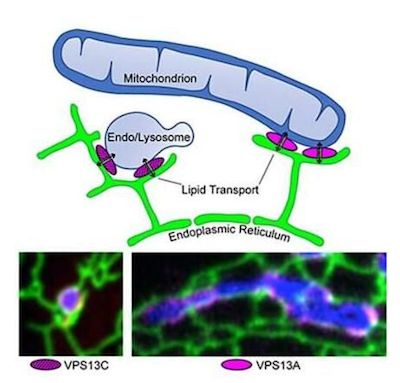
多个基因的突变与帕金森疾病直接相关,但目前研究人员并不清楚这些基因突变是如何影响个体患上帕金森疾病的;近日,一项刊登在国际杂志The Journal of Cell Biology上的研究报告中,来自耶鲁大学的科学家们通过研究重点对一种诱发家族性帕金森疾病的基因突变进行研究,他们发现,该基因能够编码一种特殊蛋白,而该蛋白能控制脂质在细胞器膜之间的转移。
文章中,研究者调查了VPS13蛋白的关键角色,VPS13蛋白的功能障碍在多种类型神经性疾病发生过程中扮演着重要作用,包括帕金森疾病等。研究者发现,VPS13蛋白能从细胞膜中提取脂质,并将其藏匿于“防水腔体”(waterproof cavity)中,随后再转移到附近的膜结构上。VPS13蛋白家族成员位于细胞中细胞器彼此相互靠近的位点,即所谓的接触点(contact sites),其能够作为不同细胞器之间的纽带,使脂质的传递更加有效。
VPS13蛋白家族成员能在细胞内的不同位点发挥作用,同时与多种不同的神经性障碍发生直接相关,与帕金森疾病相关的VPS13C蛋白就能够作用于内质网与溶酶体之间的接触面,此外,另外一种与亨廷顿样综合征(舞蹈病-棘状红细胞增多症,ChAc)相关的VPS13A蛋白也能作用于内质网和线粒体之间的接触面。
其它的帕金森疾病基因也会编码溶酶体内系统的特殊蛋白,这或许就能帮助研究人员鉴别出不同基因突变所诱发的帕金森疾病之间共有的细胞机制,同时也有助于开发治疗帕金森疾病的新型疗法。
5. Eur J Neurosci:经过CRISPR/Cas9n编辑的干细胞有望治疗帕金森病
DOI: 10.1111/ejn.14286.

在英国,帕金森病的发病率大约为1/350。在一项新的研究中,来自英国爱丁堡大学和UCB制药公司(UCB Pharma Ltd.)的研究人员在改善一种新出现的治疗帕金森病的方法上迈出了关键一步。这一进展可能有助于开发一种有希望的称为细胞替代疗法(cell replacement therapy)的疗法。专家们希望这种涉及将健康细胞移植到被帕金森病破坏的大脑区域中的疗法能够缓解震颤和平衡问题等症状。相关研究结果近期发表在European Journal of Neuroscience期刊上,论文标题为“Engineering synucleinopathy‐resistant human dopaminergic neurons by CRISPR‐mediated deletion of the SNCA gene”。
在这项新的研究中,这些研究人员构建出对帕金森病有抵抗力的人胚胎干细胞(hESC)。具体而言,他们利用一种称为CRISPR/Cas9n的先进技术切除hESC中的DNA片段。在这样做的过程中,他们剔除了与有毒性的团块(称为路易小体)形成相关的基因SNCA,其中这种毒性团块形成是帕金森患者中的脑细胞的一种典型特征。
在实验室测试中,这些干细胞在培养皿中可被转化为产生多巴胺的神经元。它们随后在接受一种化学试剂处理后就可导致路易小体形成。这些研究人员发现相比于未经过基因编辑的神经元,经过基因编辑的神经元并没有形成有毒性团块。
这些研究人员表示,这一进展可能对患有帕金森病的年轻患者和患有侵袭性帕金森病的患者是最有益的,但是它还需在人体试验中进行测试。
论文通讯作者、爱丁堡大学医学研究委员会再生医学中心的Tilo Kunath博士说,“我们知道帕金森病在神经元之间进行扩散并侵入健康细胞。这实际上可能为细胞替代疗法的潜力设置一个使用期限。我们的激动人心的发现有潜力极大地改善这些新出现的疗法。”
帕金森病治愈基金会(Cure Parkinson's Trust)研究副主任Simon Stott博士说,“细胞替代疗法是一种治疗帕金森病患者的实验性再生医学方法。这项新研究在开发这种疗法上提供了新的进展。很高兴的是,帕金森病治愈基金会资助了这项鼓舞人心的创新研究。”
6. PNAS:咖啡中的两种化合物组合或能有效抵御帕金森等大脑变性疾病
DOI: 10.1073/pnas.1813365115

近日,一项刊登在国际杂志Proceedings of the National Academy of Sciences上的研究报告中,来自美国罗格斯大学的科学家们通过研究发现,咖啡中的一种特殊化合物或能与咖啡因一起协作来帮助抵御帕金森疾病和路易体痴呆症(Lewy Body Dementia)的发生,帕金森疾病和路易体痴呆症是两种进行性、目前并无有效治愈疗法且与大脑变性相关的疾病。
研究者表示,这两种化合物或能联合作用作为一种减缓大脑神经变性的新疗法,他们指出,喝咖啡能够降低个体患帕金森疾病的风险,虽然传统认为咖啡因是咖啡的特殊保护剂,而实际上咖啡豆中含有上千种鲜为人知的化合物。这项研究中,研究人员重点对一种名为EHT的神经递质血清素的脂肪酸衍生物进行研究,其主要存在于豆类的蜡质层中,研究者发现,EHT能保护小鼠的大脑抵御与帕金森疾病和路易体痴呆症相关的异常蛋白质的积累。
当前研究中,研究者想通过研究确定是否EHT和咖啡因能够相互协作来为大脑提供保护作用,他们分别给予小鼠低剂量的EHT、咖啡因及EHT和咖啡因,当两种化合物单独使用时并不会起到保护作用,但当其组合使用时就能增强活性抑制小鼠大脑中有害蛋白的积累,这就表明,EHT和咖啡因的组合会能有效减缓上述疾病的进展,当前研究人员所使用的疗法仅能解决部分帕金森患者的疾病症状,其并不会保护患者大脑抵御大脑的退行性病变。
研究者Mouradian说道,后期还需要进行更为深入的研究来确定能够在人类机体中发挥保护作用的EHT和咖啡因的比率及使用量;EHT是多种类型咖啡中常见的化合物,最重要的是要确定摄入EHT和咖啡因的合适水平及合适比例,这样人们就不会过度摄入咖啡因了,否则就会对人类健康产生负面影响。
据美国卫生与公共服务部数据显示,帕金森是一种人类大脑障碍,其会导致患者机体不停摇动、僵硬、行走困难以及身体协调性较差,目前美国约有100万名帕金森疾病患者;而路易体痴呆症则是最常见的一种痴呆症,其在美国影响着超过100万人的健康,这种疾病会诱发患者出现思维、行为、情绪和运动问题。(生物谷Bioon.com)
1. Cell Res:意外发现!维生素B12或许可以治疗遗传性帕金森!
DOI: 10.1038/s41422-019-0153-8

巴斯克科学基金会的研究员、Biofisika研究所(CSIC-UPV/EHU)主任Iban Ubarretxena参与的一项研究发现了一种可能被开发用于对抗帕金森疾病的新型抑制剂,相关研究成果于近日发表在《Cell Research》上。
帕金森是最常见的慢性神经退行性运动障碍,影响着全球1%的70岁以上的人群。目前为止没有药物可以治疗这种疾病,而现有的治疗方法仅仅在于处理其症状,但是不能延缓其进展。虽然帕金森病的大多数病例是散发性的,但这种疾病的遗传变异主要与编码LRRK2酶的基因突变有关。
2004年一个国际研究团队发现了这个酶的一种突变和病人患这种疾病之间的关系。LRRK2酶又叫做Dardarina,在巴斯克语中的意思是“震颤”,已经成为了开发对抗遗传性帕金森最有吸引力的治疗靶标。与LRRK2相关的神经毒性和致病效应主要是由于致病突变增加了其激酶活性,这促使国际上竞相开发LRRK2的抑制剂。目前,确实存在LRRK2激酶活性特异性的强效抑制剂,但是其中许多药物会产生不良副作用或产生非常不明确的临床结果。
这项最新研究由Iban Ubarretxena领导,他和国际团队合作发现了维生素B12的一种活化成分AdoCbl在培养的细胞和脑组织中可以有效抑制LRRK2的激酶活性。它还可以显著降低一系列帕金森动物模型中LRRK2突变体的神经毒性。该研究表明维生素B12可能是一类LRRK2激酶活性的新型调节剂。
“这想研究迈出了一大步,因为它在动物模型中是一个神经保护性的维生素,而且代表着一类全新的抑制剂。因此我们可以以它为基础开发出治疗与LRRK2突变相关的遗传性帕金森的新疗法。”
2. J Clin Onco:化疗药物对帕金森患者产生积极治疗效果
DOI: 10.1200/JCO.18.02158

根据美国癌症协会的数据,前列腺癌是2018年美国男性癌症相关死亡的第二大常见原因。目前,高危局限性前列腺癌的治疗标准是放疗的组合( RT)和长期(24-36个月)雄激素抑制(AS)。研究人员推测,将辅助多西紫杉醇(一种细胞毒性化疗药物)添加到护理标准RT和长期AS治疗可能会改善患有局部高风险前列腺癌的男性的总体生存率和临床结果。
多西紫杉醇为基础的化疗改善了去势抵抗和去势敏感的前列腺癌患者的总体生存率,患者通常耐受良好,并且可能能够靶向激素抵抗细胞,从而补充AS靶向激素敏感细胞的能力。因此,NRG肿瘤学临床试验NRG-RTOG 0521旨在比较使用和不使用多西紫杉醇的化疗的护理标准,并确定添加多西紫杉醇是否能改善OS,无病生存(DFS)和远处转移率( DM)用于患有高风险非转移性前列腺癌的男性。该研究的结果最近发表在Journal of Clinical Oncology上。
多中心III期试验NRG-RTOG 0521将男性随机分配到两个可能的治疗组之一。两个治疗组均接受8周AS,然后接受RT并行AS,然后进行辅助AS治疗24个月。护理标准加化疗组在完成RT后28天开始接受另外6个剂量的多西他赛和泼尼松同时给予AS。
“随机分组后4年,细胞毒性化疗对雄激素抑制和放疗的增加使总生存率从89%提高到93%。无病生存率和远处转移率也有所改善,”医学博士Seth A. Rosenthal表示: “这些都是有希望的结果。试验结果表明多西紫杉醇化疗长期加入标准治疗对于患有高风险非转移性前列腺癌的男性,雄激素抑制疗法和RT是一种可行的治疗选择。医生应该考虑与选择适合化疗的患者讨论这一选择“
3. J Par Dis:干细胞疗法有助于缓解帕金森症
DOI: 10.3233/JPD-181488

根据最近一项研究,细胞替代疗法可能在将来减轻帕金森病(PD)的运动症状方面发挥越来越大的作用。在最近发表在《Journal of Parkinson's Disease》杂志上的文章中,作者讨论了新开发的干细胞技术如何用于治疗疾病,以及干细胞治疗的巨大希望和重大挑战。
今天最常见的PD治疗是通过多巴胺调节增强脑中黑质纹状体通路的活性,从而增加纹状体多巴胺水平并改善与该疾病相关的运动损伤。然而,这种治疗长期来看具有显著的局限性和副作用。相比之下,干细胞技术显示出治疗PD的希望,并且可能在未来几十年中至少减轻运动症状中起到越来越大的作用。
作者分析了新开发的干细胞技术如何用于治疗PD,以及临床研究人员如何迅速将这项技术转化为早期临床试验。在过去,PD中的大多数移植研究使用来自流产胚胎的人类细胞。虽然这种方式植入的细胞可以存活并保持活性长达多年,但存在科学和伦理问题:胎儿细胞供应有限、个体差异很大,难以控制质量。只有一些患者受益,一些患者则会出现副作用。
干细胞技术的最新进展意味着可以确保质量,一致性,活性和安全性,并且可以在实验室中生长基本上无限量的产生多巴胺的神经细胞用于移植。这种方法现在正迅速进入临床试验的初步测试。随着多种人胚胎干细胞系的可用性,以及从患者自身血液或皮肤细胞产生诱导多能细胞或神经元细胞的可能性,起始材料的选择也得到了扩展。最初使用多能干细胞作为供体组织的系统临床移植试验于2018年在日本启动。
“这种PD大脑修复方法肯定具有巨大的潜力,未来二十年也可能会看到干细胞工程在针对特定患者或患者群体量身定制的干细胞方面取得更大进展,”医学博士Patrik Brundin评论道。 “与此同时,还需要跨越生物、实践领域和商业障碍才能真正成为常规治疗。”

多个基因的突变与帕金森疾病直接相关,但目前研究人员并不清楚这些基因突变是如何影响个体患上帕金森疾病的;近日,一项刊登在国际杂志The Journal of Cell Biology上的研究报告中,来自耶鲁大学的科学家们通过研究重点对一种诱发家族性帕金森疾病的基因突变进行研究,他们发现,该基因能够编码一种特殊蛋白,而该蛋白能控制脂质在细胞器膜之间的转移。
文章中,研究者调查了VPS13蛋白的关键角色,VPS13蛋白的功能障碍在多种类型神经性疾病发生过程中扮演着重要作用,包括帕金森疾病等。研究者发现,VPS13蛋白能从细胞膜中提取脂质,并将其藏匿于“防水腔体”(waterproof cavity)中,随后再转移到附近的膜结构上。VPS13蛋白家族成员位于细胞中细胞器彼此相互靠近的位点,即所谓的接触点(contact sites),其能够作为不同细胞器之间的纽带,使脂质的传递更加有效。
VPS13蛋白家族成员能在细胞内的不同位点发挥作用,同时与多种不同的神经性障碍发生直接相关,与帕金森疾病相关的VPS13C蛋白就能够作用于内质网与溶酶体之间的接触面,此外,另外一种与亨廷顿样综合征(舞蹈病-棘状红细胞增多症,ChAc)相关的VPS13A蛋白也能作用于内质网和线粒体之间的接触面。
其它的帕金森疾病基因也会编码溶酶体内系统的特殊蛋白,这或许就能帮助研究人员鉴别出不同基因突变所诱发的帕金森疾病之间共有的细胞机制,同时也有助于开发治疗帕金森疾病的新型疗法。
5. Eur J Neurosci:经过CRISPR/Cas9n编辑的干细胞有望治疗帕金森病
DOI: 10.1111/ejn.14286.

在英国,帕金森病的发病率大约为1/350。在一项新的研究中,来自英国爱丁堡大学和UCB制药公司(UCB Pharma Ltd.)的研究人员在改善一种新出现的治疗帕金森病的方法上迈出了关键一步。这一进展可能有助于开发一种有希望的称为细胞替代疗法(cell replacement therapy)的疗法。专家们希望这种涉及将健康细胞移植到被帕金森病破坏的大脑区域中的疗法能够缓解震颤和平衡问题等症状。相关研究结果近期发表在European Journal of Neuroscience期刊上,论文标题为“Engineering synucleinopathy‐resistant human dopaminergic neurons by CRISPR‐mediated deletion of the SNCA gene”。
在这项新的研究中,这些研究人员构建出对帕金森病有抵抗力的人胚胎干细胞(hESC)。具体而言,他们利用一种称为CRISPR/Cas9n的先进技术切除hESC中的DNA片段。在这样做的过程中,他们剔除了与有毒性的团块(称为路易小体)形成相关的基因SNCA,其中这种毒性团块形成是帕金森患者中的脑细胞的一种典型特征。
在实验室测试中,这些干细胞在培养皿中可被转化为产生多巴胺的神经元。它们随后在接受一种化学试剂处理后就可导致路易小体形成。这些研究人员发现相比于未经过基因编辑的神经元,经过基因编辑的神经元并没有形成有毒性团块。
这些研究人员表示,这一进展可能对患有帕金森病的年轻患者和患有侵袭性帕金森病的患者是最有益的,但是它还需在人体试验中进行测试。
论文通讯作者、爱丁堡大学医学研究委员会再生医学中心的Tilo Kunath博士说,“我们知道帕金森病在神经元之间进行扩散并侵入健康细胞。这实际上可能为细胞替代疗法的潜力设置一个使用期限。我们的激动人心的发现有潜力极大地改善这些新出现的疗法。”
帕金森病治愈基金会(Cure Parkinson's Trust)研究副主任Simon Stott博士说,“细胞替代疗法是一种治疗帕金森病患者的实验性再生医学方法。这项新研究在开发这种疗法上提供了新的进展。很高兴的是,帕金森病治愈基金会资助了这项鼓舞人心的创新研究。”
6. PNAS:咖啡中的两种化合物组合或能有效抵御帕金森等大脑变性疾病
DOI: 10.1073/pnas.1813365115

近日,一项刊登在国际杂志Proceedings of the National Academy of Sciences上的研究报告中,来自美国罗格斯大学的科学家们通过研究发现,咖啡中的一种特殊化合物或能与咖啡因一起协作来帮助抵御帕金森疾病和路易体痴呆症(Lewy Body Dementia)的发生,帕金森疾病和路易体痴呆症是两种进行性、目前并无有效治愈疗法且与大脑变性相关的疾病。
研究者表示,这两种化合物或能联合作用作为一种减缓大脑神经变性的新疗法,他们指出,喝咖啡能够降低个体患帕金森疾病的风险,虽然传统认为咖啡因是咖啡的特殊保护剂,而实际上咖啡豆中含有上千种鲜为人知的化合物。这项研究中,研究人员重点对一种名为EHT的神经递质血清素的脂肪酸衍生物进行研究,其主要存在于豆类的蜡质层中,研究者发现,EHT能保护小鼠的大脑抵御与帕金森疾病和路易体痴呆症相关的异常蛋白质的积累。
当前研究中,研究者想通过研究确定是否EHT和咖啡因能够相互协作来为大脑提供保护作用,他们分别给予小鼠低剂量的EHT、咖啡因及EHT和咖啡因,当两种化合物单独使用时并不会起到保护作用,但当其组合使用时就能增强活性抑制小鼠大脑中有害蛋白的积累,这就表明,EHT和咖啡因的组合会能有效减缓上述疾病的进展,当前研究人员所使用的疗法仅能解决部分帕金森患者的疾病症状,其并不会保护患者大脑抵御大脑的退行性病变。
研究者Mouradian说道,后期还需要进行更为深入的研究来确定能够在人类机体中发挥保护作用的EHT和咖啡因的比率及使用量;EHT是多种类型咖啡中常见的化合物,最重要的是要确定摄入EHT和咖啡因的合适水平及合适比例,这样人们就不会过度摄入咖啡因了,否则就会对人类健康产生负面影响。
据美国卫生与公共服务部数据显示,帕金森是一种人类大脑障碍,其会导致患者机体不停摇动、僵硬、行走困难以及身体协调性较差,目前美国约有100万名帕金森疾病患者;而路易体痴呆症则是最常见的一种痴呆症,其在美国影响着超过100万人的健康,这种疾病会诱发患者出现思维、行为、情绪和运动问题。(生物谷Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->


