科学家在癌症生物标志物研究领域取得的新成果!
来源:生物谷原创 2025-12-30 10:44
本文中,小编整理了多篇重要研究成果,共同聚焦科学家们在癌症生物标志物研究领域取得的新成果,分享给大家!
【1】Science:科学家发现AQP5为胃癌干细胞关键标志物,为靶向治疗提供新路径
doi:10.1126/science.adr2428
近日,国际知名期刊Science发表了一项突破性研究,揭示水通道蛋白AQP5在胃幽门区癌症干细胞(CSCs)中的核心作用。该研究通过小鼠和人类多模型实验证实,AQP5不仅可作为胃癌干细胞的特异性表面标志物,还直接通过WNT、PI3K和MAPK信号通路驱动肿瘤增殖与转移。这一发现为胃癌的靶向治疗和再生医学提供了新方向。
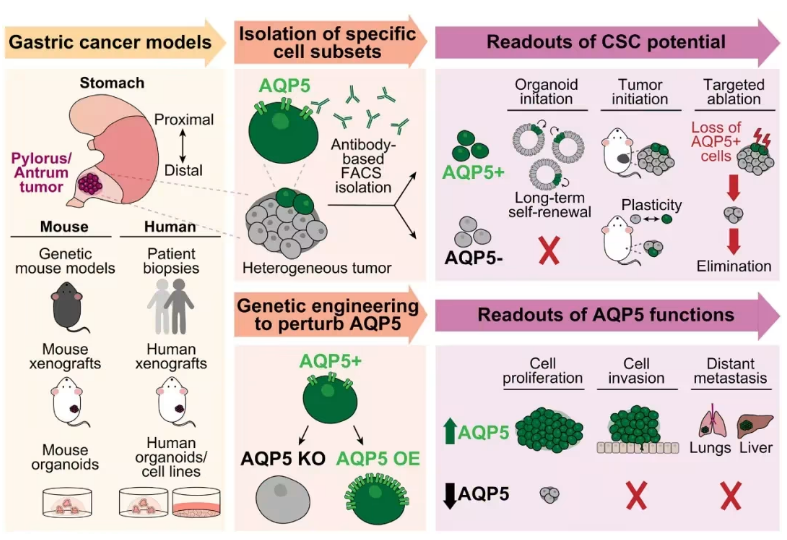
AQP5是小鼠和人类胃癌干细胞的功能性标志物
胃癌的复发与转移常归因于癌症干细胞的存在,但长期以来其特异性表面标志物难以确定。尽管LGR5等标记物在小鼠胃干细胞中已被证实,但其人类同源群体因缺乏分离工具仍不明确。此外,许多候选标志物在正常组织中广泛表达,限制了其靶向治疗的可行性。
研究团队通过单细胞测序和转基因小鼠模型发现,AQP5在幽门区胃癌细胞中高表达,且与LGR5等经典干细胞标记共定位。在功能实验中,AQP5+细胞能够启动类器官培养并在移植后重建肿瘤,而AQP5?细胞则无此能力。在人类胃癌组织中,AQP5在肠型和弥漫型胃癌及其转移灶中显著高表达,且细胞定位异常,提示其与肿瘤恶性进展相关。
【2】JITC:科学家发现能改善人类子宫内膜癌疗法的新型生物标志物
doi:10.1136/jitc-2024-010541
抗血管生成联合免疫检查点阻滞疗法已经成为标准基于铂的化疗后复发性子宫内膜癌的标准治疗方法。近日,一篇发表在国际杂志Journal for ImmunoTherapy of Cancer上题为“Immunological biomarkers of response and resistance to treatment with cabozantinib and nivolumab in recurrent endometrial cancer”的研究报告中,来自西奈山Icahn医学院等机构的科学家们通过研究发现了能改善人类子宫内膜癌疗法的新型生物标志物,相关研究结果或能帮助临床医生针对复发性子宫内膜癌患者选择更好的疗法。
文章中,研究者发现,血液中的特殊蛋白(识别出的新型生物标志物)或能帮助预测患者对两种抗癌药物组合疗法的反应,即药物卡博替尼(cabozantinib)和纳武单抗(nivolumab)的组合性疗法。子宫内膜癌是美国最常见的妇科癌症,每年影响着超过6.6万名女性的健康,据美国癌症协会推测,2025年美国将会有大约69,120名新发病例和13,860名因子宫内膜癌死亡病例;尽管免疫疗法是一种主要的疗法选择,但其并不是对每个人都有效,很多患者会经历疾病的复发,本文研究中,研究人员首次分析了能帮助临床医生个性化治疗并改善患者治疗结局的特殊血液标志物。
科学家们发现,接受纳武单抗治疗的患者与接受组合性疗法治疗的患者机体血液中的蛋白质的表现行为不同,在治疗前,体内与巨噬细胞相关的特定蛋白质水平较低的患者对药物组合的反应较高,而一些患者体内含有特殊的免疫激活标志物,这或许就能帮其更有效地抵御癌症从而延长生存期,巨噬细胞是一类在机体免疫细胞中扮演重要作用的白细胞。此外,与中性粒细胞(另一种在免疫系统中扮演重要角色的白细胞)相关的高水平蛋白质或与疗法所产生的更多副作用有关,值得注意的是,这种组合性疗法对此前接受其它疗法没有疗效的一些患者而言或许是有效的。
【3】Nat Commun:lncRNA或能作为人类肝细胞癌的潜在生物标志物和特殊治疗性靶点
doi:10.1038/s41467-025-57367-8
肝细胞癌(HCC,Hepatocellular carcinoma)是全球癌症相关死亡的第三大原因,其凶险程度仅次于肺癌和胃癌;这种起源于肝脏的恶性肿瘤,常因慢性肝炎病毒感染(尤其是乙肝病毒)而发生,且患者一旦确诊往往已处于疾病晚期阶段,目前患者5年的生存率不足50%。近年来,随着免疫治疗的兴起,科学家们逐渐认识到肿瘤微环境(Tumor Microenvironment, TME)在癌症发展中的关键作用,然而HCC的免疫逃逸机制仍然复杂且不完全清楚。
近日,一篇发表在国际杂志Nature Communications上题为“HBV-associated hepatocellular carcinomas inhibit antitumor CD8+ T cell via the long noncoding RNA HDAC2-AS2”的研究报告中,来自中国科学院生物物理研究所等机构的科学家们通过研究揭示了一种新型长非编码RNA(lncRNA)—HDAC2-AS2在HCC中的作用机制,相关研究结果为肝癌治疗带来了新的曙光。
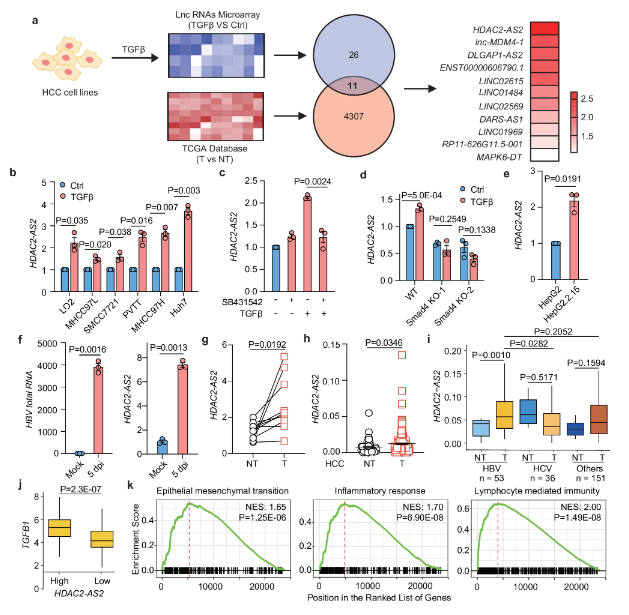
HDAC2-AS2能被TGFβ上调
肿瘤微环境是肿瘤细胞赖以生存的“土壤”,其中包含免疫细胞、细胞外基质和各种信号分子。在HCC中,肿瘤细胞能通过复杂的机制抑制免疫系统的功能从而实现免疫逃逸;长非编码RNA(lncRNA)是一类不编码蛋白质的RNA分子,近年来其被发现广泛参与肿瘤的发生、发展和免疫逃逸,然而lncRNA在HCC中的具体作用机制研究人员仍不清楚。为此研究人员通过研究聚焦于这一问题试图解开HCC免疫逃逸的“密码”。文章中,研究人员首先筛选了多种HCC细胞系,他们发现一种名为HDAC2-AS2的lncRNA在TGF-β信号通路激活后表达显著上调。TGF-β是一种重要的细胞因子,其在肝癌的发生和发展中起着关键作用,研究人员发现,HDAC2-AS2的高表达与HCC患者的不良预后密切相关,但在肿瘤细胞增殖中并无直接影响;这一现象引起了研究人员的极大兴趣,他们推测HDAC2-AS2或会通过其它机制来影响肿瘤的进展。
【4】Science:一种新发现的生物标志物可以预测脑膜瘤和乳腺癌的侵袭性
doi:10.1126/science.ads2169
在一项新的研究中,来自福瑞德-哈金森癌症研究中心和德克萨斯大学MD安德森癌症中心的研究人员利用一种新技术和计算方法,发现了一种能够准确预测脑膜瘤和乳腺癌结果的生物标志物。具体而言,他们指出组蛋白基因上发现的RNA聚合酶II(RNAPII)的数量与肿瘤的侵袭性和复发有关。相关研究结果发表在2025年2月14日的Science期刊上,论文标题为“RNA polymerase II at histone genes predicts outcome in human cancer”。
这些组蛋白基因上RNAPII的超高水平表明癌症过度增殖,并可能导致染色体改变。这些发现表明,使用一种新的基因组技术作为潜在的癌症诊断和预后工具,可能提高精准肿瘤学方法的准确性。研究者Ye Zheng博士说,“人们忽视了组蛋白基因可能是细胞复制的限速因素,反过来又是肿瘤细胞过度增殖的有力指标。这是因为目前的RNA测序方法由于组蛋白RNA的独特结构而无法检测到它们,这意味着这些文库大大低估了它们的存在。我们的新方法结合了新的实验技术和计算管道,建立了一个全面的生态系统,可以利用多种癌症类型的活组织样本来提高肿瘤诊断和预后。”
这项研究的结果是由福瑞德-哈金森癌症研究中心基础科学部的论文共同第一作者Steven Henikoff博士在实验室开发的一种新的分析技术实现的,该技术使得研究人员能够使用福尔马林固定的石蜡包埋(FFPE)样本更好地研究基因表达。
【5】Cell:新研究揭示了一种驱动侵袭性骨肉瘤的新机制,并提出一种预测骨肉瘤预后的新型生物标志物
doi:10.1016/j.cell.2024.12.005
骨肉瘤是一种侵袭性癌症,最常见于10岁至20岁的儿童和年轻人,正值骨骼快速生长时期。虽然罕见,但它对年轻人及其家人产生了重大影响,因为治疗可能需要手术或截肢。骨肉瘤也有可能扩散到其他器官,最常见的是肺部。由于骨肉瘤在基因组上非常复杂,因此很难确定是什么基因突变导致了这种疾病。因此,在过去的40年里,治疗选择几乎没有进展。
在一项新的研究中,来自EMBL-EBI、伦敦大学学院、皇家国家骨科医院和英格兰基因组学研发实验室的研究人员解决了导致骨肉瘤肿瘤侵袭性发展和进化的基因组重排的驱动因素之谜。通过分析骨肉瘤患者的最大全基因组数据集,他们发现了一种新的称为LTA(loss-translocation-amplification)染色体碎裂的突变机制,这种机制存在于大约50%的高级别骨肉瘤病例中。
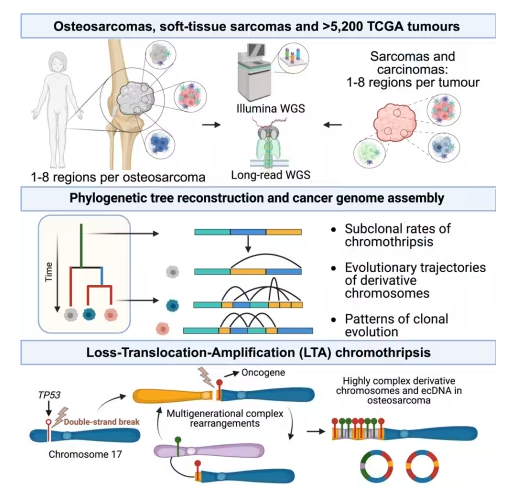
相关研究结果于2025年1月14日在线发表在Cell期刊上,论文标题为“Ongoing chromothripsis underpins osteosarcoma genome complexity and clonal evolution”。这一发现解释了使这种肿瘤类型如此具有侵袭性的独特生物学,以及在骨肉瘤癌细胞中观察到的高水平基因组不稳定性。这项研究还提供了一种预后生物标志物—癌细胞中可以帮助预测患者预后的生物学特征,这可能用于预测这种疾病的可能过程。
研究者Isidro Cortes Ciriano说,“多年来,我们已经知道骨肉瘤细胞具有人类癌症中最复杂的基因组,但我们无法解释其背后的机制。通过研究每个肿瘤不同区域的遗传异常,并使用让我们读取长片段DNA的新技术,我们能够了解染色体是如何断裂和重新排列的,以及这如何影响骨肉瘤的疾病进展。”
【6】Nature子刊:利用从唾液中发现的SNP标志物可能预测一个人患癌症、心血管疾病、糖尿病和神经退行性疾病的风险
doi:10.1038/s41525-025-00509-0
在一项新的研究中,由巴斯克大学领导的一个研究团队在唾液中发现了数百种分子标志物,这些分子标志物可能揭示一个人患癌症、心血管疾病、糖尿病和神经退行性疾病等重大疾病的风险。他们的研究成果为开发一种强大且无创的早期诊断和精准医学工具奠定了基础。相关研究结果发表在npj Genomic Medicine杂志上。
研究者José Ramón Bilbao表示,唾液是最易获取的生物体液之一,但在临床实践中仍未得到充分利用。我们的研究结果表明,唾液中的分子标志物能够反映口腔以外的全身性病理过程。众所周知,唾液样本常用于进行遗传测试以确定亲子关系等事情,但正如这项研究所显示的那样,基于唾液的临床分析潜力远不止于此。
Bilbao及其团队分析了超过350人的唾液样本,并整理了可能影响唾液中基因组功能的常见DNA变异,即单核苷酸多态性(SNP)。具体而言,他们发现这些多态性如同开关,可激活或抑制其影响的基因功能。
将这项研究的数据与先前大型国际遗传学研究中关于慢性疾病风险的结果进行对比后,他们观察到,唾液中检测到的许多相同多态性与前列腺癌、冠心病、帕金森病和2型糖尿病等常见疾病的较高发病风险相关。
【7】一滴血就能查乳腺癌?新型微流控芯片做到了!仅需50 μL血浆、35分钟出结果,还能精准检测外泌体多个生物标志物!
doi:10.1016/j.aca.2025.343743
在生活节奏日益加快的当下,女性面临着来自工作、家庭等多方面的压力,健康问题也愈发值得关注。乳腺癌作为女性最常见的恶性肿瘤之一,其发病率呈逐年上升趋势,严重威胁着女性的生命健康。早期准确诊断乳腺癌,能够为患者争取更有效的治疗时机,显著提高生存率。然而,传统的乳腺癌诊断方法,如乳腺钼靶、穿刺活检等,要么存在一定的辐射风险,要么具有侵入性,给患者带来身体和心理上的双重负担。因此,寻找一种快速、准确且非侵入性的诊断技术迫在眉睫。
近期,发表于Anal Chim Acta的一项研究Immunofluorescent analysis of exosomes using a microchip filled with transparent antibody-conjugated beads for breast cancer liquid biopsy为解决这些难题带来了新的思路。吉林大学的科研团队研发出一种新型微流控免疫分析芯片(Exo-MIC),旨在实现血浆样本中外泌体的连续、快速、高效富集与检测,为癌症及其他疾病的早期诊断提供有力支持。
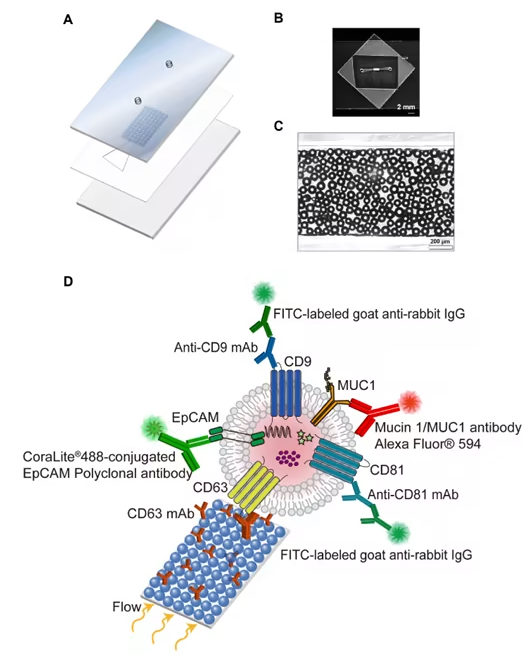
微流控芯片装置示意图和外泌体检测示意图
Exo-MIC的设计十分巧妙,它由玻璃基板、丙烯酸盖和中间的通道层构成,采用压敏粘合剂(PSA)键合法制备。芯片的反应腔内填充了透明的抗体偶联微珠,这些微珠能够干扰液体样本的层流状态,提升传质效率,扩大免疫亲和反应的接触面积,进而增强抗体与靶蛋白的结合力,聚焦荧光信号,有效提高检测的灵敏度和效率。
【8】Mol Cell:识别出能预测肝癌患者对免疫疗法反应的特殊生物标志物
doi:10.1016/j.molcel.2024.09.026
肝细胞癌(HCC,hepatocellular carcinoma)起源于慢性炎症,肝星状细胞(HSCs,hepatic stellate cells)的激活是通过形成促肿瘤发生的微环境所发挥作用的,这一过程的关键就是p62,其失活会导致肝癌的发生。
近日,一篇发表在国际杂志Molecular Cell上题为“Opposing regulation of the STING pathway in hepatic stellate cells by NBR1 and p62 determines the progression of hepatocellular carcinoma”的研究报告中,来自美国威尔康乃尔医学院等机构的科学家们通过进行一项临床前研究有望确定哪些肝细胞癌患者能因免疫疗法的治疗而获益。相关研究为深入研究一对p62和NBR1蛋白提供了新的见解,同时还阐明了其在调节肝星状细胞中干扰素反应中的相反功能,肝星状细胞是机体肝脏抵御肿瘤的关键免疫组分。
本文研究结果表明,这些特化细胞中高水平的免疫抑制性NBR1或能帮助识别出哪些患者不太可能会对免疫疗法产生反应;而且降低NBR1的策略还能帮助促使动物模型中的肿瘤发生萎缩,这或许就有望为那些不会对免疫疗法产生反应的患者亚群提供一种潜在的新型治疗手段。研究者Jorge Moscat教授指出,p62和NBR1是阴和阳,与NBR1相反,如果p62在肝星状细胞中含量较高的话,患者就不会患癌,但如果其含量较低,患者机体的免疫系统就会被破坏,如果NBR1含量较高,患者机体的免疫系统就会受损,但如果NBR1含量较低,患者机体的免疫反应就会增强。
【9】Brief Bioinform:利用基因组测序和AI分析或能揭示隐藏在乳腺癌发病背后的特殊遗传标志物
doi:10.1093/bib/bbae346
乳腺癌是如今影响西方女性健康最常见的恶性肿瘤,据估计,有高达10%的乳腺癌病例的发生归因于种系突变(germline variants),然而大多数家族性乳腺癌病例的遗传基础研究人员并不确定,因此发现促进家族性乳腺癌的易感基因或具有一定的挑战性,因为其被认为是非常罕见的、较低的外显率和复杂的生物学机制。
近日,一篇发表在国际杂志Briefings in Bioinformatics上题为“Discovering predisposing genes for hereditary breast cancer using deep learning”的研究报告中,来自耶路撒冷希伯来大学等机构的科学家们通过研究开发了一种新方法来分析乳腺癌高发的家族个体机体的遗传突变,通过分析12个家庭的1218个遗传突变,研究人员识别出了80个基因与乳腺癌风险增加有关,同时他们还强调了过氧化物酶体和线粒体通路在乳腺癌易感性和患者生存中的重要作用,这在以前被研究人员完全忽视了。
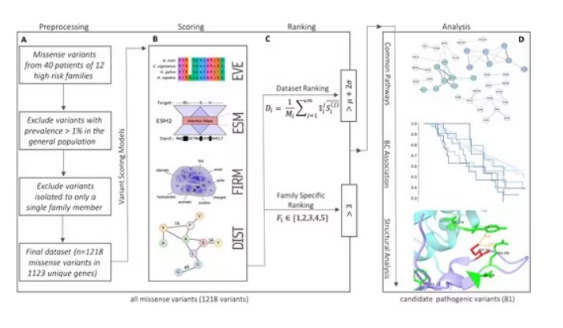
突变分析流程
本文研究结果或能为阐明家族性乳腺癌背后的遗传基础提供了新的见解,尤其是其在中东血统的家庭中普遍存在;文章中,研究人员利用一种创新性的分析方法专门用来分析有乳腺癌发病史的家庭个体机体的遗传突变,这种方法结合了先进的机器学习技术和对蛋白质结构的详细分析,旨在调查罕见的遗传突变。通过对12个家庭中发现的1218个突变进行仔细分析,研究人员识别出了80个基因或会明显影响机体的乳腺癌风险,这一研究发现包括了70个此前未知的与乳腺癌相关的基因,这或许就极大扩散了研究人员对这种疾病遗传背景的理解。
【10】Front Med:对DNA损伤修复基因进行表观遗传学沉默或能揭示一种胰腺癌疗法的潜在标志物
doi:10.1007/s11684-023-1053-3
合成致死性(Synthetic lethality)是一种新型癌症疗法模式。近日,一篇发表在国际杂志Frontiers of Medicine上题为“Epigenetic silencing of BEND4, a novel DNA damage repair gene, is a synthetic lethal marker for ATM inhibitor in pancreatic cancer”的研究报告中,来自中国人民解放军总医院等机构的科学家们通过研究发现,BEND4的表观遗传学沉默或能作为一种潜在的合成致死性标记物,从而增强ATM抑制剂治疗胰腺癌的疗效。
文章中,研究人员提供了一种新方法来靶向作用名为BEND4的肿瘤抑制基因,BEND4在胰腺癌中会频繁甲基化和沉默。研究人员深入揭示了BEND4在DNA损伤修复中所扮演的关键角色,以及其与ATM抑制剂疗法联合治疗时作为指标性标志物的潜力。研究人员利用了综合性的方法进行研究,包括细胞系实验、组织样本分析和体内研究等,他们评估了BEND4在多种胰腺癌细胞系和组织中的表达和甲基化状态,结果发现BEND4甲基化与患者机体肿瘤分化不良之间存在显著关联。
此外,BEND4的甲基化也被识别为胰腺导管腺癌(PDAC)患者机体中独立的预后较差标志物;研究结果表明,BEND4能抑制PDAC细胞的生长,诱导G1/S阻滞和细胞凋亡,同时还能抑制癌细胞的迁移和侵袭,其背后的机制涉及BEND4与Ku80之间的相互作用,Ku80是非同源末端连接(NHEJ,non-homologous end joining)途径的关键参与者,而该通路是一种主要的DNA双链断裂(DSB)修复通路。研究者指出,BEND4的过量表达能增强NHEJ的效率,而对其进行敲除则会降低NHEJ的效率,从而就突出了BEND4在DNA损伤修复过程中扮演的关键角色。(生物谷Bioon.com)
生物谷更多精彩盘点!敬请期待!
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


