Nature:揭示特殊的大肠杆菌驱动机体结直肠癌发生背后的分子机制
来源:生物谷原创 2024-11-29 11:57
本文研究结果或为开发抗粘附素疗法提供了新的治疗途径,这种新型疗法旨在减轻基因毒素colibactin所诱导的DNA损伤并能抑制结直肠癌的开始和进展,尤其是有患结直肠癌风险的个体。
多种细菌会被认为会促进结直肠癌的发生,包括pks+大肠杆菌,其能产生基因毒素colibactin从而诱导宿主机体的上皮细胞发生特征性突变,然而,目前研究人员并不清楚这种高度不稳定的基因毒素colibactin分子是如何进入到宿主上皮细胞并引起损伤的。
近日,一篇发表在国际杂志Nature上题为“Colibactin-driven colon cancer requires adhesin-mediated epithelial binding”的研究报告中,来自比利时根特大学等机构的科学家们通过研究揭示了肠道中某些大肠杆菌是如何通过结合肠道细胞并释放一种DNA破坏性毒素,从而来促进机体结肠癌发生的,相关研究揭示了一种潜在降低癌症风险的新方法。
结肠癌是第三大最常见和最致命的癌症类型,让人震惊的是,其发病率不断上升,尤其是在年轻人群体中;新出现的研究证据表明,肠道微生物(肠道中主要的健康细菌集合)群中的某些细菌或能通过在很大程度上未知的机制来促进结肠癌的发生。其中一种被怀疑有致癌特性的细菌就是pks+大肠杆菌(pks+ E. coli),其能产生名为colibactin的基因毒素,colibactin能结合并损伤人类的DNA,并引起增加癌症风险的突变,这些细菌及其所引起的突变在结肠癌患者体内会明显过量存在。
截止到目前为止,科学家们并不清楚pks+大肠杆菌是如何抵达并损伤肠壁从而促进癌症发生的,这项研究中,研究人员进行实验发现,这些细菌能在自由游动状态和吸附到肠道组织内衬(肠道上皮)的模式之间不断切换,这种吸附是通过特定的细菌菌毛所实现的,细菌菌毛事一种细菌表面长而薄的蛋白纤维,最终就会形成粘附素(adhesins)从而与肠道上皮细胞中的受体相结合。研究者Maude Jans博士说道,我们发现,这种菌毛的结合会明显增加结肠肿瘤的数量、尺寸和侵袭性。
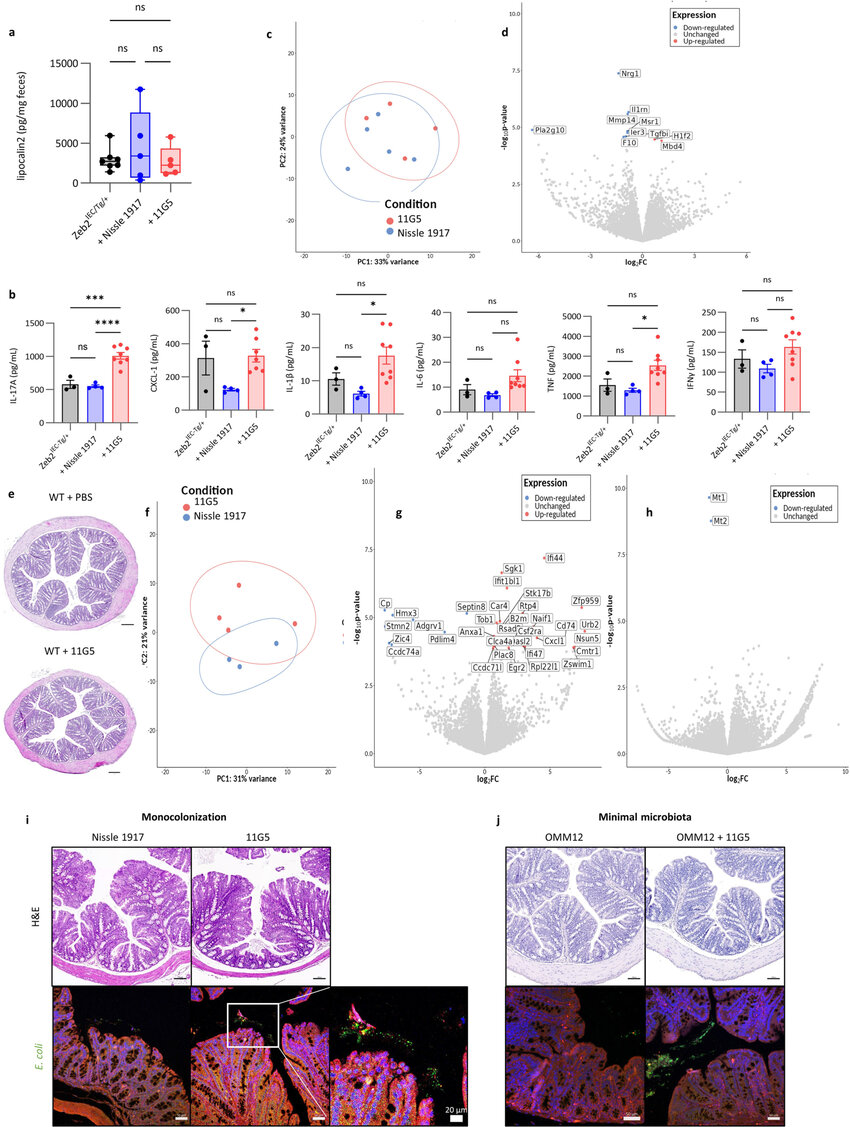
大肠杆菌11G5感染并不会增加Zeb2IEC-Tg/+小鼠机体的结肠炎症,也并不会影响野生型幼崽机体的上皮组织
本文研究结果表明,pks+大肠杆菌与肠道上皮的结合被认为是结肠癌发生的关键一步,研究人员发现,通过干扰这些细菌附着机制,肿瘤的发生就会被大大减弱。如今研究人员就能识别出介导与结肠细胞结合的特殊细菌粘附素,即FimH和FmlH,他们推测,这些粘附素的结合就允许细菌在上皮细胞附近产生基因毒素colibactin,最终导致DNA损伤和癌症的发生。研究人员还指出,移除这些粘附素就会剥夺细菌运输colibactin并促进DNA损伤的能力。
基于这些研究发现,研究人员利用能阻断这些必要细菌粘附素结合的分子测试了一种治疗性手段来预防细菌的粘附,值得注意的是,他们能在临床前模型中明显抑制DNA的损伤和肿瘤发生,这种治疗方法非常有前途,因为其能成功靶向作用有害的大肠菌群菌株,且并不会影响机体有益的肠道菌群,并不像抗生素那样。此外研究人员还强调道,西方生活方式会让机体的肠壁更容易受到包括pks+大肠杆菌在内的有害细菌的侵袭。这项最新研究结果还揭示了这一领域存在的一个普遍的谜团,即一些被批准用作益生菌(被认为能促进机体健康的活细菌)的大肠杆菌携带有pks基因,但在实验室实验中却并不会增加机体的患癌风险。
研究者Remaut教授说道,我们发现,这些菌株的确会制造colibactin毒素,并且能表达治病菌株将毒素运输到上皮细胞中的FimH和FmlH粘附素;事实证明,这些菌株含有一种名为FimH的突变体,这种突变体的作用效果并不好,因为colibactin毒素或许无法抵达其靶点。然而,研究人员表明,仅仅几个突变就足以恢复这些菌株中FimH强大的结合力和基因毒素的活性,这就强调了其作为良性益生菌或许应该需要重新被考虑。
综上,本文研究结果或为开发抗粘附素疗法提供了新的治疗途径,这种新型疗法旨在减轻基因毒素colibactin所诱导的DNA损伤并能抑制结直肠癌的开始和进展,尤其是有患结直肠癌风险的个体。(生物谷Bioon.com)
参考文献:
Jans, M., Kolata, M., Blancke, G. et al. Colibactin-driven colon cancer requires adhesin-mediated epithelial binding. Nature (2024). doi:10.1038/s41586-024-08135-z.
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


