《细胞·代谢》:南医大/武大团队发现肝癌代谢重编程的新机制!
来源:奇点糕 2023-05-25 16:47
驱动肝细胞癌(HCC)代谢重编程的关键因素找到了!
驱动肝细胞癌(HCC)代谢重编程的关键因素找到了!
近期,南京医科大学王学浩/浦立勇/钱晓峰/王科及武汉大学张鹏团队发表了一篇文章,他们通过大规模转录组数据库和生存相关性筛选,确定了胸苷激酶1(TK1)是HCC代谢重编程的关键驱动因素,下调TK1的表达能延缓HCC的进展。
此外,研究还发现,TK1不仅通过其酶活性和脱氧胸腺嘧啶核苷酸(dTMP)的产生促进HCC的发生,还可以不在酶的作用下直接与蛋白精氨酸甲基转移酶1(PRMT1)结合促进糖酵解,为HCC生长提供能量。
了解TK1的酶依赖性和非依赖性分子机制可以帮助我们开发或制定不同的HCC治疗策略。研究发表在《细胞·代谢》上。

论文首页截图
HCC是世界上最常见的癌症相关死亡原因之一,每年确诊患者达80多万。尽管免疫治疗、手术切除、肝移植等治疗方法能够改善HCC患者预后,但肿瘤复发率仍然很高。因此,找到治疗HCC的新方法和新靶点,变得尤为重要。
代谢重编程是HCC的关键特征。为了迅速扩张自己的领地,肿瘤细胞会改变自己的代谢方式,以确保有足够的营养来满足生长和传播的需要。而针对这种代谢方式改变的治疗方法也为HCC的治疗提供了一个新的方向。
鉴于此,南京医科大学和武汉大学的研究人员将研究的重点放在了找出与HCC代谢重编程有关的基因上。
为了筛选出与HCC进展有关的基因,研究人员从多个公共数据库中选取了样本量(HCC和邻近正常组织)大于150,基因覆盖率较高的数据集进行研究,最终在前5个上调的与HCC发生密切相关的基因中选中了TK1,一方面TK1与恶性肿瘤行为、代谢重编程和不良预后有关,另一方面,TK1是里面唯一一个没有被重视的基因。
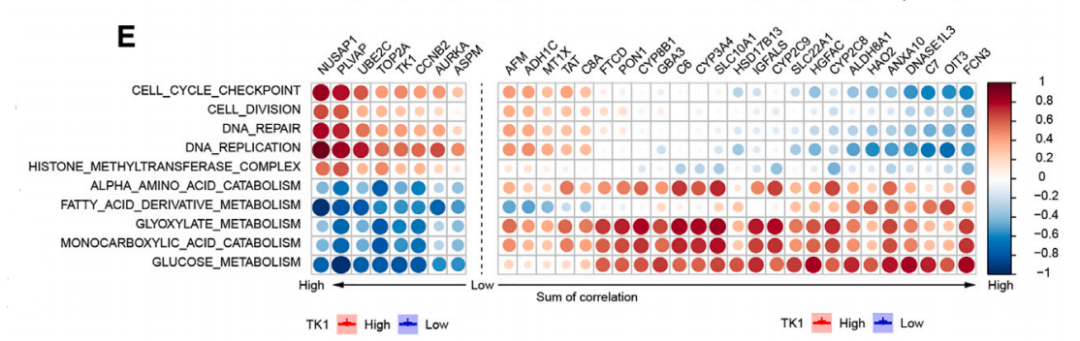
与HCC发生密切相关的基因
接下来,研究人员在TCGA和ICGC数据库中验证了TK1在HCC中的表达水平的确要高于邻近正常组织。根据TK1表达水平的不同,研究将以上两个数据库中的样本分成了TK1高表达组和TK1低表达组。
结果发现,TK1高表达组个体的生存预后要明显低于TK1低表达组,且TK1高表达组显现出与癌症进展和代谢重编程相关的显著富集生物过程,这也意味着TK1在HCC进展中起着至关重要的作用。
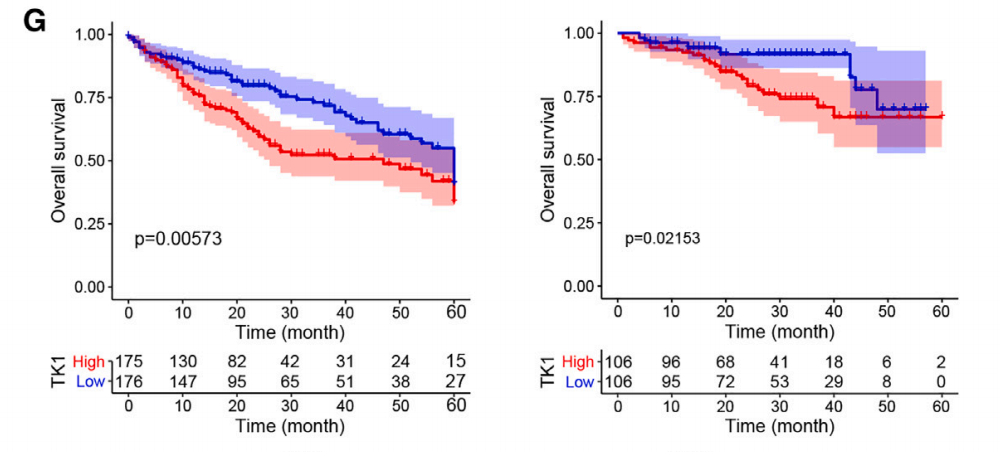
TK1表达与个体的生存预后的关系
在收集了90对HCC样本和对应的邻近组织样本后,研究人员观察到HCC组织中TK1的mRNA表达水平明显高于相邻的正常组织,这进一步验证了TK1在HCC中的表达上调。
那么是什么原因导致TK1在HCC中上调呢?
根据cBioPortal数据库信息,研究人员评估了TK1 mRNA表达与DNA甲基化水平之间的关联。结果发现,TK1基因的表达与DNA甲基化水平呈显著负相关(p=2.0e-14)。
利用亚硫酸氢盐测序法PCR(BSP)和甲基化特异性PCR(MSP)确定HCC标本中TK1启动子的甲基化状态后,研究人员发现,与邻近正常组织相比,HCC中TK1启动子序列发生了低甲基化,且TK1启动子甲基化水平与TK1表达成负相关,这说明,HCC中TK1基因的表达水平上升可能是由于其启动子序列低甲基化造成的。
既往研究显示,TK1可促进体外HCC细胞的增殖和迁移,为了评估TK1是否能促进HCC在体内的增殖能力,研究将TK1敲低的Hep3B细胞、过表达TK1的YY8103细胞及其相应的对照HCC细胞接种到裸鼠中。
结果发现,在TK1敲低组中,可以观察到肿瘤体积和重量的下降,TK1过表达组则相反。HE染色、免疫组化分析显示,下调TK1可抑制HCC细胞的增殖能力,提高HCC细胞的凋亡率。在肺转移小鼠模型中,研究人员同样观察到下调TK1可抑制HCC生长以及肺转移。
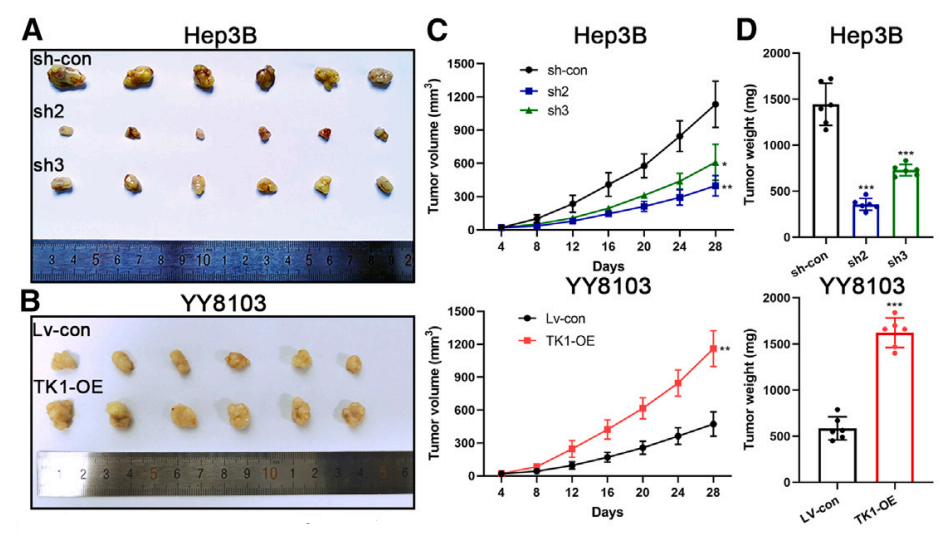
TK1表达水平与肿瘤大小的关系
为了进一步揭示TK1在HCC进展中的作用,研究对YY8103细胞系进行了无标记蛋白质组学分析,并通过GO富集分析确定了最显著富集的生物过程是代谢过程。于是,研究人员对YY8103细胞系进行了非靶向代谢组学分析后发现,随着TK1表达水平的改变,代谢谱也发生了变化。KEGG通路分析显示,癌症中心碳代谢(CCM)变化最大。
CCM主要涉及糖酵解、磷酸戊糖途径和柠檬酸循环这三个途径,其中糖酵解是肿瘤细胞中最典型的代谢途径。为了检测TK1对糖酵解的直接影响,研究人员进行了代谢通量分析、18F-FDG PET/CT的测定以及结合临床HCC患者队列数据后发现,无论在体外还是体内,TK1均有助于糖酵解。
我们知道TK1具有典型激酶活性,以往的研究均集中在TK1催化dTMP产生的作用上,为了确定TK1促进HCC进展和糖酵解这一过程是否需要酶的参与,研究人员构建了TK1的野生型(WT)和激酶失活变体(MUT#1),重组到Hep3B细胞和YY8103细胞中。
结果发现,TK1-WT和TK1-MUT#1过表达均增强了肿瘤细胞的增殖、迁移和糖酵解,只不过与TK1-WT相比,TK1-MUT#1作用相对较弱。这说明,TK1不仅可以通过其酶活性,还可以通过与酶无关的机制促进HCC进展和糖酵解。
接下来,研究人员进一步对YY8103细胞进行了免疫共沉淀-质谱联用(IP-MS)分析,再结合蛋白质组学分析结果,确定了PRMT1是与TK1相互作用并受到TK1调节的蛋白质。此外,研究还通过实验验证了TK1与PRMT1之间存在直接相互作用。
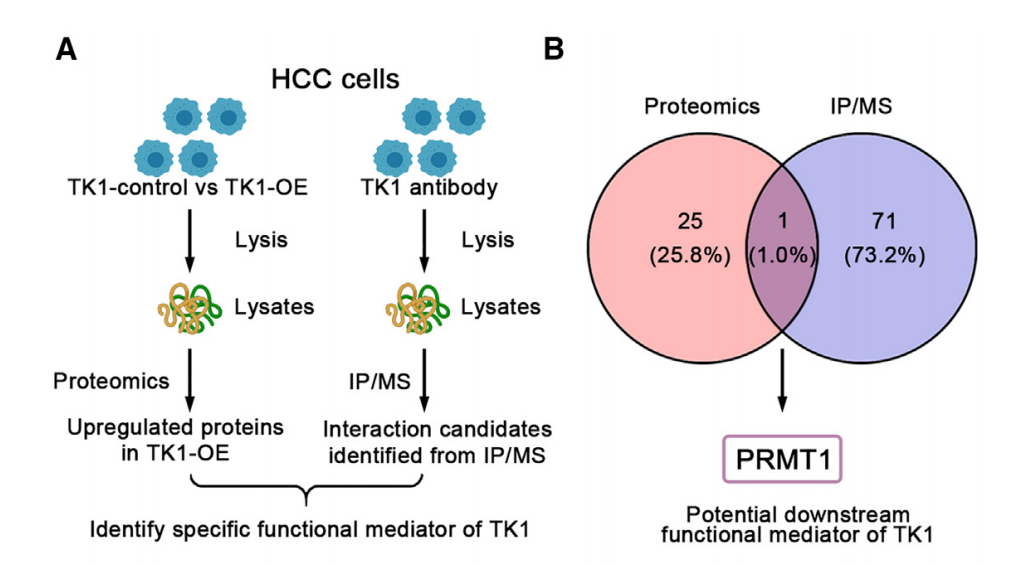
PRMT1是受TK1调节的蛋白质
具体来说,TK1又是如何调控PRMT1的呢?
研究人员用蛋白印记检测了TK1过表达时PRMT1的表达情况,结果发现,当TK1过表达时,PRMT1蛋白表达增加、PRMT1泛素化降低(稳定性增高)。鉴于TK1不能直接影响蛋白泛素化,研究人员推测这中间还存在一个去泛素化酶(DUB)辅助调控PRMT1的表达。
有研究显示,正常情况下,TRIM48可与PRMT1的甲基转移酶结构域相互作用,调控PRMT1的泛素化和降解。在本文中,研究人员发现TK1过表达,显著降低了TRIM48-PRMT1的相互作用,进而减缓了PRMT1的降解。所以研究人员推测TK1通过中断TRIM48介导的泛素化和PRMT1的降解来稳定PRMT1。
为了验证这项发现的临床相关性,研究人员分析了人HCC组织中TK1和PRMT1的表达水平。结果发现TK1的表达水平与PRMT1的表达呈正相关,且TK1或PRMT1低表达的患者普遍预后更好,这说明TK1和PRMT1表达水平可能作为识别HCC患者预后的生物标志物。此外,研究人员利用小鼠肝癌模型探究TK1敲除对HCC的治疗潜力。结果发现,TK1敲除后小鼠生存率得到了提升。
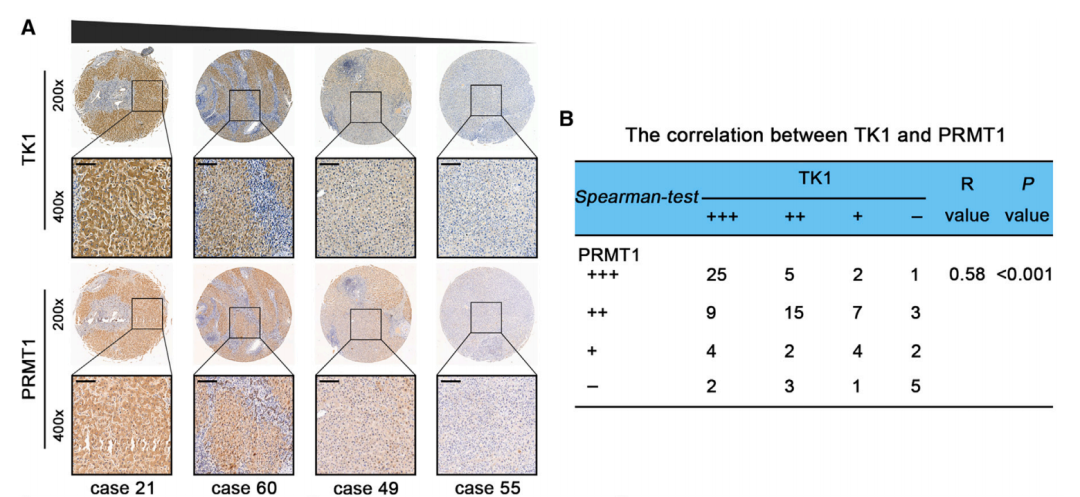
TK1的表达水平与PRMT1的表达呈正相关
总之,该研究不仅发现了HCC代谢重编程的关键驱动因子TK1,还揭示了TK1在HCC发展中的双重作用机制,即通过酶依赖性和不依赖于酶的方式促进HCC恶性进程和糖酵解。未来可以通过靶向这两种分子机制来发展不同的HCC治疗策略。让我们拭目以待吧~
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


