Alkermes重度抑郁新药提交上市申请 有望近期上市
Alkermes公司今天宣布向FDA提交滚动上市申请,以寻求治疗重度抑郁障碍(MDD)新药ALKS 5461的批准。ALKS 5461有全新的作用机制,可以作为治疗重度抑郁障碍的辅助疗法。Alkermes公司希望在2017年年底前完成该新药的申请。抑郁症是一个非常普遍,然而又被忽视的大众性疾病。全世界范围,高达3至4亿的人口饱受抑郁的困扰,多数患者对标准疗法不应答。根据DSM-5(Di
武田在日本提交抗炎药Entyvio(vedolizumab)上市申请,治疗中度至重度溃疡性结肠炎(UC)
2017年8月25日/生物谷BIOON/--日本制药巨头武田(Takeda)近日宣布,已向日本劳动卫生福利部(MHLW)提交了人源化单克隆抗体药物vedolizumab治疗中度至重度溃疡性结肠炎(ulcerative colitis,UC)成人患者的新药申请(NDA)。此次NDA的提交,是基于一项多中心、随机、双盲、安慰剂对照、平行组III期临床研究CCT-101的数据。该研究在292
FDA受理安进CGRP抗体上市申请
新闻事件今天FDA受理了安进和合作伙伴诺华的偏头痛预防药物、CGRP抗体erenumab(商品名Aimovig)的上市申请,PDUFA日期为2018年5月17日,这令Aimovig有望成为第一个上市的CGRP抗体。共2600多病人参与的多个临床试验显示Aimovig可以减少发病次数、致残比例、和急救药物使用。Aimovig安全性较好,常见副反应包括呼吸道感染、注射疼痛、恶心等。据估计CGRP市场总
美国FDA受理辉瑞抗炎药Xeljanz治疗中重度活动性溃疡性结肠炎(UC)上市申请
2017年7月14日讯 /生物谷BIOON/ --美国制药巨头辉瑞(Pfizer)近日宣布,美国食品和药物管理局(FDA)已受理其口服JAK抑制剂Xeljanz(tofacitinib)的一份补充新药申请(sNDA),该申请寻求FDA批准Xeljanz用于中度至重度活动性溃疡性静脉炎(UC)成人患者的治疗。FDA已指定这份sNDA的处方药用户收费法(PDUFA)为2018年3月。值得一
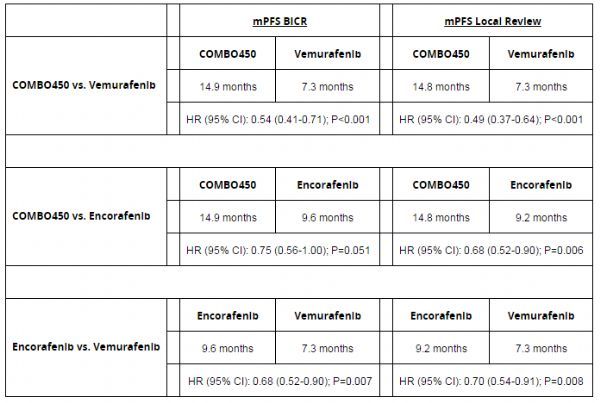
Array向美国FDA提交黑色素瘤组合疗法COMBO450上市申请
2017年7月6日 讯 /生物谷BIOON/ --Array生物制药公司近日宣布,已向美国食品和药物管理局(FDA)提交了每日2次45mg剂量binimetinib与每日一次450mg剂量encorafenib的组合疗法(COMBO450)治疗BRAF突变、晚期、不可切除性或转移性黑色素瘤患者的新药申请(NDA)。如果获批,该组合疗法将为BRAF突变阳性晚期黑色素瘤患者群体提供一个新的
美FDA受理Celltrion和梯瓦美罗华生物仿制药CT-P10上市申请
以色列制药巨头梯瓦(Teva)与合作伙伴韩国生物制药公司Celltrion近日联合宣布,美国食品和药物管理局(FDA)已受理单克隆抗体生物仿制药CT-P10的生物制品许可申请(BLA),该药是罗氏最畅销的单抗药物美罗华(Rituxan,通用名:rituximab,利妥昔单抗)的生物仿制药,后者适应症包括:非霍奇金淋巴瘤(NHL)、慢性淋巴细胞白血病(CLL)、类风湿性关节炎、肉芽肿性血
葛兰素史克向美国FDA提交Nucala(美泊利单抗)治疗嗜酸性肉芽肿血管炎(EGPA)的上市申请
2017年7月3日讯 /生物谷BIOON/ --英国制药巨头葛兰素史克(GSK)近日宣布已向美国食品和药物管理局(FDA)提交了白介素-5(IL-5)拮抗剂Nucala(mepolizumab,美泊利单抗)的一份补充生物制品许可申请(sBLA),寻求批准该药作为糖皮质激素的一种附加疗法,用于嗜酸性肉芽肿血管炎(EGPA)成人患者的治疗。EGPA即Churg-Strauss综合征,是一种
和黄癌症新药3期成功 将在中国申请上市
近日,药明康德合作伙伴公司Hutchison China MediTech(Chi-Med,和黄中国医药科技)在美国临床肿瘤学会(ASCO)年会上以口头报告形式公布了其新型血管内皮生长因子受体(VEGFR)激酶抑制剂fruquintinib的关键性3期研究结果。FRESCO是一项随机、双盲、安慰剂对照、多中心的3期试验,在中国评估了fruquintinib治疗局部晚期或转移性结直肠癌(CRC)患者
ViiV向美国和欧盟提交全球首个二合一HIV维持疗法上市申请
由葛兰素史克(GSK)、辉瑞(Pfizer)、盐野义(Shionogi)共同持股的HIV/AIDS药物研发公司ViiV Healthcare近日宣布,已向美国食品和药物管理局(FDA)提交了二合一HIV复方药物dolutegravir/rilpivirine的新药申请(NDA),同时已向欧洲药品管理局(EMA)提交了该药的上市许可申请(MAA),该药是全球首个仅由2种药物组成的HIV维持疗法。此次
EMA 受理山德士 2 款生物仿制药上市申请
诺华(Novartis)旗下仿制药单元山德士(Sandoz)近日宣布,欧洲药品管理局(EMA)已受理该公司提交的 2 款生物仿制药的上市许可申请(MAA),其中一款所对应的原研药是艾伯维的旗舰产品 Humira(修美乐,通用名:adalimumab,阿达木单抗),另一款所对应的原研药是默沙东和强生的重磅抗炎药 Remicade(类克,通用名:infliximab,英夫利昔单抗),这 2 种品牌药均