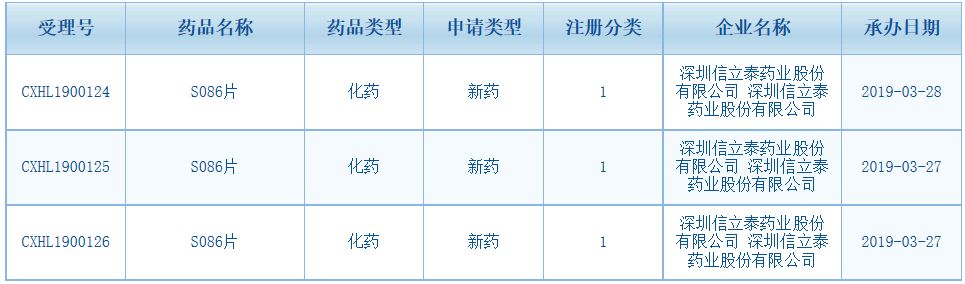
信立泰抗心衰新药S086&nbSp;用于原发性高血压获得临床许可
近期,信立泰发布公告称,公司申报的S086片“原发性高血压”适应症临床申请获得国家药品监督管理局(NMPA)的临床试验默示许可。据查询,本次新增适应症“原发性高血压”的临床申请于2019年3月获得CDE承办。公告透露,信立泰已完成S086片Ⅰ期临床相关研究,原发性高血压适应症准备进入Ⅱ期临床阶段。根据病因,高血压可分为原发性高血压和继发性高血压。继发性高血压
诺华新一代S1P受体调节剂Mayzent欧盟批准在即!
2019年11月18日/生物谷BIOON/--瑞士制药巨头诺华(NovartiS)近日宣布,欧洲药品管理局(EMA)人用医药产品委员会(CHMP)已发布积极审查意见,推荐批准Mayzent(Siponimod),用于以复发或炎症活动的影像学特征(例如,Gd增强的T1病灶或活动性、新的或扩大的T2病灶)为证据的活动性疾病的继发进展型多发性硬化症(SPMS)成人患者的治疗。尽管每例患者的MS进展不同,
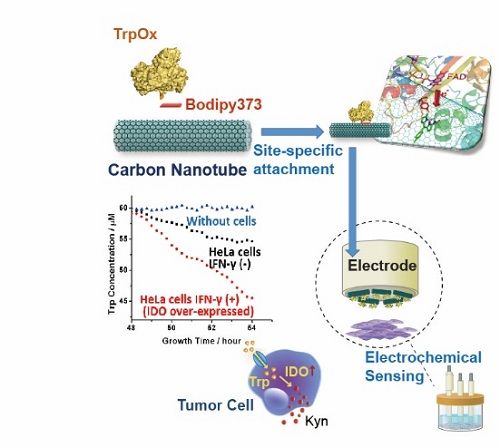
研究基于基因密码子扩展及新型生物正交反应“S-Click”方法改造氨基酸氧化酶
&nbSp;10月5日,《德国应用化学》(Angewandte Chemie International Edition)期刊以“Hot Article”的形式发表了中国科学院生物物理研究所王江云课题组题为S-click reaction for iSotropic orientation of oxidaSeS on electrodeS to promote electron tranSfer
强生S1P1调节剂poneSimod头对头III期疗效击败赛诺菲Aubagio(奥巴捷)!
2019年09月13日/生物谷BIOON/--欧洲多发性硬化症治疗与研究委员会(ECTRIMS)第35届会议于9月11-13日在瑞典斯德哥尔摩举行。此次会议上,美国医药巨头强生(JNJ)旗下杨森制药首次对外发布了研究性多发性硬化症(MS)口服药物poneSimod治疗复发型多发性硬化症(RMS)成人患者的头对头III期研究OPTIMUM的结果。poneSimod是一种新型、口服、选择性鞘氨醇-1-
沃特世推出全新Xevo&nbSp;TQ-S&nbSp;cronoS串联四极杆质谱仪
&nbSp;近日,沃特世公司(纽约证券交易所代码:WAT)隆重推出全新Xevo TQ-S cronoS和升级款Xevo TQ-S micro ,进一步扩充了公司旗下的串联四极杆质谱产品系列。此次推出的Xevo TQ-S cronoS是一款全新的串联四极杆质谱仪,擅长对较宽浓度范围内的各种小分子有机化合物进行常规定量分析。而备受市场赞誉的Xevo TQ-S micro则在此次升级中增强了性能,将定量
强生口服选择性S1P1调节剂poneSimod III期临床获得成功!
2019年07月27日/生物谷BIOON/--美国医药巨头强生(JNJ)旗下杨森制药近日公布了III期临床研究OPTIMUM的积极顶线结果。该研究在复发型多发性硬化症(RMS)成人患者中开展,比较了poneSimod与Aubagio(teriflunomide,特立氟胺)的疗效和安全性。Aubagio是赛诺菲的一款口服多发性硬化症药物。结果显示,该研究达到了主要终点和大多数次要终点。OPTIMUM
第四代EGFR抑制剂将入临床&nbSp;有望破解肺癌C797S耐药突变
&nbSp;&nbSp;一百年前,肺癌在医学的视野中还是一种罕见病。一百年后,非小细胞肺癌已跃居为全球多地发病率、死亡率最高的恶性肿瘤。表皮生长因子受体(epidermal growth factor receptor,EGFR)基因突变型患者,在非小细胞肺癌人群中占比极高(20-40%),因此每一代EGFR靶向抑制剂推向临床和市场,都是世人翘首期盼的重磅突破。第三代EGFR抑制剂问世后,终于从根
新基新型口服亚型选择性S1P受体调节剂ozanimod在美欧进入审查
2019年06月10日讯 /生物谷BIOON/ --新基(Celgene)近日宣布,美国FDA已受理ozanimod治疗复发型多发性硬化症(RMS)的新药申请(NDA),欧洲药品管理局(EMA)也已受理ozanimod治疗复发缓解型多发性硬化症(RRMS)的上市许可申请(MAA)。ozanimod是一种口服1-磷酸鞘氨醇(S1P)受体调节剂,能够以高亲和力选择性结合S1P亚型1(S1P1)和亚型5
新基新型口服S1P受体调节剂ozanimod再次提交美国上市申请
2019年03月31日讯 /生物谷BIOON/ --美国生物制药巨头新基(Celgene)近日宣布,已再次向美国食品和药物管理局(FDA)提交了一份新药申请(NDA),寻求批准ozanimod用于复发型多发性硬化症(RMS)成人患者的治疗。3月11日,该公司也向欧洲药品管理局(EMA)提交了ozanimod治疗复发缓解型多发性硬化症(RRMS)成人患者的上市许可申请(MAA)。ozanimod是新
新基新型多发性硬化症口服药物S1PR1/5调节剂ozanimod申请上市
2019年03月13日讯 /生物谷BIOON/ --美国生物制药巨头新基(Celgene)近日宣布,已向欧洲药品管理局(EMA)提交了一份营销授权申请(MAA),申请批准ozanimod用于复发缓解型多发性硬化症(RRMS)成人患者的治疗。ozanimod是新基2015年豪掷73亿美元收购ReceptoS公司的核心资产。在美国监管方面,2018年早些时候ozanimod遭到FDA拒绝,理由是非临床