研究基于基因密码子扩展及新型生物正交反应“S-Click”方法改造氨基酸氧化酶
来源:生物物理所 2019-10-09 18:37
10月5日,《德国应用化学》(Angewandte Chemie International Edition)期刊以“Hot Article”的形式发表了中国科学院生物物理研究所王江云课题组题为S-click reaction for isotropic orientation of oxidases on electrodes to promote electron transfer
10月5日,《德国应用化学》(Angewandte Chemie International Edition)期刊以“Hot Article”的形式发表了中国科学院生物物理研究所王江云课题组题为S-click reaction for isotropic orientation of oxidases on electrodes to promote electron transfer at low potentials 的研究文章。文中报道了该课题组开发的基于基因密码子扩展及新型生物正交反应“S-Click”方法改造氨基酸氧化酶,成功实现了氨基酸的快速、实时、精准的电化学检测。
氨基酸是重要的生理生化代谢与细胞信号分子,异常氨基酸代谢导致许多严重疾病,因此实时氨基酸分析对医学、诊断及生命科学具有重要意义。随着生命科学的不断发展,在国际期刊上关于氨基酸在细胞代谢、基础病理方面的重要性研究日渐增多,例如色氨酸的代谢,与精神疾病,免疫疾病,以及癌细胞的免疫逃逸都具有重要关联。此外,色氨酸,甘氨酸,精氨酸,丝氨酸的代谢与肿瘤发生发展具有重要关系,已成为重要的精准药物靶点。目前对于氨基酸的检测主要有光谱,液相色谱,酶联显色反应等,上述手段都难以对人体体液中的氨基酸实现实时、动态的分析,也正因为缺乏一种对体液中氨基酸的快捷、实时、灵敏准确分析的手段,不但限制了对不同氨基酸与人类健康关系的进一步研究,而且错失了通过对这种重要生理代谢基础物质的监控来早期预警健康状况的机会。
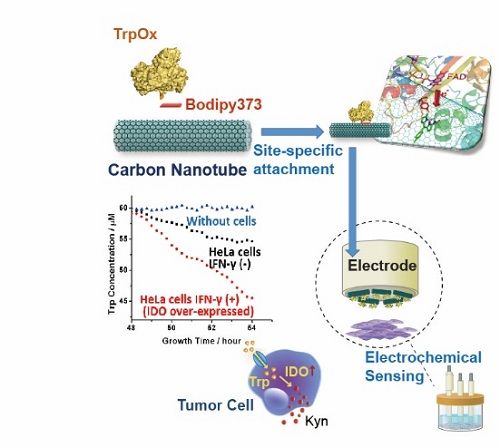
改进酶电化学生物传感器(EEB)的重点之一是改善酶和电极之间的电子传递。在EEB中使用电子介体是一种改善电子传递的常用方法,但使用电子介体通常会导致相对于酶的原始氧化还原电位增加的过量电位,并且氧化还原介质通常是非选择性的,不仅促进了电极和蛋白质之间的电子转移,也促进了各种干扰分子的电子转移。此外,电子介体在活体分析领域的应用也存在诸多限制。利用纳米材料增强酶电极的电子转移为第3代生物传感器的实现做出了巨大贡献,但酶相对于电极表面的随机取向导致电子转移效率的较大变化。该研究通过基于基因密码子扩展的非天然氨基酸插入技术,位点特异性地将巯基苯丙氨酸(TF)插入到酶特定位点中,TF的巯基通过该研究发展的新型生物正交“S-Click”反应与连接分子(Bodipy373)的氯苯基团特异偶联,而连接分子通过π-π stacking组装到碳材料表面,实现不同氨基酸氧化酶在碳材料电极表面的定点偶联(如图2所示)。该团队开创的定点偶联体系(S-Click, 图2C),相比于目前主流的基于叠氮基-炔烃基“点击化学”的偶联体系,具有更好的反应活性与生物相容性,更符合开发可穿戴设备的需求。基于该技术制备的色氨酸氧化酶电极展现出了更高更均匀的酶负载,同时在电化学测试中也展现出了极低催化电位的色氨酸直接生物电催化(图3)。
利用基于基因密码子扩展的氨基酸生物电化学传感器,团队进一步在血液样品及癌细胞培养体系中对色氨酸、甘氨酸进行了精准的实时原位动态检测(图4)。
生物物理所研究员王江云为论文的通讯作者,副研究员夏霖为论文的第一作者。该工作得到国家自然科学基金、重点研发计划、中科院重点部署项目以及深圳市“三名”工程的资助。(生物谷Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


