Mayo Clinic Proceedings:高盐分摄入或许也会增加机体患2型糖尿病的风险
来自杜兰大学等机构的科学家们通过研究发现,经常在食物中添加盐或许与机体2型糖尿病患病风险增加有关。
2023-11-07
《柳叶刀》子刊:这些食物吃了易得糖尿病!12万余人近12年随访证实,高升糖指数饮食与2型糖尿病风险增加15%有关
在既往研究中,饮食高升糖指数和高血糖负荷与2型糖尿病之间的关联是有争议的,不过这项研究可以说给出了明确的答案。
2024-04-28
AIM:夜猫子要当心糖尿病风险!6万余女性研究发现,晚睡型人相较早睡型人糖尿病风险升高72%,即使排除生活方式影响仍增19%
考虑到睡眠类型不仅部分由遗传决定,而且很多人可能还受到工作要求的限制,因此可能很难改变,夜猫子姐妹们还是得多关注饮食和运动,才好身体倍儿棒呀!
2023-10-08
Nat Med:科学家识别出或能解释2型糖尿病风险差异的特殊基因簇和生物学通路
这些多祖先的2型糖尿病基因簇或许包含了更广泛生物学机制,并能为解释2型糖尿病风险描述的祖先相关差异提供初步的见解。
2024-03-14
Nature:科学家发现或能帮助确定人类2型糖尿病风险和疾病并发症的特殊遗传标记物
将多祖先全基因组关联性研究数据与单细胞表观基因组学研究相结合或能帮助揭示驱动人类2型糖尿病发生和进展的病原学异质性,这或许有望为优化全球获得遗传知情糖尿病的护理提供一条新途径。
2024-02-23
柳叶刀子刊:母亲吸烟与降低后代1型糖尿病风险相关,成年后影响消失
近日,瑞典卡罗林斯卡学院的研究人员在《柳叶刀》子刊" The Lancet Regional Health-Europe "上发表了一篇题为" Prenatal and adult exposure
2023-11-20
2型糖尿病用了基础胰岛素血糖还是高怎么办?最新指南推荐和临床实践经验告诉你!
胰岛素是治疗2型糖尿病(T2DM)的一种重要手段,尤其当采用饮食、运动及口服降糖药物等治疗方式后血糖仍控制不佳时,基础胰岛素常作为首选临床治疗方案。
2023-12-26
科学家全面分析人体膳食纤维摄入与2型糖尿病关系,找到9种相关肠菌并发现降低糖尿病风险的肠菌代谢物
这项研究成果突出了肠道微生物在人类代谢健康和疾病中的重要作用,为精准营养和个性化医疗提供了强有力的科学支撑。
2024-04-18
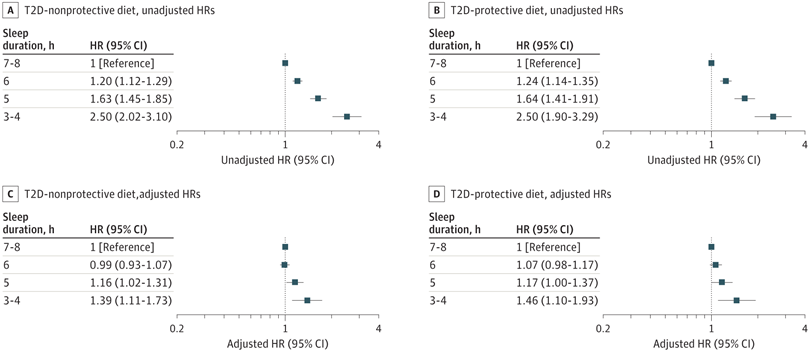
近25万人队列研究显示,每天只睡3-4小时与2型糖尿病风险升高41%有关
一般来说,如果睡不够7小时,我们就会认为睡眠时间过短了。有不少研究发现,急性睡眠不足与葡萄糖耐量受损和胰岛素抵抗有关,可能预示着2型糖尿病的发展。
2024-04-05