Advanced Science:免疫检查点LAG-3竟是tau蛋白种子传播的载体!
这项研究发现,Lag-3可以与tau PFF特异性结合,促进了病理性tau蛋白在神经元之间的传输。而抑制Lag-3则可以阻止这一现象。
2024-03-06
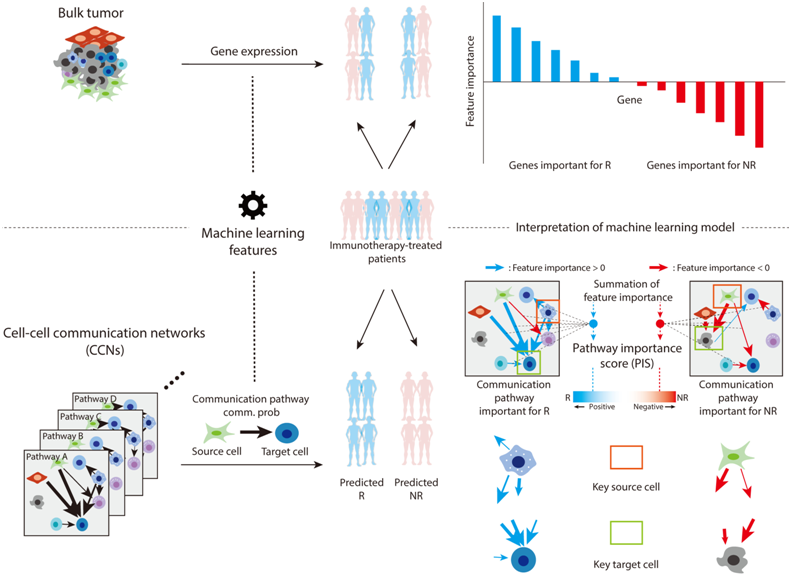
Nat Immunol | 郭安源/甘璐开发提高免疫检查点阻断疗效的药物预测方法
免疫疗法,特别是免疫检查点阻断(ICB),旨在激活和调动免疫系统来根除恶性细胞,并在各种恶性肿瘤中取得了令人印象深刻的临床成功。
2024-03-20
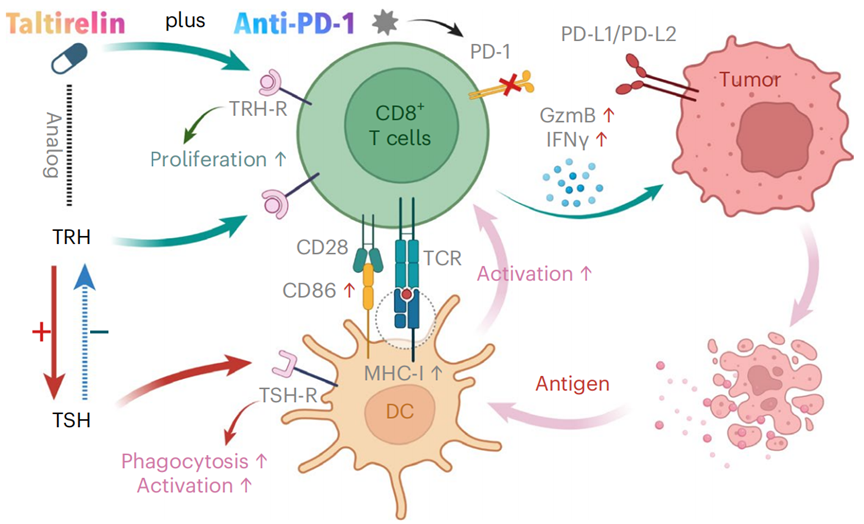
《自然·免疫学》:华西团队发现为免疫检查点抑制剂寻找“黄金搭档”新方法!
这项研究开辟了一种新的途径,通过基因组学预测可以增强ICB疗法效果的药物,克服了基于传统免疫治疗靶点进行预测或筛选的局限性,为癌症治疗提供了新的希望。
2024-04-06
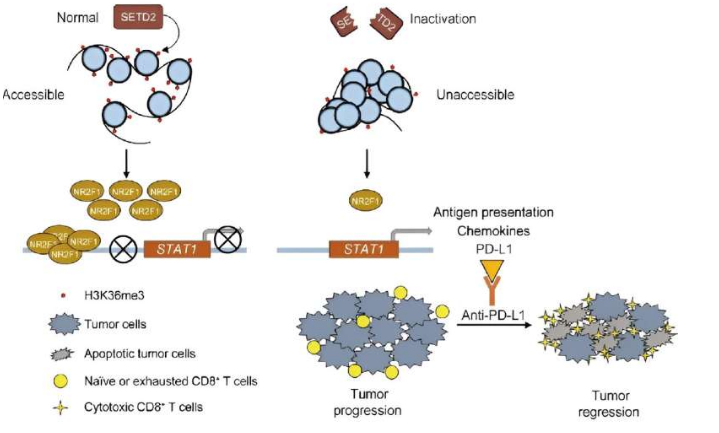
JITC:在人类致死性癌症中识别出免疫检查点抑制剂的新型生物标志物
来自中国科学院上海营养与健康研究所等机构的科学家们通过研究在人类癌症中识别出了一种新型的免疫检查点抑制剂(ICIs)生物标志物。
2023-12-22
Mol Ther:科学家识别出一种新型机制有望增强检查点阻断癌症免疫疗法的潜力
来自利物浦大学等机构的科学家们通过研究分析了免疫系统如何来帮助改善癌症治疗,随后他们发现了一种潜在的新方法或能帮助并开发更好地癌症疗法。
2024-01-30
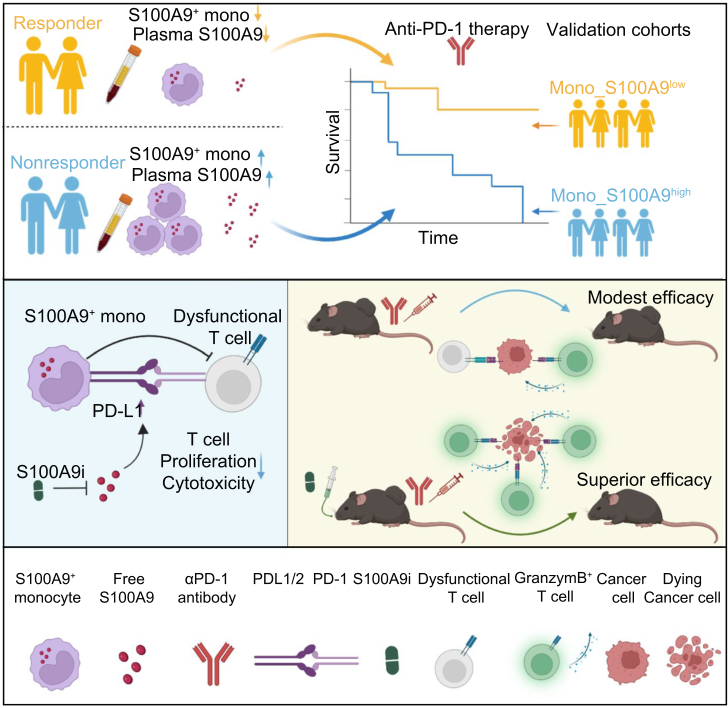
浙江大学研究者们揭示了免疫检查点阻断治疗耐药的单核细胞内在机制
本研究确定了血液中独特的单核细胞特征S100A9+CD14+,作为预测晚期HCC患者对ICB反应不良的有希望的生物标志物。阻断S100A9与抗pd -1药物协同作用,促进HCC根除。
2024-03-28
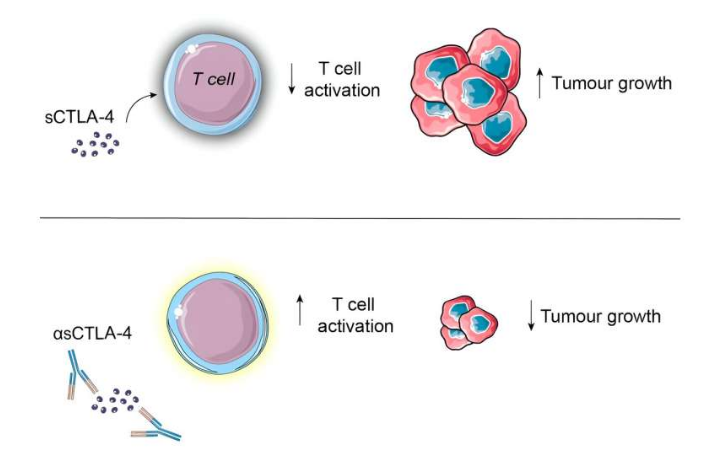
CD:科学家首次证实,BCL-2也是免疫检查点,新的免疫Combo来了!
虽然研究团队把BCL-2抑制剂增强DCs功能,进而改善抗肿瘤免疫应答的作用归类为“脱靶效应”(off-target effects),但相比各种各样的副作用,这类积极的脱靶效应当然多多益善。
2023-09-01