神经干细胞研究进展(第6期)
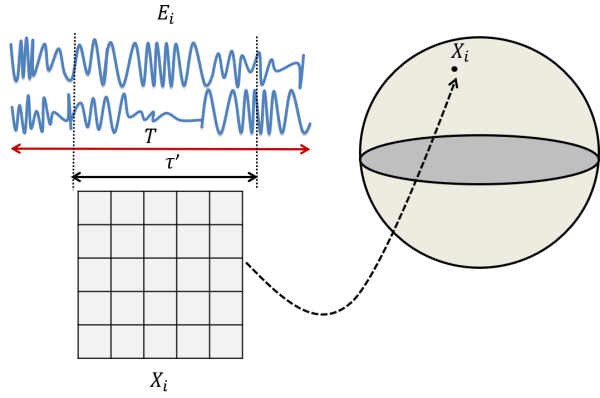
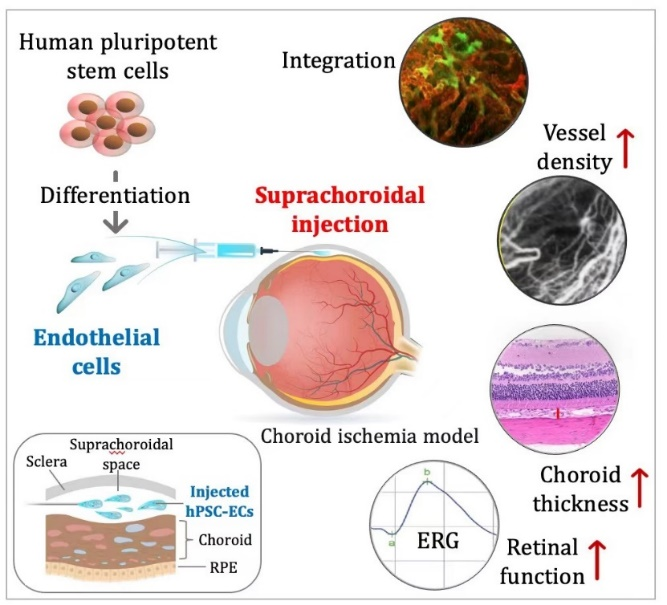
神经干细胞(neural stem cell)是指存在于神经系统中,具有分化为神经神经元、星形胶质细胞和少突胶质细胞的潜能,从而能够产生大量脑细胞组织,并能进行自我更新,并足以提供大量脑组织细胞的细胞
2023-12-31
Science子刊:腺病毒疫苗治疗HPV相关癌症,1期临床结果发布
进一步分析表明,这种有益反应与肿瘤微环境有关,疫苗通过扩增外周HPV特异性T细胞而发挥作用。这些结果表明,有必要对RRP患者进行进一步的PRGN-2012的临床开发,目前正在进行2期临床试验。
2023-12-14
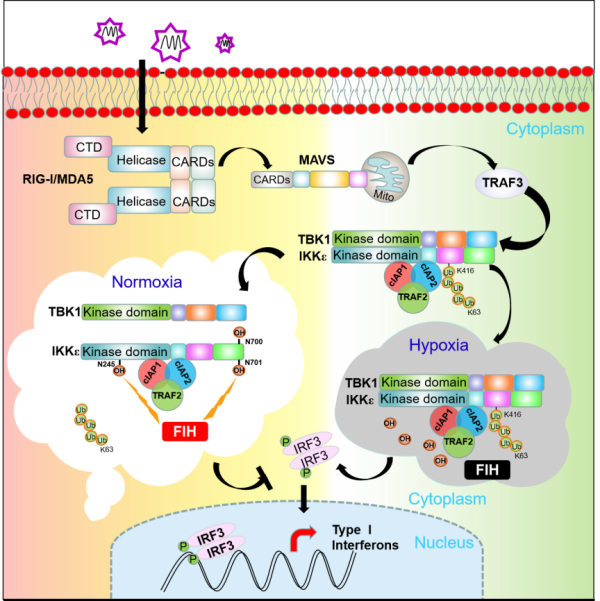
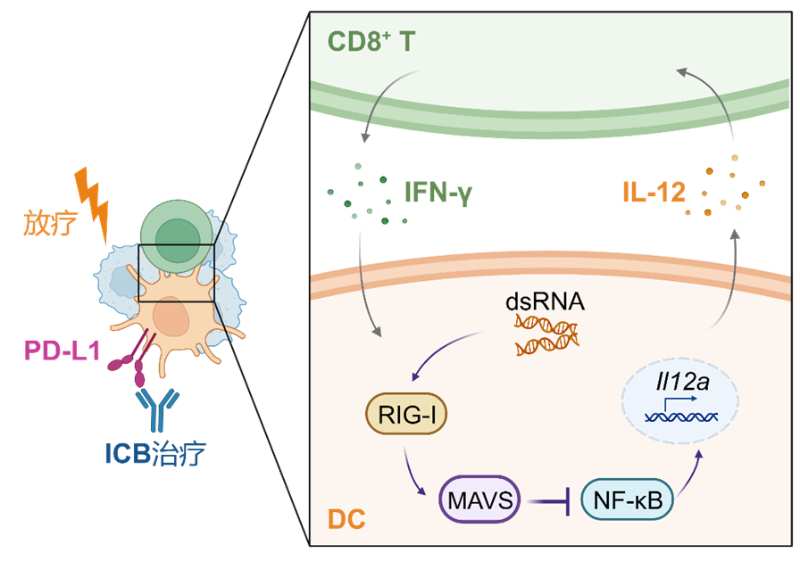
《Science Immunology》发表肿瘤免疫逃逸机制研究新成果
该项研究颠覆了以往对MAVS通路的认识,发现了MAVS通路是肿瘤浸润DC功能障碍的驱动因子,阐明了MAVS通路调控DC抗肿瘤免疫应答的新机制
2023-12-25
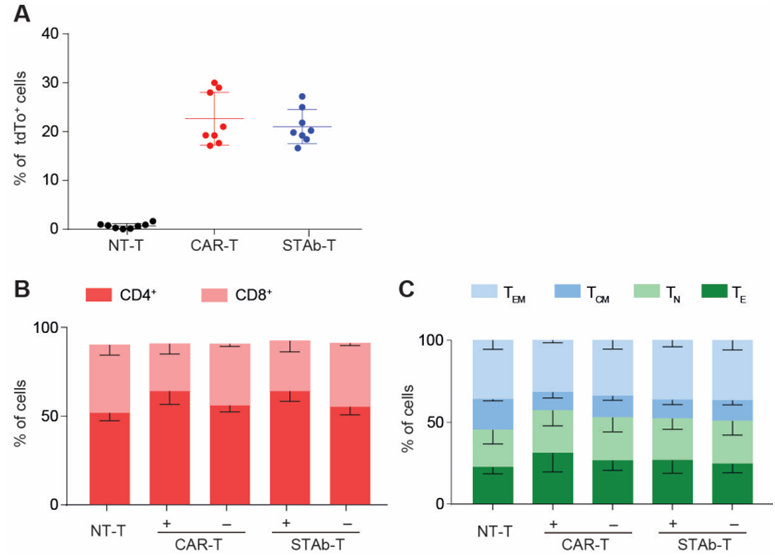
CAR-T细胞疗法研究进展(第41期)
CAR-T (Chimeric Antigen Receptor T-Cell Immunotherapy),即嵌合抗原受体T细胞免疫疗法。该疗法是一种出现了很多年但近几年才被改良使用到临床中的新型细
2024-02-27
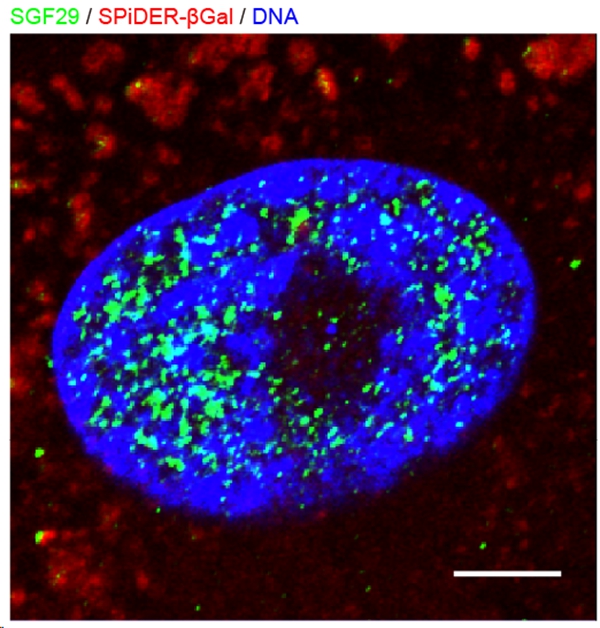
研究揭示相分离调控衰老的机制
细胞区室化是细胞内复杂生化过程有序进行的基础,也是生命演化在细胞水平的重大事件。磷脂双分子层包裹的有膜细胞器是传统认知的细胞区室。与之相对,生物大分子通过分子间多价相互作用发生相分离
2023-11-10