盘点:2020年上半年美国FDA批准的24创新疗法,6款已被中国药企引入大中华区开发!
来源:本站原创 2020-07-01 21:29
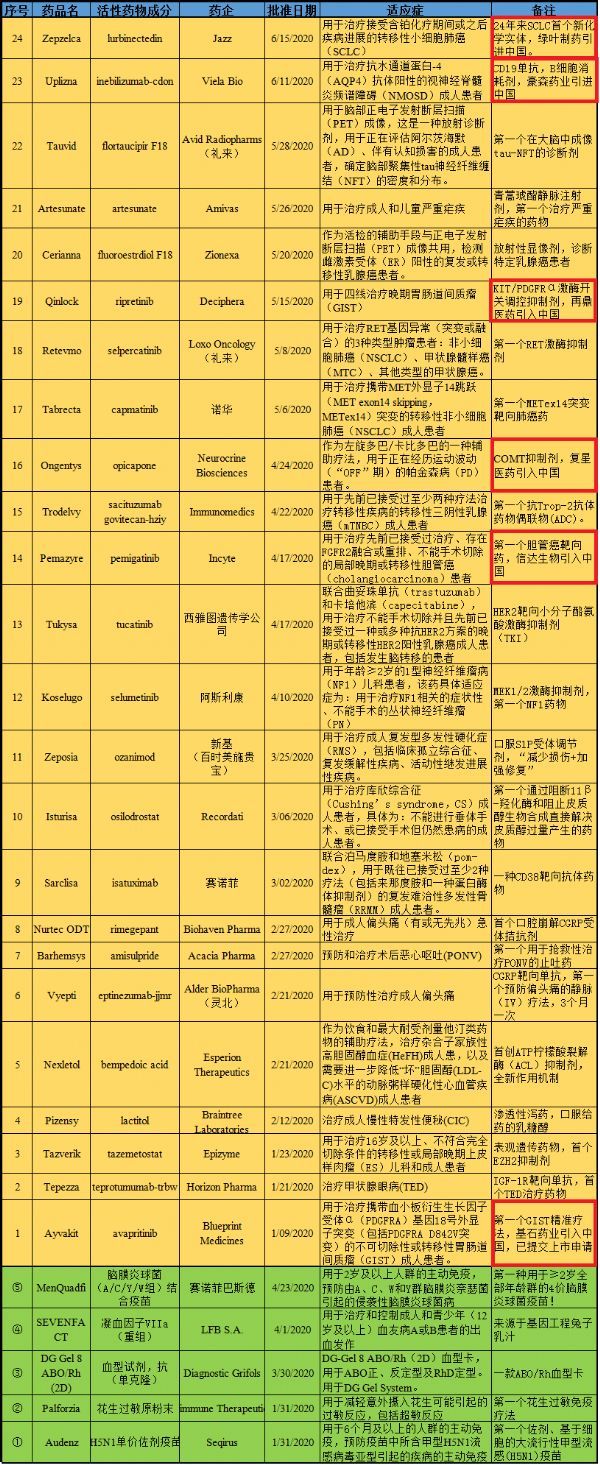
2020年上半年,FDA共批准了24款创新疗法,6个被引入大中华区开发。

2020年07月01日讯 /生物谷BIOON/ --根据美国食品和药物管理局(FDA)药品评审与研究中心(CDER)的数据统计,在2020年上半年,FDA批准了24款创新疗法。而根据FDA生物制剂评审与研究中心(CBER)的数据统计,在2020年上半年,FDA还批准了5款生物制剂,包括:一款食物过敏免疫疗法(Palforzia)、一款流感疫苗(Audenz)、一款ABO/Rh血型卡(DG Gel 8 ABO/Rh (2D))、一款重组凝血因子VIIa(Sevenfact)、一款4价脑膜炎球菌疫苗(MenQuadfi)!
值得注意的是,24款创新疗法中,有多款已被中国药企引入大中华区开发(见图中红框),包括:(1)Zepzelca——24年来小细胞肺癌(SCLC)首个新化学实体,绿叶制药;(2)Uplizna——首个治疗视神经脊髓炎谱系障碍(NMOSD)的B细胞消耗剂,豪森药业;(3)Qinlock——首个四线胃肠道间质瘤(GIST)药物,再鼎医药;(4)Ongentys——治疗帕金森患者OFF期的COMT抑制剂,复星医药;(5)Pemazyre——首个胆管癌靶向药物,信达生物;(6)Ayvakit——首个GIST精准疗法,基石药业,已提交中国上市申请。
每隔一段时间,生物谷医药板块小编会对统计表格进行更新,希望这些创新疗法能够尽快进入中国市场,造福中国的广大患者。(生物谷Bioon.com)
参考:美国FDA新药数据库、生物谷
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->