三阴性乳腺癌(TNBC)重磅消息!TROP-2靶向抗体-药物偶联疗法Trodelvy获美国FDA加速批准!
来源:本站原创 2020-04-23 14:41
Trodelvy是FDA批准的第一个专门治疗复发或难治性mTNBC的ADC药物,也是FDA批准的第一个抗Trop-2 ADC药物。与标准护理相比,Trodelvy代表着一个显著的进步,该药上市后的销售峰值预计将达到10亿美元以上。
2020年04月23日讯 /生物谷BIOON/ --Immunomedics是下一代抗体药物偶联物(ADC)技术的先驱,致力于帮助癌症患者改变生活。其专有的ADC平台的核心是使用一种新型的链接子,这种链接子不需要酶来释放有效荷载,可在肿瘤细胞内和肿瘤微环境中递送活性药物,从而产生近旁效应(bystander effect)。近日,该公司宣布,美国食品和药物管理局(FDA)已批准Trodelvy(sacituzumab govitecan-hziy),用于先前已接受过至少两种疗法治疗转移性疾病的转移性三阴性乳腺癌(mTNBC)成人患者。值得一提的是,Trodelvy是FDA批准的第一个专门治疗复发或难治性mTNBC的ADC药物,也是FDA批准的第一个抗Trop-2 ADC药物。
TNBC是一种预后很差的侵袭性癌症,除了传统化疗之外,治疗方案极其有限。Trodelvy有潜力成为TNBC治疗的一个标准护理药物。在临床试验中,Trodelvy在难治mTNBC患者中显示了临床意义上的缓解,该药将为临床医生提供一个新的工具,为mTNBC患者带来更好的治疗结局。行业分析人士此前表示,根据II期临床数据,与标准护理相比,Trodelvy代表着一个显著的进步,该药上市后的销售峰值预计将达到10亿美元以上。
Trodelvy的活性药物成分为sacituzumab govitecan,这是一种新型、首创的抗体药物偶联物(ADC)药物,由靶向TROP-2抗原的人源化IgG1抗体与化疗药物伊立替康(一种拓扑异构酶I抑制剂)的代谢活性产物SN-38偶联而成。TROP-2是一种在90%以上的TNBC中表达的细胞表面糖蛋白。
之前,FDA授予了Trodelvy突破性药物资格(BTD)和优先审查。根据单臂多中心II期研究中观察到的客观缓解率(ORR)和缓解持续时间(DOR)数据,Trodelvy通过加速审批程序获得批准。该适应症的持续批准,将取决于验证性III期ASCENT研究(入组500例mTNBC患者)中临床益处的验证和描述。就在最近,基于独立数据安全监测委员会(DSMC)的建议,ASCENT研究已提前终止,原因是在多个终点方面取得了令人信服的疗效证据,数据将在今年年中公布。
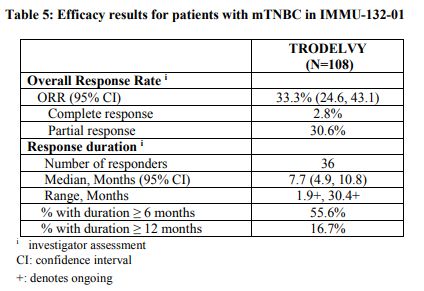
单臂多中心II期研究中共入组了108例过度预治疗的mTNBC成人患者,这些患者先前接受过多种疗法(范围:2-10种)治疗转移性疾病。数据显示,Trodelvy治疗的客观缓解率(ORR)为33.3%(95%CI:24.6,43.1)、中位缓解持续时间(DOR)为7.7个月(95%CI:4.9,10.8)。
Trodelvy药物标签中附有一则黑框警告,提示严重的中性粒细胞减少和严重的腹泻。发生在25%或以上患者中的最常见不良反应,包括恶心、中性粒细胞减少、腹泻、疲劳、贫血、呕吐、脱发、便秘、食欲减退、皮疹和腹痛。发生在超过5%患者中的最常见3级或4级不良事件是中性粒细胞减少、白细胞减少、贫血、低磷血症、腹泻、疲劳、恶心和呕吐。2%的患者因不良事件而停止治疗。没有与治疗相关的死亡病例,也没有神经病变或间质性肺病的严重病例。
乳腺癌是女性中最常见的癌症类型,全球每年确诊超过200万例。三阴乳腺癌(TNBC)约占所有乳腺癌比例的15%,与其他类型乳腺癌相比,TNBC在50岁以下女性中更为常见。TNBC特指雌激素受体(ER)、孕激素受体(PR)及人表皮生长因子受体2(HER-2)三者均为阴性表达的乳腺癌,进展迅速,预后极差,5年生存率不到15%。TNBC对激素疗法和HER2靶向疗法(如罗氏赫赛汀Herceptin)均无效,临床治疗选择非常有限,主要依靠化疗。

Trodelvy是一种新型、首创的抗体药物偶联物(ADC)药物,由靶向TROP-2抗原的人源化IgG1抗体与化疗药物伊立替康(一种拓扑异构酶I抑制剂)的代谢活性产物SN-38偶联而成。TROP-2是一种在90%以上的TNBC中表达的细胞表面糖蛋白。目前,Immunomedics公司正在评估Trodelvy治疗多种类型癌症,包括mTNBC、尿路上皮癌、非小细胞肺癌等。
值得一提的是,TNBC治疗方面,2019年3月罗氏PD-L1肿瘤免疫疗法Tecentriq获美国FDA批准,联合化疗(Abraxane)一线治疗PD-L1阳性局部晚期或转移性三阴性乳腺癌(TNBC)患者。此次批准,使Tecentriq+Abraxane组合成为治疗TNBC的首个癌症免疫治疗方案。(生物谷Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->


