特应性皮炎(AD)新药!利奥制药抗IL-13单抗tralokinumab:挑战赛诺菲Dupixent的生物药!
来源:本站原创 2020-07-11 16:38
tralokinumab从阿斯利康授权获得,在欧盟和美国已进入审查阶段。

2020年07月11日讯 /生物谷BIOON/ --丹麦药企利奥制药(LEO Pharma)近日宣布,美国食品和药物管理局(FDA)已受理tralokinumab的生物制品许可申请(BLA),该药用于治疗中度至重度特应性皮炎(AD)成人患者。FDA已启动对该BLA的正式审查,处方药用户收费法(PDUFA)目标日期为2021年第二季度。今年6月,欧洲药品管理局(EMA)也受理了tralokinumab治疗中度至重度AD成人患者的营销授权申请(MAA),其人用医药产品委员会(CHMP)正在对该MAA进行监管审查。
如果获得批准,tralokinumab将成为第一个挑战赛诺菲/再生元Dupixent(dupilumab)的生物制剂,该药目前是特应性皮炎(AD)治疗领域的领先产品和唯一生物制剂。
特应性皮炎(AD)是一种慢性、炎症性、炎症性皮肤病,以剧烈瘙痒和湿疹为特征。AD是皮肤屏障功能障碍和免疫失调导致慢性炎症的结果。2型细胞因子,包括白细胞介素13(IL-13)在AD病理生理学的关键方面起着中心作用。
tralokinumab是一种全人IgG4单克隆抗体,通过强效、特异性中和白细胞介素13(IL-13)发挥作用。IL-13是一种重要的细胞因子,在驱动特应性皮炎内在炎症方面发挥关键作用。通过以高亲和力特异性结合IL-13,tralokinumab可阻断IL-13与其受体的相互作用以及随后的下游IL-13信号传导。
tralokinumab是利奥制药从阿斯利康授权获得。2016年7月,双方达成了一项价值10亿美元的协议,阿斯利康将2款皮肤病资产(tralokinumab和brodalumab)授权给利奥制药。此次资产剥离,阿斯利康目的是将业务范围进一步聚焦于三大核心领域——肿瘤、呼吸、心血管&肾脏及代谢。此次授权获得的2款抗体药物中,brodalumab已于2017年7月获得欧盟批准,用于治疗中度至重度斑块型银屑病成人患者。
近年来,利奥制药在皮肤病学领域持续发力。在2019年,该公司与Elektrofi扩大合作,利用后者的微粒悬浮制剂技术(ElektrojectTM)开发皮肤病学抗体药物的创新给药方法,实现几秒内以相对小体积给药高剂量抗体治疗。此外,该公司还完成收购拜耳的处方皮肤病学业务。
2019年底,利奥制药还与成都先导(HitGen)扩大合作,通过行使选择权,从成都先导授权了一些小分子化合物,这些化合物是成都先导利用其专有的DNA编码文库(DEL)筛选、针对利奥制药提供的一个未公开的皮肤病学靶标。随着项目的推进,成都先导有资格获得相关的临床前和临床里程碑付款和特许权使用费。
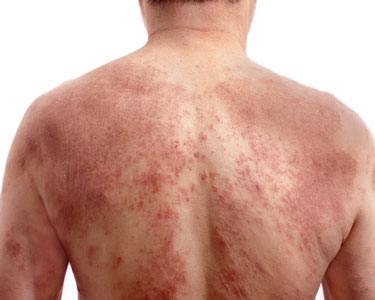
特应性皮炎(图片来源:icresearch.net)
此次tralokinumab BLA提交,基于3项关键性III期研究(ECZTRA 1、2、3)的数据。前2项是随机、双盲、安慰剂对照、多国52周研究,分别入组了802例和794例患者,评估了tralokinumab(300mg,皮下注射)治疗中度至重度AD成人患的疗效和安全性。第3项是双盲、随机、安慰剂对照、多国32周研究,评估了tralokinumab(300mg,皮下注射)联合局部皮质类固醇激素(TCS)治疗中度至重度AD成人患者的疗效和安全性。
结果显示,3项研究均达到了全部的主要终点和次要终点。主要终点包括:治疗第16周调查员全面评估(IGA)为皮损完全清除(IGA评分为0)或皮损几乎完全清除(IGA评分为1)、治疗第16周湿疹面积和严重程度指数(EASI)评分较基线改善≥75%。次要终点包括:从基线检查到第16周,特应性皮炎(SCORAD)、瘙痒数值评定量表(NRS)至少为4分、皮肤科生活质量指数(DLQI)的变化。研究中,tralokinumab和安慰剂的总体不良事件发生率相当。这些结果表明,对于中重度AD成人患者,tralokinumab是一种有效且耐受性良好的长期治疗方案。
利奥制药全球研发执行副总裁Kim Kjøller医学博士表示:“在中度至重度特应性皮炎仍无法控制的患者群体中,存在着一个重要的未满足医疗需求。如果获得批准,tralokinumab将成为第一种专门中和IL-13细胞因子的生物制剂,最重要的是,它为患有这种衰弱疾病的成年人群提供了一种更有针对性的治疗方法。我们将继续与欧美监管机构合作,尽快将这种创新疗法带给患者。”(生物谷Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->


