HER2阳性胃癌ADC药物!阿斯利康/第一三共Enhertu专门西方胃癌试验:总缓解率38%,持久缓解!
来源:本站原创 2021-09-18 01:43
Enhertu是第一个获批治疗HER2阳性胃癌的ADC疗法,与护理相比显著延长患者生存。
2021年09月18日讯 /生物谷BIOON/ --阿斯利康(AstraZeneca)与第一三共制药(Daiichi Sankyo)近日在2021年欧洲医学肿瘤学会(ESMO)虚拟大会上公布了阳性2期DESTINY-Gastric02临床试验(NCT04014075)的详细结果。数据显示,在先前接受过一种曲妥珠单抗方案治疗的HER2阳性转移性和/或不可切除性胃或胃食管连接部(GEJ)腺癌患者中,HER2靶向抗体偶联药物(ADC)Enhertu(fam-trastuzumab deruxtecan)治疗提供了具有临床意义且持久的肿瘤缓解。
虽然HER2靶向疗法在一线转移性胃癌治疗中的益处已得到充分证实,但疾病最终会进展。DESTINY-Gastric02是第一个专门评估Enhertu治疗西方胃癌患者的试验。在初步分析中,经独立中心审查(ICR)评估,Enhertu(6.4 mg/kg)治疗确认的总缓解率(ORR)为38%。接受Enhertu治疗的患者中,观察到3例(3.8%)完全缓解(CR)、27例(34.2%)部分缓解(PR)。中位随访5.7个月后,中位缓解持续时间(DoR)为8.1个月(95%CI:4.1-NE)。中位无进展生存期(PFS)为5.5个月(95%CI:4.2-7.3)。确认的疾病控制率(DCR)为81%(95%CI:70.6-89.0)。
这些结果与之前发表在《新英格兰医学杂志》上的DESTINY-Gastric01 2期临床试验的结果一致。DESTINY-Gastric02试验中,Enhertu的总体安全性与DESTINY-Gastric01试验中的一致。最常见的3级或更高级别的药物相关治疗期不良事件(TEAE)为贫血(7.6%)、中性粒细胞减少症(7.6%)、恶心(3.8%)、疲劳(3.8%)。据独立审查委员会确定,有6例(7.6%)治疗相关间质性肺病(ILD)或肺炎报告。大多数(83%)为低级别(1级或2级),1例为5级(ILD或肺炎相关死亡)。
阿斯利康肿瘤研发执行副总裁Susan Galbraith表示:“来自DESTINY-Gastric02试验的数据再次肯定了Enhertu对进展期胃癌患者潜在益处的临床意义。患者在接受初始治疗后通常会经历疾病进展,然后面临有限的治疗选择,因此今天的结果给患者和治疗医生带来了希望。”
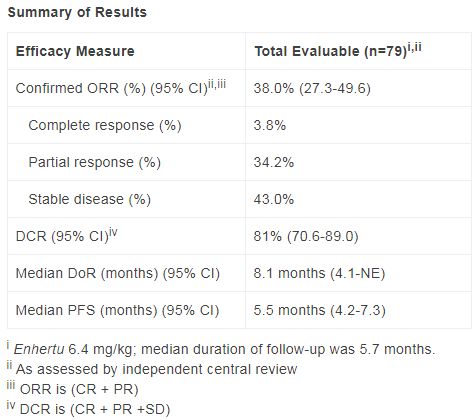
DESTINY-Gastric02临床试验数据
胃癌的预后不佳,尤其是在疾病的晚期时,只有5%-10%的患者存活5年。约五分之一的胃癌被认为是HER2阳性。然而,在接受曲妥珠单抗治疗的胃癌患者中,有29%-69%的患者观察到HER2表达缺失,提示HER2表达降低可导致曲妥珠单抗治疗进展,并可能与不良预后相关。在一线HER2靶向系统治疗后病情进展的患者,二线治疗选择有限,迫切需要新的HER2靶向疗法。
Enhertu是第一个被批准治疗HER2阳性胃癌的ADC药物,该药分别于2020年9月、2021年1月在日本、美国获得批准,用于治疗HER2阳性转移性胃或GEJ腺癌患者。值得一提的是,Enhertu是第一个显示在先前接受过化疗和抗HER2疗法治疗的HER2阳性转移性胃癌患者中与化疗相比显著延长总生存期(中位OS:12.5个月 vs 8.4个月)的HER2靶向疗法。根据临床试验中令人信服的强劲疗效,Enhertu将成为这类患者临床治疗的新护理标准。
该批准基于开放标签、随机2期DESTINY-Gastric01试验的结果。该试验入组了187例(包括日本149例)HER2阳性晚期胃癌或胃食管交界腺癌(定义为:IHC3+或IHC2+/ISH+)患者,这些患者先前接受过2种或多种方案(包括5-FU、含铂化疗、曲妥珠单抗)但病情进展。研究中,患者以2:1的比例随机分配,接受Enhertu(6.4mg/kg)或研究调查员选择的化疗(紫杉醇或伊立替康单药治疗),每三周一次。
结果显示,研究达到了主要终点和关键次要终点:与化疗组相比,Enhertu治疗组在客观缓解率(ORR)和总生存期(OS)方面取得了统计学意义和临床意义的改善。具体数据为:在175例可评估患者(包括140例日本患者)中,通过独立中央审查(ICR)评估:Enhertu组的ORR为51.3%(95%CI:41.9-60.5%)、化疗组为14.3%(95%CI:6.4-26.2%)。在一项预先指定的中期分析中,Enhertu组与化疗组相比死亡风险降低41%(HR=0.59;95%CI:0.39-0.88;p=0.0097)。Enhertu组的中位OS为12.5个月、化疗组为8.4个月。

胃癌是全世界第五大常见癌症,也是第四大癌症死亡原因。晚期或转移性疾病患者的5年生存率仅为5%-10%。在2020年,全球胃癌新发病例约100万例、死亡76.8万例。东亚的胃癌发病率明显较高,约占所有病例的一半。胃癌通常在晚期确诊,但即使在疾病早期确诊,存活率仍然很低。
大约五分之一的胃癌为HER2阳性。HER2是一种酪氨酸激酶受体促生长蛋白,表达于许多类型的肿瘤细胞表面,包括乳腺癌、胃癌、肺癌和结直肠癌。HER2过表达可能与被称为HER2扩增的特定HER2基因改变相关。
对于HER2阳性的晚期或转移性胃癌,推荐的一线治疗方案是化疗+曲妥珠单抗联合疗法。曲妥珠单抗是一种抗HER2药物,已被证实与化疗联合用药可改善患者生存。然而,在接受曲妥珠单抗治疗后的胃癌患者中,有29%-69%的患者观察到HER2表达缺失,这提示HER2表达降低可导致曲妥珠单抗的治疗进展,并可能与胃癌的不良预后有关。对于转移性胃癌患者,在使用曲妥珠单抗为基础的方案进行初始治疗后如果发生进展,治疗选择是有限的,并且在世界上许多地区没有其他HER2靶向药物可用。
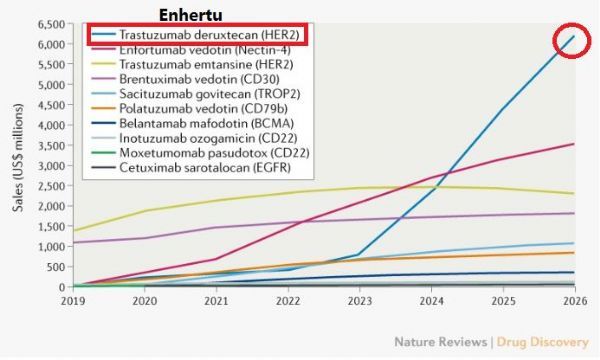
2026年ADC药物销售预测(图片来源于文献PMID 33762691)
Enhertu是一种新一代抗体药物偶联物(ADC),通过一种4肽链接子将靶向HER2的人源化单克隆抗体trastuzumab(曲妥珠单抗)与一种新型拓扑异构酶1抑制剂exatecan衍生物(DX-8951衍生物,DXd)链接在一起,可靶向递送细胞毒制剂至癌细胞内,与通常的化疗相比,可减少细胞毒制剂的全身暴露。
2019年3月,阿斯利康与第一三共达成了一项总价值高达69亿美元的免疫肿瘤学合作,共同开发Enhertu,用于治疗各种HER2表达水平或HER2突变的癌症患者,包括胃癌、结直肠癌、肺癌,以及HER2低表达的乳腺癌。根据协议,双方将在全球范围内共同开发和商业化Enhertu,第一三共保留日本市场的独家权利,同时将全权负责制造和供应。
截至目前,Enhertu已获批2个适应症:(1)用于治疗在转移性疾病中已接受过2种或2种以上抗HER2药物治疗的HER2阳性转移性乳腺癌成人患者;(2)用于治疗局部晚期或转移性HER2阳性胃或胃食管连接部(GEJ)腺癌成人患者。
业界对Enhertu的商业前景非常看好。今年3月,《自然综述·药物发现》(Nature Reviews Drug Discovery)期刊发表文章(The oncology market for antibody-drug conjugates)指出,全球已上市的抗体偶联药物(ADC)的市场规模到2026年预计将超过164亿美元,Enhertu将以62亿美元的销售额位居第一位。(生物谷Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->