2021年终盘点:Science杂志重磅级突破性研究成果
来源:本站原创 2021-01-02 22:39
2021年12月26日讯/生物谷BIOON/---时至岁末,2021年已经接近尾声,迎接我们的将是崭新的2022年,2021年三大国际著名杂志Cell、Nature和Science(CNS)依旧刊登了很多重磅级的研究进展,本文中小编就对2021年Science杂志发表的亮点研究进行整理,分享给大家!
2021年12月26日讯/生物谷BIOON/---时至岁末,2021年已经接近尾声,迎接我们的将是崭新的2022年,2021年三大国际著名杂志Cell、Nature和Science(CNS)依旧刊登了很多重磅级的研究进展,本文中小编就对2021年Science杂志发表的亮点研究进行整理,分享给大家!
1.Science:我国科学家成功构建肿瘤浸润T细胞的泛癌单细胞图谱
doi:10.1126/science.abe6474
靶向肿瘤特异性T细胞的癌症免疫疗法已使许多癌症患者受益,但是针对不同类型的癌症的临床疗效差异很大。肿瘤浸润T细胞经常进入功能失调状态,这一现象被广泛称为T细胞衰竭(T cell exhaustion),而效应T细胞的抗肿瘤功能受多种因素调节,包括调节性T细胞(Treg细胞)的存在。T细胞的状态和丰度在不同癌症类型的肿瘤微环境(TME)中有所不同,这可能从根本上影响不同的临床参数,如对免疫疗法的药物反应。
在一项新的研究中,为了建立一种高分辨率的泛癌T细胞图谱,来自中国北京大学的研究人员对各种癌症类型的患者的肿瘤、癌旁组织和血液样本进行了单细胞RNA测序(scRNA-seq),并收集了其他已发表的scRNA-seq数据集。在校正了混杂因素和批次效应后,对这些不同的数据进行了整合。该图谱由21种癌症类型的316名患者的scRNA-seq数据组成。将T细胞表面上的T细胞受体(TCR)序列与基因表达谱组合起来,以描述T细胞的扩增和动态。应用各种计算方法来研究不同癌症类型的T细胞的特征和丰度。相关研究结果发表在2021年12月17日的Science期刊上,论文标题为“Pan-cancer single-cell landscape of tumor-infiltrating T cells”。
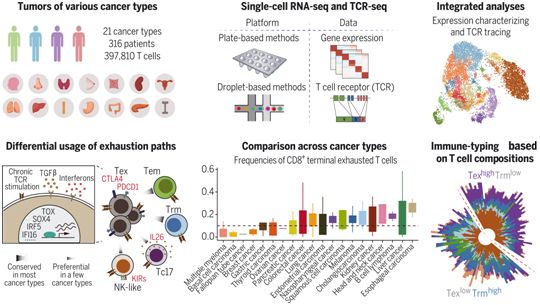
人类泛癌T细胞图谱的系统分析。图片来自Science, 2021, doi:10.1126/science.abe6474。
对于CD4+T细胞而言,TFH/TH1双功能T细胞似乎起源于TFH细胞,也是值得注意的pTRT,并与肿瘤突变负荷相关联。他们还发现,pTRT的转录程序可以受到肿瘤微环境中TGF-β和干扰素的影响。T细胞状态的丰度因癌症类型的不同而有很大的差异。基于肿瘤浸润T细胞的组成,癌症患者可以被免疫分型为一组具有高频率的终末衰竭CD8+T细胞和另一组具有高频率的组织驻留记忆CD8+T细胞,并且免疫类型与临床特征相关,如患者的生存率和对免疫检查点阻断的反应。
2.Science:重大进展!利用纳米孔DNA测序技术成功扫描单个蛋白
doi:10.1126/science.abl4381
在一项新的研究中,利用纳米孔DNA测序技术,来自荷兰代尔夫特理工大学和美国伊利诺伊大学的研究人员成功扫描了单个蛋白。通过在微小的纳米孔中一次一个氨基酸地慢慢移动线性化的蛋白,他们能够读出与该蛋白的信息内容有关的电流。他们将他们的概念验证于2021年11月4日在线发表在Science期刊上,论文标题为“Multiple rereads of single proteins at single–amino acid resolution using nanopores”。这种新的单分子肽读取器标志着蛋白鉴定的突破,并为单分子蛋白测序和对单细胞内的蛋白进行编目开辟了道路。
蛋白是我们细胞的主力军,然而我们根本不知道我们都携带着哪些蛋白。蛋白是由20种不同类型的氨基酸组成的长肽串,相当于一条有不同种类珠子的项链。从DNA蓝图中,我们能够预测蛋白由哪些氨基酸组成。然而,最终的蛋白可能与DNA蓝图大相径庭,例如,由于翻译后的修饰。目前测量蛋白的方法很昂贵,仅限于数量大的蛋白,不能检测许多罕见的蛋白。利用基于纳米孔的技术,人们已经能够扫描和测序单个DNA分子。在这项新的研究中,论文通讯作者、代尔夫特理工大学的Cees Dekker及其团队如今已将这种技术改编为一次一个氨基酸地扫描单个蛋白。
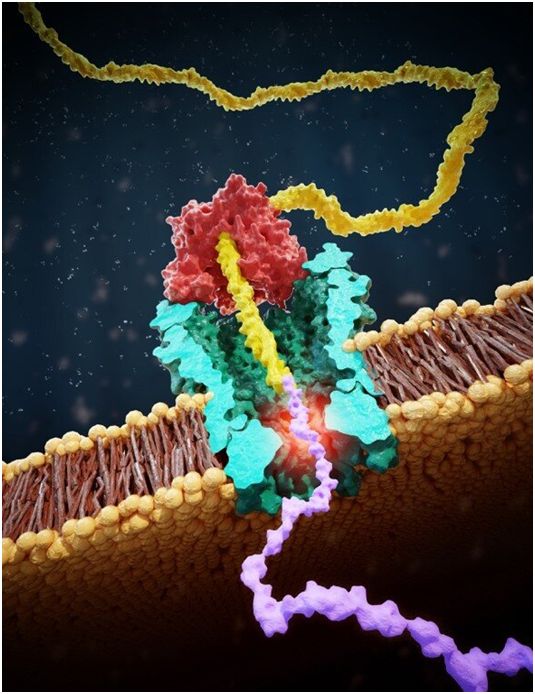
多肽读取器的工作示意图:在解旋酶(红色)拉着附着一个肽分子(紫色)的DNA分子(黄色),让DNA分子缓慢通过纳米孔(绿色),从而允许读出的离子电流信号(橙色突出表示)表征暂时阻塞纳米孔的氨基酸。图片来自Cees Dekker Lab TU Delft / SciXel。
3.Science:重大进展!揭示白内障形成的病理机制,有望开发出新的疗法
doi:10.1126/science.abk0410
随着年龄的增长,衰老在各种退化性疾病的发病中发挥着重要作用,包括白内障的缓慢发展。白内障是一种晶状体混浊,困扰着全世界数百万人的视力。形成眼球晶状体的透明细胞在一生中不断分裂,但在老年人中,这种细胞分裂过程的效率较低,而且衰老的细胞会引发透明度的下降。尽管发病机制在很大程度上还不清楚,但具有早发白内障遗传倾向的患者可以帮助确定分子机制。
缺乏脂质激酶PI3K-C2α会导致鱼类、小鼠和人类的白内障提前发生。这表明PI3K-C2α参与维持一种进化上保守的保护晶状体免受透明度下降影响的机制。在这一发现的基础上,来自意大利都灵大学等研究机构的研究人员在一项新的研究中,从该激酶参与有丝分裂以及正确的细胞分裂可避免衰老和白内障最终产生的概念出发,想要确定PI3K-C2α在晶状体中的作用。相关研究结果发表在2021年12月10日的Science期刊上,论文标题为“PI(3,4)P2-mediated cytokinetic abscission prevents early senescence and cataract formation”。
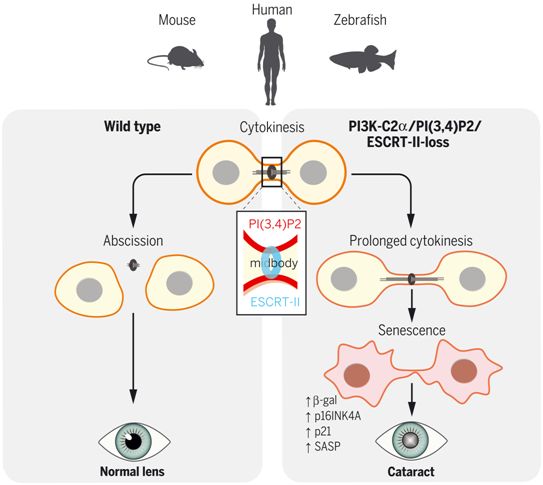
图片来自Science, 2021, doi: 10.1126/science.abk0410。
在中心颗粒体,ESCRT I(endosomal sorting complexes required for transport I)复合物触发了ESCRT II蛋白聚合体的去核,随后触发膜切割ESCRT III装置的去核。作为ESCRT II复合物中的一种关键成分,VPS36锚定在局部预形成的PI(3,4)P2上,从而适当地让ESCRT II蛋白聚合体在中心颗粒体上保持稳定。这是在鱼类、小鼠和人类中发现的,这表明这一过程在整个脊椎动物进化过程中一直是保守的。
如果没有PI3K-C2α及其脂质产物PI(3,4)P2,ESCRT装置就会失去效率,细胞分裂就会延迟。延长的细胞分裂引发了p16INK4A的表达和转录程序的激活,从而导致衰老,这很可能避免了细胞分裂后再融合和四倍体化的基因组不稳定性。然而,细胞分裂演变为一种有弹性的细胞过程,在各种ESCRT复合体的组装中,冗余的途径很常见。例如,ESCRT III组装的另一种绕过了对ESCR II聚合体的需要的途径依赖于连接蛋白ALIX的功能。在晶状体中,ALIX表达不良,特别需要PI3K-C2α、PI(3,4)P2和VPS36途径来保护晶状体细胞免受细胞分裂延迟、衰老以及最终的白内障形成。
4.Science:揭示一些组织在缺氧时利用延胡索酸进行细胞呼吸
doi:10.1126/science.abi7495
人类需要氧气分子来完成一种叫做细胞呼吸(cellular respiration)的过程,这个过程发生在我们细胞的线粒体中。通过一系列被称为电子传递链的反应,电子在某种细胞接力赛中被传递,使细胞能够产生ATP,而ATP为我们的细胞提供能量以完成它们的重要功能。在这个电子传递链的末端,留下两个电子,它们通常被传递给氧气,即“最终电子受体(terminal electron acceptor)”。这就完成了反应,并允许更多的电子进入电子传递链,使这个过程继续进行下去。然而,在过去,科学家们已经注意到,即使在没有氧气的情况下,细胞也能够保持电子传递链的一些功能。美国怀特黑德生物医学研究所博士后研究员Jessica Spinelli说,“这表明线粒体实际上可以有部分功能,即使氧气不是电子受体。我们想了解,这是如何做到的?当氧气不是最终电子受体时,线粒体如何能够维持这些电子输入?”
在一项新的研究中,Spinelli及其研究团队找到了这些问题的答案。他们的研究表明,当细胞缺乏氧气时,另一种叫做延胡索酸(fumarate)的分子可以介入并作为最终电子受体,使线粒体在这种环境中发挥功能。它回答了细胞代谢领域的一个长期之谜,并有可能为研究导致组织内低氧水平的疾病(包括缺血、糖尿病和癌症)提供信息。相关研究结果发表在2021年12月2日的Science期刊上,论文标题为“Fumarate is a terminal electron acceptor in the mammalian electron transport chain”。
5.Science:组织干细胞维持不同的表观遗传记忆机制
doi:10.1126/science.abh2444
组织干细胞对环境线索作出反应并进行整合,从而决定了它们的命运和功能。损伤诱发了干细胞微环境发生根本性变化,从而触发干细胞经历一系列精心设计的事件,包括离开原来的壁龛(niche),迁移到伤口部位,克服炎症,重新产生组织,并在新的部位居住下来。伤口也能诱发可塑性,调动干细胞来修复相关但不同的组织。目前还不清楚干细胞是否在伤口修复中积累和保留这些空间和时间上的经验记忆,如果是的话,这如何发生,后果如何。
在毛囊(HF)内,毛囊干细胞(HFSC)通常只制造毛发,但当伤口损坏覆盖毛囊的皮肤组织时,它们就会被重新利用。在一项新的研究中,来美国洛克菲勒大学的研究人员利用谱系追踪,监测HFSC在伤口修复和干细胞可塑性过程中的时间进展。在离开它们的壁龛和再生缺失的组织后,它们可以长期保持在新的表皮中,并在此后维持皮肤屏障。通过探索转录组和表观基因组的动态变化,并研究这些迁移的HFSC在新的壁龛中的行为,他们了解到这些干细胞积累了关于它们过去经历的离散表观遗传记忆,其中的每一种都以不同的方式影响整体组织功能。相关研究结果发表在2021年11月26日的Science期刊上,论文标题为“Stem cells expand potency and alter tissue fitness by accumulating diverse epigenetic memories”。
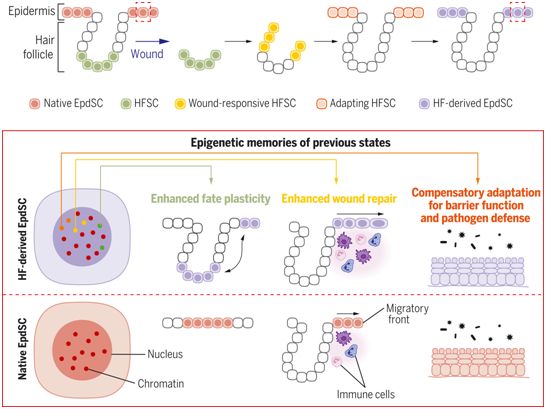
干细胞积累了它们过去经历的表观遗传记忆。图片来自Science, 2021, doi:10.1126/science.abh2444。
6.Science:揭示大脑的岛叶皮层利用身体信号来调节恐惧
doi:10.1126/science.abj8817
恐惧是生存的必要条件,但必须得到很好的调节,以避免有害的行为,如惊恐发作或过度的冒险行为。如今,在一项新的研究中,来自德国马克斯-普朗克神经生物学研究所的研究人员在小鼠身上发现,大脑依靠身体的反馈来调节恐惧。相关研究结果发表在2021年11月19日的Science期刊上,论文标题为“Fear balance is maintained by bodily feedback to the insular cortex in mice”。
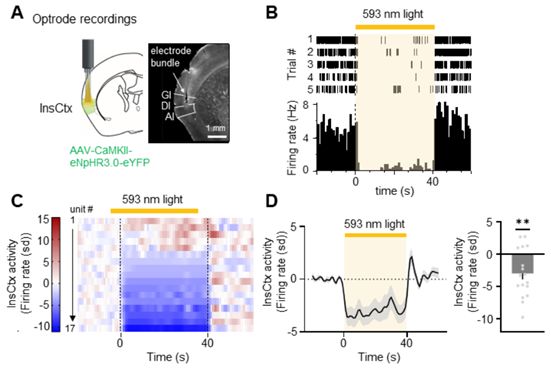
在光遗传学抑制期间InsCtx的体内电生理单单位记录。图片来自Science, 2021, doi:10.1126/science.abj8817。
为了更多地了解这个基本过程,Gogolla团队检查了具有不同恐惧水平的小鼠的岛叶皮层的活动。在恐惧程度较低的小鼠中,一旦它们接触到引起恐惧的音调,岛叶皮层的活动就会增加。相反,高度恐惧的动物在听到这种音调时显示出岛叶皮层活动的减少。令人震惊的是,Klein观察到,一旦小鼠表现出恐惧诱发的僵住行为,它的心率就会下降,岛叶皮层的活动也会下降。高度恐惧的小鼠在听到这种音调时僵住的频率和时间都大大增加,这可以解释观察到的它们的岛叶皮层的失活。
为了测试心率和岛叶皮层活动之间的联系,Gogolla团队通过迷走神经干扰了身体和大脑之间的信息流动。有趣的是,当心脏和大脑之间的交流被中断时,岛叶皮层的活动保持稳定,在僵住期间没有减少。因此,这项新的研究表明,岛叶皮层需要来自身体的反馈,以将恐惧维持在一个适当的水平。此外,它还提供证据表明,僵住期间发生的身体变化是情绪调节的一个重要部分,而且僵住远不止是一种被动的情绪反应。
7.Science:揭示食蟹猴发育过程中的X染色体剂量补偿机制
doi:10.1126/science.abd8887
哺乳动物的性染色体是双态的,即X和Y染色体。雌性有两条X染色体,而雄性有一条X染色体和一条Y染色体。X染色体编码800多个基因;相比之下,Y染色体编码关键的雄性决定因子SRY,但一般来说它编码的基因数量较少。进化出的机制可确保X染色体和常染色体之间以及雌性和雄性之间的基因剂量平衡,即X染色体上调(XCU)和X染色体失活(XCI)。在小鼠中对XCI进行了深入研究,为染色体活动的表观遗传学调控提供了一种模式。长链非编码RNA Xist在激活X染色体上的一连串抑制事件中起着核心作用,包括组蛋白H3赖氨酸27三甲基化(H3K27me3)和组蛋白H2A赖氨酸119单泛素化(H2AK119u1),这些抑制事件在发育早期导致了XCI。然而,最近的研究发现了不同哺乳动物之间在XCI机制方面的关键分歧。在人类中,XIST对于实现XCI是不够的,而且XCI的机制仍然不清楚。
食蟹猴是与人类存在密切亲缘关系的灵长类动物。它们可以作为人类发育的适当模型,并提供有关剂量补偿机制进化的关键信息。在一项新的研究中,来自日本京都大学等研究机构的研究人员对食蟹猴早期发育和生殖细胞发育过程中的X染色体活动进行了全面表征。相关研究结果发表在2021年11月19日的Science期刊上,论文标题为“The X chromosome dosage compensation program during the development of cynomolgus monkeys”。

猴子发育过程中X染色体活动的动态变化。图片来自Science, 2021, doi:10.1126/science.abd8887。
单细胞转录组分析显示,雄性食蟹猴逐渐实现XCU,而雌性食蟹猴则与XCI同时出现XCU,这两者在植入后1周时建立了X染色体:常染色体的剂量补偿。另一方面,雌性生殖细胞在没有抑制的情况下双等位基因地表达X连锁基因,或在它们特化后重新激活,抑制两条染色体上的XIST(E13-E17),然后擦除H3K27me3(E22-E28)。此后,它们获得了完全的双等位基因X连锁基因表达和XIST重新表达(E42)。
8.Science:重大突破!因脊髓损伤而瘫痪的患者新福音!一次注射新型两亲超分子肽纤维支架在4个星期内让瘫痪的小鼠恢复行走能力
doi:10.1126/science.abh3602
在一项新的研究中,来自美国西北大学的研究人员开发出含有两种肽序列的促进神经再生的两亲超分子肽纤维支架(supramolecular peptide fibril scaffold)。单次注射这种支架可逆转脊髓损伤后的瘫痪和修复脊髓组织。他们对瘫痪小鼠的脊髓周围组织进行了一次
注射。仅仅四个星期后,这些小鼠就恢复了行走能力。相关研究结果发表在2021年11月12日的Science期刊上,论文标题为“Bioactive scaffolds with enhanced supramolecular motion promote recovery from spinal cord injury”。

脊髓,图片来自me-pedia.org。
在这种疗法发挥它的功能后,这种支架在12周内被生物降解为细胞的营养物,然后完全从体内消失,没有明显的副作用。这是第一项研究表明科学家们首次通过改变化学结构来控制这种支架中的分子的集体运动,从而提高治疗效果。
论文通讯作者、西北大学的Samuel I. Stupp说,“我们的研究旨在找到一种可以防止个人在重大创伤或疾病后瘫痪的疗法。几十年来,这一直是科学家们面临的一个重大挑战,因为我们身体的中枢神经系统,包括大脑和脊髓,在受伤后或退行性疾病发生后没有任何明显 的自我修复能力。我们将直接向美国食品药品管理局(FDA)提出申请,开始批准这种新疗法用于人类患者,因为这些患者目前的治疗选择非常少。”
9.Science:肠道杀菌蛋白SPRR2A在肠道蠕虫感染时保护肠道屏障
doi:10.1126/science.abe6723
先前的研究已表明,编码SPRR2A(small proline-rich protein 2A, 富含脯氨酸的小蛋白2A)的基因在小鼠小肠中在共生细菌定植后高度上调。为了阐明SPRR2A在肠道中的功能,来自美国德克萨斯大学西南医学中心的研究人员在一项新的研究中探究了它的调节、作用机制、对肠道微生物群的影响以及限制致病性细菌感染的能力。当小鼠感染了肠道蠕虫(寄生虫),Sprr2a的表达进一步升高,超过了共生微生物群诱导的水平。肠道蠕虫感染极大地改变了肠道的免疫反应,并导致上皮损伤和肠道细菌对组织的入侵增加。因此,这些作者在这项新的研究中也探讨了SPR2A上调的分子基础及其在肠道蠕虫感染期间的生理作用。相关研究结果发表在2021年11月5日的Science期刊上,论文标题为“Small proline-rich protein 2A is a gut bactericidal protein deployed during helminth infection”。
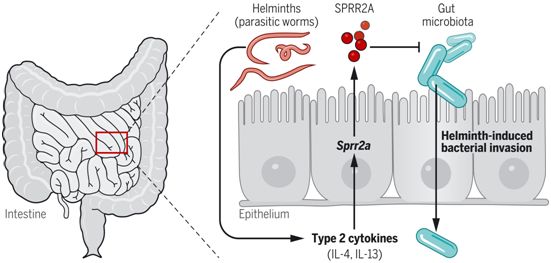
在肠道蠕虫感染时,SPRR2A保护肠道屏障。图片来自Science, 2021, doi:10.1126/science.abe6723。
这些作者进行了体外生化研究以确定SPRR2A的生物活性。纯化的重组SPRR2A在体外选择性地杀死革兰氏阳性菌,而革兰氏阴性菌对SPRR2A的杀伤力有抵抗力。SPRR2A的杀菌机制涉及与带负电荷的脂质结合并破坏细菌的细胞膜。他们培育出缺乏Sprr2a的小鼠,发现总体的细菌载量保持不变。然而,SPRR2A的缺失导致小肠腔和粘液层中革兰氏阳性菌的扩大,这与SPRR2A在体外对革兰氏阳性菌的选择性杀菌活性相一致。Sprr2a缺乏的小鼠还表现出对单核细胞增多性李斯特菌(一种革兰氏阳性肠道病原体)感染的易感性增加。
肠道蠕虫感染可引起肠道上皮的损伤,这促进了细菌对肠道屏障的破坏,并强调了在肠道蠕虫感染期间需要AMP的表达。尽管其他AMP[比如REG3G和溶菌酶]在小鼠感染肠道蠕虫Heligmosomoides polygyrus期间显示出表达减少,但这种感染诱导的SPRR2A表达水平到高于细菌定植引起的水平。肠道蠕虫感染引起了2型细胞因子的产生,如IL-4和IL-13。SPRR2A与其他肠道AMP不同的是,它在肠道蠕虫感染期间被2型细胞因子进一步诱导。因此,肠道蠕虫感染期间Sprr2a的诱导需要STAT6,这是一种转录因子,在IL-4和IL-13的下游发挥作用,诱导2型免疫反应。最后,SPRR2A对于防止肠道细菌(主要是革兰氏阳性菌亚群)在Heligmosomoides polygyrus感染期间侵入肠道屏障是必要的。
10.Science:抑制捣乱的造血干细胞制造抗炎分子,有望从根源上阻止克隆性造血引发的白血病
doi:10.1126/science.aba9304
随着年龄的增长,我们中的许多人获得了突变,导致我们的一些造血干细胞比其他的造血干细胞增殖得更快,形成它们自己独特的群体或“克隆”。这被称为克隆性造血(clonal hematopoiesis)。在某些情况下,源于单个基因改变或突变的造血干细胞的单个克隆,可以扩展到占一个人的血细胞的30%之多。如果这样的“捣乱(rogue)”克隆获得了更多的突变,它可能导致骨髓增生症(一种罕见的血液疾病),并进而导致白血病。
在一项新的研究中,美国波士顿儿童医院干细胞研究项目主任Leonard Zon博士及其团队想知道是否可以将这些捣乱细胞群体扼杀在萌芽状态,防止潜在的致命白血病的发生。如果可以的话,这可能帮助那些随着年龄增长而发生克隆性造血的成年人,以及患有各种血液疾病的儿童,如Shwachman-Diamond综合征、GATA2缺乏症或RUNX1家族性血小板疾病,其中克隆性造血可在儿童时期产生。相关研究结果发表在2021年11月5日的Science期刊上,论文标题为“Resistance to inflammation underlies enhanced fitness in clonal hematopoiesis”。
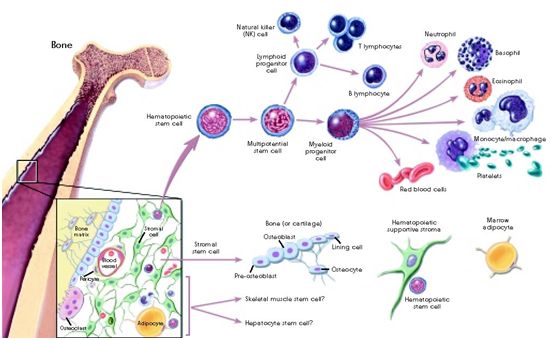
造血干细胞分化,图片来自Wikipedia。
事实上,某些突变,如基因asxl1的突变,确实导致了一个造血干细胞群体---一种单一颜色的细胞---在斑马鱼中占据主导。这些作者随后进一步研究了不同种类的血细胞会因此而开启哪些基因。携带导致克隆性造血的突变的成熟白细胞开启了一系列的炎症基因。相反,突变的造血干细胞则开启了抗炎基因,并制造抗炎分子,保护自己免受炎症影响。当他们敲除这些保护性基因之一---nr4a1---时,这种突变的造血干细胞克隆失去了适应优势,变得不那么占据主导地位。
11.Science:揭示细菌利用可交换的防御基因对抗噬菌体攻击
doi:10.1126/science.abb1083
细菌病毒,即所谓的噬菌体,会破坏细菌。细菌不断暴露在噬菌体的攻击之下。在一项新的研究中,奥地利维也纳大学微生物学家Martin Polz领导的一个研究团队如今研究了细菌如何抵御病毒捕食者,即噬菌体。该研究表明,细菌具有专门为防御噬菌体而设计的可交换
的遗传因子,使细菌群体能够令人惊讶地迅速转换其先天免疫力。细菌如何以及如何快速产生对噬菌体的抵抗力的问题对于开发基于噬菌体的疗法来对付细菌感染具有至关重要的意义。相关研究结果发表在2021年10月22日的Science期刊上,论文标题为“Rapid
evolutionary turnover of mobile genetic elements drives bacterial resistance to phages”。

噬菌体,图片来自Birkbeck/Modeling。
每个细菌不仅拥有与它所属的物种的所有其他细菌共享的核心基因组,而且还包含可移动遗传因子。这种可移动、可交换的基因组在不同的细菌之间可能有所不同,但它的总体功能仍然不为人所知。这项新的研究表明,它主要为一个目的服务:噬菌体防御。相应地,与 噬菌体的斗争塑造了基因组的交换,从而塑造了细菌的进化。
12.Science:肌肉细胞的细胞核迁移也可促进受损肌肉的自我修复
doi:10.1126/science.abe5620
众所周知,肌肉再生是通过一个复杂的过程,涉及几个步骤,并依赖于肌肉干细胞(也称为卫星细胞)。如今,来自西班牙庞培法布拉大学、瓦伦西亚大学和葡萄牙里斯本大学医学院的研究人员描述了生理性损伤后肌肉再生的一种新机制,它不依赖于肌肉干细胞,但依
赖于肌肉细胞的细胞核重新排列。这种保护机制为更广泛地理解生理和疾病中的肌肉修复开辟了道路。相关研究结果发表在2021年10月15日的Science期刊上,论文标题为“Muscle repair after physiological damage relies on nuclear migration for cellular
reconstruction”。
论文共同作者、庞培法布拉大学小组负责人Pura Muñoz-Cánoves说,“在这项研究中,我们发现了一种替代性的肌肉细胞自主的再生机制。”这些作者使用不同的体外损伤模型以及小鼠和人类的运动模型,发现在受伤后,细胞核被吸引到损伤部位,加速了称为肌纤维的
收缩单元(contractile unit)的修复。”
接下来,这些作者分析了他们观察到的这种分子机制:“我们在实验室用肌肉细胞进行的实验表明,细胞核向损伤部位的移动导致了mRNA分子的局部递送。这些mRNA分子在损伤部位被翻译成蛋白,作为用于肌肉修复的构成单元。这一发现代表了肌肉生物学、生理学和肌
肉功能障碍理解上的一个重要进展。”
具体而言,这些作者发现在小鼠和人类中,运动所经历的局部肌肉损伤会激活一种不依赖于肌肉干细胞的肌纤维自我修复机制。小鼠肌肉损伤触发了涉及钙离子、Cdc42和磷酸激酶C的信号级联反应,并通过微管和动力蛋白(dynein)将肌肉细胞的细胞核吸引到受损部位
。这些细胞核的移动加速了肌纤维的修复,并在局部递送mRNA以进行细胞重建。肌纤维自我修复是一种细胞自主的保护机制,代表了理解健康和疾病中肌肉结构恢复的一种替代性模式。
13.Science:揭示细胞毒性T细胞如何重新装上武器,进行一次又一次的杀戮
doi:10.1126/science.abe9977
细胞毒性T细胞(CTL)是免疫系统中的重要细胞,能够识别并摧毁癌细胞和受到病毒感染的细胞。这种杀伤性是由专门的溶细胞蛋白---包括穿孔蛋白和颗粒酶B---的释放所介导的,这些溶细胞蛋白来自储存的分泌颗粒。使CTL成为特别有效的杀手的一个特点是它们能够
进行持续的、连续的杀伤,单个CTL攻击多个目标,一个接一个地攻击。尽管线粒体质量与CTL抗肿瘤活性相关,但CTL表现出对糖酵解的依赖性增加,这表明对线粒体呼吸的依赖性降低。在CTL寻找、识别和杀伤它们的目标时,线粒体是否、如何或为何做出贡献,目前还
不是很清楚。
USP30(ubiquitin carboxyl-terminal hydrolase 30, 泛素羧基末端水解酶30)是一种已知可抑制线粒体自噬的去泛素酶,在对单基因缺失小鼠的大规模筛选中被确定为CTL杀伤性的调节因子。这些结果表明线粒体可能在CTL生物学特性中发挥了一种以前未被重视的作用
。因此,在一项新的研究中,来自英国剑桥大学和邓迪大学的研究人员获得了来自USP30缺陷小鼠的CTL,以研究这种缺陷的性质,并了解它如何影响CTL的杀伤性。相关研究结果发表在2021年10月15日的Science期刊上,论文标题为“Mitochondrial translation is
required for sustained killing by cytotoxic T cells”。
USP30缺陷小鼠的T细胞发育不受影响。然而,一旦遭受激活,CD8+T细胞产生的CTL具有急性线粒体损失和杀伤力受损。USP30缺陷的CTL的细胞毒性随着时间的推移而减弱,表明其持续杀伤力有缺陷。尽管Usp30-/- CTL失去了线粒体并降低了氧化磷酸化,但是它们的迁移
能力、信号传递和分泌---这些都是CTL杀伤性所需的---都是完整的。然而,这些作者发现Usp30-/- CTL的分泌颗粒大小减少,新合成的关键溶细胞蛋白---穿孔蛋白和颗粒酶B---的中间产物也减少。这表明在蛋白从头合成过程中存在内在的缺陷,而这种蛋白从头合成正
是持续杀伤所必需的。
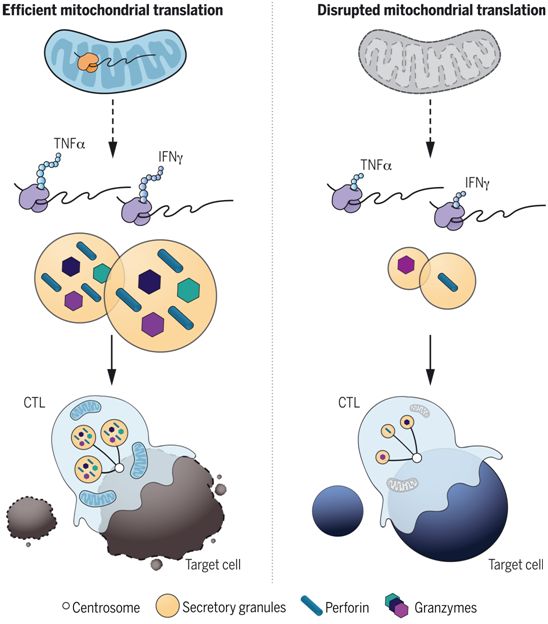
线粒体调节CTL的持续杀伤性,图片来自Science, 2021, doi:10.1126/science.abe9977。
线粒体翻译如何选择性地影响溶细胞蛋白的翻译并调节CTL的杀伤能力?mTOR信号和整合应激反应(integrated stress response)的激活都没有引起Usp30-/-CTL的细胞翻译和杀伤性丧失。然而,在USP30剔除的CTL和经过多西环素处理的CTL中,可以兼作RNA结合蛋白 (RBP)的代谢酶的表达发生了改变。因此,这些研究结果表明RBP的转录后调节--一种在CTL中被充分描述的现象---可能调控USP30缺失后检测到的蛋白合成选择性下调。
14.Science:重大进展!新方法让成年哺乳动物的心肌细胞恢复年轻状态,可使心脏具有再生能力
doi:10.1126/science.abg5159
现有研究表明,成年哺乳动物的心脏不包含心脏干细胞,而且绝大多数心肌细胞不会分裂。因此,在成年哺乳动物的心脏中,心肌细胞的替换非常缓慢,阻止了受损心肌的再生。心肌细胞的有丝分裂后的性质阻止了心脏肿瘤的形成,但同时也将心肌细胞的更新降到最低。相比之下,胎儿心脏显示出相当大的再生潜力,因为存在不太成熟的仍有增殖能力的心肌细胞。
图片来自Pixabay/CC0 Public Domain。
这项新的研究建立在先前研究---表明如果婴儿在子宫内遭遇心脏损伤,心脏可以自我修复,因为心肌细胞处于一种允许恢复青春的状态---的基础上。在出生后或以后的生活中则不是这样,这是因为心肌细胞没有再生能力。经过几年的努力,这些作者发现了一种让成年心肌细胞恢复到类似胎儿的心肌细胞的方法:利用转录因子Oct4、Sox2、Klf4和c-Myc(OSKM)对它们进行重编程。他们的研究表明,表达这些因子可使心肌细胞更新。这种重新编程还包括使用抗生素多西环素(doxycycline)这种开关。
具体而言,他们发现Oct4、Sox2、Klf4和c-Myc(OSKM)的心脏特异性表达能诱导成年的心肌细胞去分化到类似于胎儿心肌细胞的多能性状态,从而赋予成年心肌细胞以再生能力而重新进入有丝分裂。OSKM的瞬时特异性表达延长了产后小鼠心脏的再生窗口期,并诱导成年心肌细胞的基因表达程序,从而使之类似于胎儿心肌细胞。延长OSKM在成年心肌细胞中的表达会导致心肌细胞重编程和心脏肿瘤的形成。在心肌梗塞前和心肌梗塞期间短期表达OSKM可以改善心肌损伤并提高心脏功能,这表明时间上控制的心肌细胞去分化和重编程可以使成年哺乳动物的心肌细胞重新进入有丝分裂,促进心脏再生。
15.Science:颠覆常规!人体代谢率在生命早期就达到顶峰,在60岁后才开始下降
doi:10.1126/science.abe5017; doi:10.1126/science.abl4537
我们大多数人都记得,有一段时间,我们可以想吃什么就吃什么,却不会发胖。但是,在一项新的研究中,来自美国、中国、日本、英国、挪威、摩洛哥、加纳、荷兰、法国、瑞士、挪威、德国、毛里求斯、牙买加、南非、肯尼亚、卢旺达、芬兰、丹麦和奥地利的研究人员发现人体的代谢---燃烧卡路里的速度---实际上在生命早期就达到了顶峰,而开始其不可避免的下降的时间比人们想象的要晚。相关研究结果发表在2021年8月13日的Science期刊上,论文标题为“Daily energy expenditure through the human life course”。
这些作者分析了从一周岁到95岁的6600多人在全世界29个国家进行日常生活时消耗的平均卡路里。为了得出每日总能量消耗的数字,他们依靠“双标水(doubly labeled water)”方法。这是一种尿液测试,涉及让一个人喝水,水分子中的氢和氧已经被替换成自然产生的“重元素”形式,然后测量它们被冲出的速度。
这些作者发现,每磅体重中,婴儿的代谢率是最高的。在出生后的头12个月里,能量需求会急剧上升,到一岁时,按体型来说,一岁的孩子燃烧卡路里的速度比成年人快50%。这不仅仅是因为在出生后的第一年,婴儿正忙于将他们的出生体重增加到三倍。这些数据显示,在婴儿期最初的激增之后,代谢每年减缓约3%,直到我们到达20多岁,这时代谢稳定下来,达到一个新的正常水平。尽管青少年时期是成长的高峰期,但是这些作者在考虑到体型因素后,并没有看到青少年时期的每日热量需求有任何增加。
事实上,这些作者发现,在中年时期--人的20岁、30岁、40岁和50岁--的能量消耗是最稳定的。即使在怀孕期间,随着婴儿的成长,随着体重的增加,女性的卡路里需求也不会比预期的多或少。
这些数据表明,人体的代谢直到60岁以后才真正开始下降。这种减缓是渐进的,每年只有0.7%。但是一个90多岁的人每天需要的卡路里比处于中年时期的人少26%。
16.Science:重大进展!揭示哺乳动物干细胞利用抗病毒Dicer抵御多种RNA病毒入侵
doi:10.1126/science.abg2264; doi:10.1126/science.abj5673
在一项新的研究中,来自英国弗朗西斯-克里克研究所的研究人员发现了一种以前认为随着哺乳动物的进化而消失的重要机制有助于保护哺乳动物的干细胞免受SARS-CoV-2和寨卡病毒等RNA病毒的侵害。他们认为,这一发现有朝一日可能在开发新的抗病毒治疗方法中得到利用。相关研究结果发表在2021年7月9日的Science期刊上,论文标题为“An isoform of Dicer protects mammalian stem cells against multiple RNA viruses”。
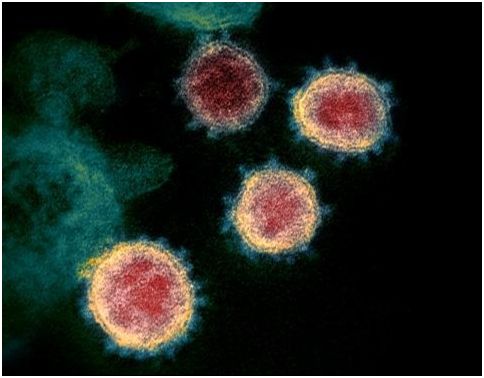
SARS-CoV-2(之前称为2019-nCoV)的透射电镜图,图片来自NIAID RML。
论文通讯作者、弗朗西斯-克里克研究所免疫生物学实验室的Caetano Reis e Sousa说,“了解干细胞如何保护自己免受RNA病毒的侵害是非常吸引人的。事实上,这种保护也是植物和无脊椎动物所使用的,这一事实表明,这种保护可能早在哺乳动物的历史上就存在了,直到进化树分裂的时候。出于某种原因,虽然所有哺乳动物细胞都拥有触发这一过程的先天能力,但似乎只有干细胞才会依赖它。通过进一步了解这一过程,并揭开我们免疫系统的秘密,我们希望为药物开发开辟新的可能性,因为我们努力利用我们身体抵抗感染的天然能力。”
17.Science:重大进展!揭示肠道HDL蛋白保护肝脏免受损伤机制
doi:10.1126/science.abe6729
高密度脂蛋白(HDL)参与维持胆固醇稳态,也可能通过它与众多血浆蛋白的相互作用而具有抗炎或抗微生物的作用。肝脏合成体内的大多数HDL,但肠道也产生HDL。然而,肠道HDL与肝脏产生的HDL发挥的不同作用还没有被确定。HDL颗粒在重塑其货物时,会在组织空间中循环,但到目前为止,HDL在组织内的转运很少被研究。
在一项新的研究中,来自美国华盛顿大学圣路易斯医学院的研究人员推断,了解HDL的转运模式可能会深入了解它在健康和疾病中的作用,包括肠道制造的HDL是否与肝脏制造的HDL在功能上是冗余的。利用他们以前产生的可在任何组织位置上对HDL进行光标记的基因敲入小鼠,他们旨在追踪肠道合成的HDL的命运。相关研究结果发表在2021年7月23日的Science期刊上,论文标题为“Enterically derived high-density lipoprotein restrains liver injury through the portal vein”。
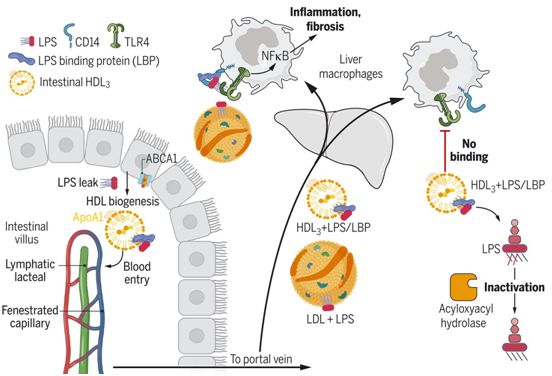
肠道HDL的转运和功能特性,图片来自Science, 2021, doi:10.1126/science.abe6729。
从机制上讲,LPS结合蛋白(LBP)在HDL3颗粒中富集,并且是HDL3掩盖LPS而不被TLR4检测所需的。这一发现是出乎意料的,因为LBP通过将LPS传送到CD14,然后CD14再将LPS传送到TLR4,从而促进TLR4信号传递。因此,HDL3与TLR4信号平台的一个已知组分---LBP---相互作用,以掩盖LPS而不被检测到。如果不与TLR4结合,HDL3-LBP-LPS复合物就不能保留在肝脏中。相反,它离开了肝脏,而与它相结合的LPS被灭活。部分上由肝脏巨噬细胞产生的能使LPS中的关键脂肪酸残基脱酰基以便激活TLR4的酰基羧酸水解酶(acyloxyacyl hydrolase)仍能访问并作用于与HDL3结合的LPS,使之解毒。低密度脂蛋白(LDL)结合LPS,但不结合LBP,因此不能阻止LPS对肝脏巨噬细胞的激活。LBP与磷脂转移蛋白和胆固醇酯转移蛋白同属脂质结合蛋白家族,它们在重塑HDL的脂质结构方面有公认的作用。另一种微生物脂质,即来自革兰氏阳性细菌的脂磷壁酸(lipoteichoic acid),已知可与LBP结合。他们发现,它也与HDL3形成复合物,并抑制肝脏巨噬细胞的激活。
18.Science:重写细菌基因组遗传密码的新方法可一次在蛋白中添加多种非天然的氨基酸
doi:10.1126/science.abg3029; doi:10.1126/science.abi9892
几乎所有的有机体都是通过20种不同的氨基酸组合在一起来构建它们的蛋白质。为了在这种组合过程中添加新的氨基酸,科学家们重新设计了基因和其他的蛋白质构建工具,从而产生了具有独特化学特性的对制造药物很有帮助的蛋白质。但是,这类研究工作很费时费力,而且通常一次只能添加一种新的氨基酸。
如今,研究人员打开了做更多事情的闸门。他们近期报告说,对一种细菌的基因组进行广泛的重写,使他们能够在一种蛋白质中添加许多新的氨基酸。这项研究工作可能为合成抗生素和抗肿瘤药物开辟新途径。相关研究结果发表在Science期刊上,论文标题为“Sense codon reassignment enables viral resistance and encoded polymer synthesis”。
通过重写大肠杆菌基因组,研究人员将几种非天然氨基酸整合到细菌蛋白质中。图片来自Steve Gschmeissner/Science Source。
这种重新利用正是Chin和他的同事们如今所完成的。通过研究大肠杆菌菌株Syn61,他们剔除了编码识别UGC和UCA的转移RNA(tRNA)的基因,并将丝氨酸插入延伸中的蛋白质中。他们还移除了对UAG终止密码子产生反应而关闭蛋白质合成的化学化合物。然后,他们将编码新型tRNA的基因添加回来,它们只要遇到UGC、UCA或UAG就会插入非自然氨基酸。最后,他们将这些密码子添加到基因组中他们希望出现非自然氨基酸的地方。他们报告说,这使他们能够在一种蛋白质中一次性添加三种非自然氨基酸。他们还可以在每种蛋白中添加每种非自然氨基酸的多个拷贝。
19.Science:重大进展!一种新的细胞核分类系统出炉!发现在两种细胞核类型之间来回切换的方法
doi:10.1126/science.abe2218
150年前,俄国科学家Dmitri Mendeleev创造了化学元素周期表,这是一个根据原子核的特性对原子进行分类的系统。如今,在一项新的研究中,一个研究生命之树的生物学家团队公布了一个新的细胞核分类系统,并发现了一种将一种类型的细胞核转化为另一种类型的细胞核的方法。相关研究结果发表在2021年5月28日的Science期刊上,论文标题为“3D genomics across the tree of life reveals condensin II as a determinant of architecture type”。
这项研究是几次单独努力的结果。其中的一个努力聚焦于DNA动物园(DNA Zoo),这是一个由十几个机构组成的国际联盟,包括贝勒医学院、美国国家科学基金会支持的莱斯大学理论生物物理中心(CTBP)、西澳大学和海洋世界(SeaWorld)。DNA动物园团队的科学家们一直在一起工作,对可以有几米长的染色体如何折叠以适应整个生命树上不同物种的细胞核进行分类。无论是观察蠕虫、海胆、海鞘还是珊瑚,他们一直看到相同的折叠模式出现。最终,他们意识到他们看到了两个整体的细胞核结构:在一些物种中,染色体的组装方式就像印刷报纸的页面,外缘在一边,折叠的中间在另一边;在其他物种中,每条染色体都被揉成了一个小球。
他们遇到了难题。这些数据提示着,在进化过程中,物种可以在一种细胞核类型和另一种细胞核类型之间来回切换。他们想知道:这种控制机制是什么?是否有可能在实验室里将一种类型的细胞核变为另一种类型的细胞核?
与此同时,荷兰的一个独立团队(下称荷兰团队)也发现了一些意想不到的东西。该团队当时正在做一种叫做凝缩蛋白II(condensin II)的蛋白质的实验,他们知道它在细胞如何分裂中起作用,但是他们观察到最奇怪的事情:当在人类细胞中让该蛋白发生突变时,染色体会完全重新排列,这真是令人费解。
这两个团队在奥地利山区的一次会议上相遇,并进行相互交流。他们很快意识到,他们找到了一种将人类细胞从一种细胞核类型转换为另一种细胞核类型的方法。
20.Science:阻止成纤维细胞的Engrailed-1基因激活可使皮肤伤口愈合而不留下疤痕
doi:10.1126/science.aba2374; doi:10.1126/science.abi5770
皮肤伤口一般通过形成疤痕来愈合,这是一种由表达Engrailed-1(En1)基因的成纤维细胞谱系介导的纤维化过程。疤痕在三个方面与正常未受伤的皮肤不同:(i) 它们缺乏毛囊、皮脂腺和其他真皮附属物(dermal appendage);(ii) 它们含有密集的、平行的细胞外基质纤维,而不是未受伤皮肤的“篮筐编织(basket-weave)”模式;(iii) 由于这种基质结构的改变,它们缺乏皮肤的正常弹性和强度。一种成功的疤痕疗法将通过促进真皮附属物的重新生长、正常的基质超微结构的重建和机械强度的恢复来解决这三个差异。然而,人们对阻碍出生后皮肤再生性愈合反应的细胞和分子机制知之甚少,也不知道是否可以通过调节特定的成纤维细胞谱系来绕过这些机制。
在一项新的研究中,来自美国斯坦福大学医学院的研究人员想要了解疤痕成纤维细胞(scarring fibroblast, ,也称为瘢痕成纤维细胞)是否纯粹来自于未受伤皮肤中现有的En1阳性成纤维细胞的扩增,或者En1阳性疤痕成纤维细胞是否可以通过激活出生后的En1阴性成纤维细胞在伤口微环境(wound niche)中的En1表达而从新产生。相关研究结果发表在2021年4月23日的Science期刊上,论文标题为“Preventing Engrailed-1 activation in fibroblasts yields wound regeneration without scarring”。

皮肤成纤维细胞中的Engrailed-1激活导致疤痕形成,图片来自Science, 2021, doi:10.1126/science.aba2374。
成纤维细胞移植和谱系追踪研究显示,网状真皮层的En1阴性成纤维细胞(ENF)在伤口微环境中激活En1,产生了大约40%~50%的疤痕成纤维细胞。这一现象取决于机械线索:在软基质上培养的ENF细胞或用机械信号蛋白(比如YAP)的化学抑制剂处理的ENF细胞不会激活En1。通过RNA测序对表达En1的ENF细胞和用短发夹RNA(shRNA)进行En1敲降的ENF细胞进行比较,结果表明En1调节一系列与皮肤纤维化有关的基因。
在愈合的伤口中,通过维替泊芬(verteporfin)抑制YAP,阻断En1激活,可促进ENF细胞介导的修复,在30天内实现皮肤再生,并伴随功能性毛囊和皮脂腺的恢复。对疤痕和再生皮肤的定量比较表明,YAP抑制诱导恢复正常的真皮超微结构,进而使得正常的机械断裂强度得到恢复。白喉毒素介导的出生后表达En1的成纤维细胞的剔除和针对成纤维细胞的转基因YAP敲除同样促进了正常皮肤结构的恢复,这表明对En1激活的调控,无论是直接方式还是间接方式,都能导致伤口再生。(生物谷 Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


