多发性硬化症新药!诺华ofatumumab在美欧进入审查,可在家每月一次皮下注射的B细胞疗法!
来源:本站原创 2020-02-25 10:41
2020年02月25日讯 /生物谷BIOON/ --瑞士制药巨头诺华(Novartis)近日宣布,美国食品和药物管理局(FDA)和欧洲药品管理局(EMA)已分别受理了抗体药物ofatumumab治疗复发型多发性硬化症(RMS)成人患者的生物制品许可申请(BLA)和营销授权申请(MAA)。ofatumumab是一种新型B细胞疗法,具有持久的疗效和良好的安全性。

2020年02月25日讯 /生物谷BIOON/ --瑞士制药巨头诺华(Novartis)近日宣布,美国食品和药物管理局(FDA)和欧洲药品管理局(EMA)已分别受理了抗体药物ofatumumab治疗复发型多发性硬化症(RMS)成人患者的生物制品许可申请(BLA)和营销授权申请(MAA)。ofatumumab是一种新型B细胞疗法,具有持久的疗效和良好的安全性。
如果获得批准,ofatumumab有潜力成为广泛RMS患者群体的首选疗法、并成为第一种可在家轻松给药和管理(采用自动注射笔每月一次皮下注射)的B细胞疗法。ofatumumab在美国预计2020年6月获批,在欧洲预计2020年第二季度获批。诺华致力于将ofatumumab带给全球的患者,在其他国家的监管申请正在进行中。
ofatumumab的监管申请基于2项III期临床研究(0ASCLEPIOS I,II)的积极数据。这2项研究均为头对头(head-to-head,H2H)研究,在复发型多发性硬化症(RMS)患者中开展,评估了每月一次皮下注射20mg剂量ofatumumab与每日一次口服Aubagio(teriflunomide,特立氟胺)14mg片剂的疗效和安全性。Aubagio是赛诺菲的一款口服多发性硬化症药物,也是行业领先的MS口服疾病修正治疗药物。
这2项研究的结果已在2019年9月在瑞典斯德哥尔摩举行的欧洲多发性硬化症治疗与研究委员会(ECTRIMS)第35届会议上公布。
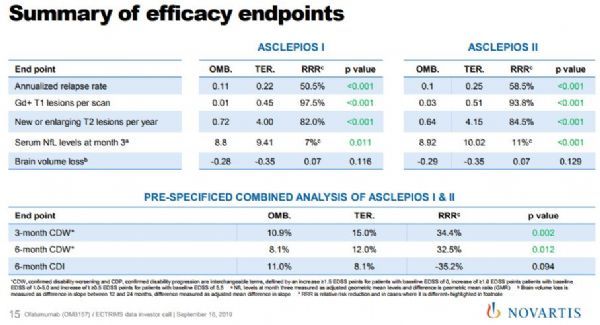
结果显示,2项研究均达到了主要终点,采用年复发率(ARR)评估,与Aubagio相比,ofatumumab使确认复发数量显示出高度显著和临床意义的减少,具体数据为:两项研究中,Aubagio治疗组ARR分别为0.22和0.25,ofatumumab治疗组ARR分别为0.11和0.10,ARR相对降低50.5%和58.8%(2项研究均p<0.001)。与Aubagio相比,ofatumab对钆增强(Gd+)T1病灶和新的或扩大的T2病灶均显示出高度显著的抑制作用,显示出对新的炎症活动的深度抑制。此外,两项研究还达到了延迟确认残疾进展(CDP)时间的关键次要终点,具体数据为:在一项预先指定的汇总分析中,与Aubagio相比,ofatumumab将3个月CDP相对风险降低34.4%(p=0.002)、将6个月CDP相对风险降低32.5%(p=0.012)。总体而言,ofatumumab具有持续的疗效和良好的安全性。2项研究中观察到的ofatumumab安全性与来自II期研究的观察结果一致。
此外,诺华还完成了APLIOS研究,这是一项开放标签II期研究,在RMS患者中开展,旨在确定通过预充式注射器(ASCLEPIOS I、II研究中所使用的)和自动注射笔(用于RMS5患者)皮下注射给药ofatumumab的生物等效性。这项研究的积极成果将在美国佛罗里达州举行的美洲多发性硬化治疗和研究委员会(ACTRIMS)论坛上发表。这些结果表明,ofatumumab可提供一种高效的B细胞疗法,可以在家中使用患者友好的自动注射器笔进行自我给药。
诺华神经科学全球项目负责人Krishnan Ramanathan表示:“我们很高兴ofatumumab有潜力成为寻求有效干预的患者和医生的首选治疗方案。ofatumumab在RMS患者展现了很高的疗效和良好的安全性,该药物有望提供第一个可在家中自行给药的B细胞疗法。我们坚定地致力于为整个MS疾病谱的患者重塑治疗,并与监管部门密切合作,确保尽快为MS患者提供药物。”
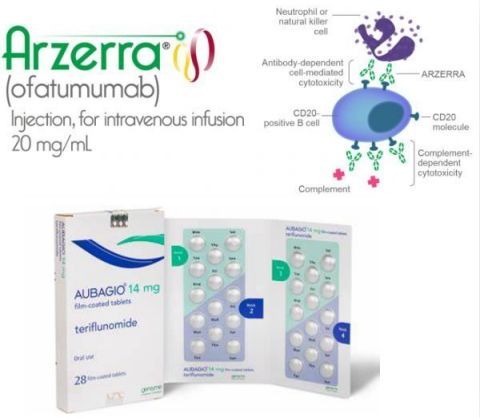
ofatumumab是一种全人抗CD20单抗,通过结合B细胞表面的CD20分子并诱导有效的B细胞溶解和耗尽而发挥作用。,此前,ofatumumab已被批准治疗慢性淋巴细胞白血病(CLL),以品牌名Arzerra销售。但诺华已为ofatumumab指定了一个新的研发代码OMB157,开发作为新一代的B细胞耗竭剂,该药具有更快速的B细胞耗竭作用并保留免疫力的潜在有利安全特性,同时具有每月一次皮下注射进行自我给药的便利性,有望挑战罗氏快速增长的CD20靶向药物Ocrevus(ocrelizumab),后者2019年全球销售额增长57%,达到了惊人的37.08亿瑞士法郎。
ofatumumab(OMB157)治疗多发性硬化症(MS)患者的IIb期阳性结果在2014年公布,显示在给药后的前24周,新的脑损伤数量显著减少。2015年12月,诺华从Genmab获得了ofatumumab所有适应症的权利,包括MS。2016年8月,诺华启动ofatumumab治疗复发型多发性硬化症(RMS)的III期项目。
诺华MS产品组合

多发性硬化症(MS)通过炎症和组织损伤破坏大脑、视神经和脊髓的正常功能,影响全球约230万人。该病通常分为三种类型:复发-缓解型多发性硬化症(RRMS)、继发进展型多发性硬化症(SPMS,通常定义为认知和身体变化以及残疾的整体积累)、原发进展型多发性硬化症(PPMS)。约85%的患者最初出现复发类型的多发性硬化症。
在该领域,诺华的产品组合包括:Gilenya(fingolimod,S1P调节剂)、Mayzent(siponimod,新一代S1P调节剂)、Extavia(皮下注射用干扰素β-1b)。此外,旗下山德士在美国销售Glatopa(醋酸格拉替雷,20mg/mL,40mg/mL),该药是梯瓦重磅MS药物Copaxone的仿制药。(生物谷Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->