降糖药治疗心衰!阿斯利康Farxiga(达格列净)里程碑III期显著降低心衰恶化&心血管死亡风险!
来源:本站原创 2020-03-30 02:46
2020年3月29日讯 /生物谷BIOON/ ---阿斯利康(AstraZeneca)近日公布了降糖药Farxiga(中文商品名:安达唐,通用名:dapagliflozin,达格列净)里程碑III期DAPA-HF研究亚组分析的新数据,结果显示:在射血分数降低的心力衰竭(HFrEF)患者中,无论其背景疗法(即其他治疗心力衰竭的药物)如何,与安慰剂相比,Farx

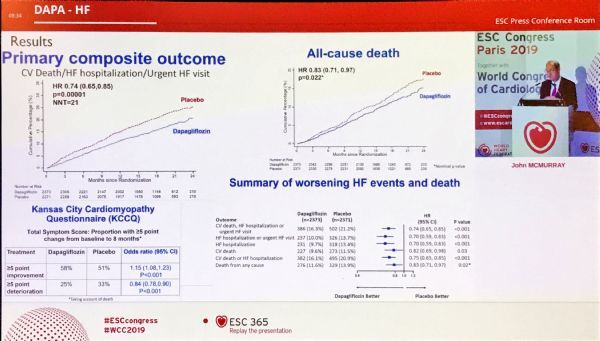
2020年3月29日讯 /生物谷BIOON/ ---阿斯利康(AstraZeneca)近日公布了降糖药Farxiga(中文商品名:安达唐,通用名:dapagliflozin,达格列净)里程碑III期DAPA-HF研究亚组分析的新数据,结果显示:在射血分数降低的心力衰竭(HFrEF)患者中,无论其背景疗法(即其他治疗心力衰竭的药物)如何,与安慰剂相比,Farxig显著降低心力衰竭(HF)恶化或心血管(CV)死亡的主要复合终点的发生率(16.3% vs 21.2%;HR=0.74[95%CI:0.65-0.85],p<0.0001)。
Farxiga在接受广泛的药物治疗、设备治疗、心脏再同步治疗的HFrEF患者中进行了评估,在所有这些治疗亚组中观察到主要结果的一致性降低(主要终点的HR范围:0.57-0.86)。这些结果于近日举行的美国心脏病学会年度科学会议/世界心脏病学大会(ACC.20/WCC Virtual)虚拟会议上公布,并发表于《欧洲心脏杂志》(European Heart Journal)。文章题目为:Effects of dapagliflozin in DAPA-HF according to background heart failure therapy。
阿斯利康生物制药研发部执行副总裁Mene Pangalos表示:“DAPA-HF试验的这些新数据进一步强化了Farxiga在糖尿病之外的临床效果。通过降低心力衰竭恶化的风险,无论背景治疗如何,Farxiga都有潜力改善目前的护理标准,并减轻全球心力衰竭患者的疾病负担。”
Farxiga是一种首创的、每日口服一次的、选择性、钠葡萄糖协同转运蛋白2(SGLT2)抑制剂,该药已批准的适应症为:(1)作为一种单药疗法以及作为组合疗法的一部分,用于2型糖尿病成人患者,改善血糖控制。(2)用于存在2型糖尿病、存在心血管疾病或多个CV风险因素的患者,降低心衰住院风险。
2020年1月,美国FDA受理了Farxiga的一份补充新药申请(sNDA)并正进行优先审查:将Farxiga用于伴或不伴2型糖尿病的HFrEF成人患者,降低CV死亡或HF恶化的风险。FDA已指定该sNDA的处方药用户收费法(PDUFA)目标日期为2020年第二季度。2019年9月,FDA授予了Farxiga快速通道资格(FTD),用于HFrEF或射血分数保留的心力衰竭(HFpEF)成人患者,降低CV死亡或HF恶化的风险。2019年8月,FD还授予了Farxiga另一个FTD,用于伴或不伴2型糖尿病的慢性肾脏病(CKD)患者,延缓肾功能衰竭进展以及预防CV和肾脏死亡。
Farxiga在治疗2型糖尿病方面有很好的应用,FDA对Farxiga治疗HFrEF补充新药申请的优先审查表明,该药也有潜力为心力衰竭患者带来积极影响。心力衰竭影响全球约6400万人,约一半人在确诊后5年内死亡。如果获得批准,Farxiga将成为首个治疗心力衰竭的SGLT2抑制剂。
此次sNDA基于里程碑III期DAPA-HF试验的结果。该研究结果已于2019年9月发表于《新英格兰医学杂志》(NEJM)并在欧洲心脏病学会(ESC)2019年会上公布。结果显示,在射血分数降低的心力衰竭(HFrEF)患者(有或无2型糖尿病)中,当联合标准护理时,与安慰剂相比,Farxiga降低了CV死亡或HF恶化复合结局的发生率。
DAPA-HF是评估一种SGLT2抑制剂联合标准护理药物(包括血管紧张素转化酶[ACE]抑制剂、血管紧张素II受体阻滞剂[ARB]、β-受体阻滞剂、盐皮质激素受体拮抗剂[MRA]和脑啡肽酶抑制剂)治疗HFrEF成人患者(伴有和不伴有2型糖尿病)的首个心力衰竭结局研究。这是一项国际性、多中心、平行组、随机、双盲研究,在射血分数降低(LVEF≤40%)的心衰患者(HFrEF)中开展,包括伴有和不伴有2型糖尿病的患者。研究评估了每日一次10mg剂量Farxiga与安慰剂,联合标准护理治疗的疗效和安全性。研究的主要终点是心衰恶化事件(住院或等效事件,例如紧急心衰就诊)或心血管(CV)死亡的时间。
结果显示,研究达到了主要复合终点:与安慰剂相比,Farxiga将心血管(CV)死亡或心衰恶化复合终点的风险显著减少了26%(p<0.0001),并显示出复合终点的每个单独组分风险都减少了,具体数据为:将发生首次心衰恶化的风险降低了30%(p<0.0001)、将心血管死亡风险降低了18%(p=0.0294)。Farxiga对主要复合终点的影响在所研究的关键亚组中大体一致。此外,结果还显示:堪萨斯城心肌病调查问卷(KCCQ)测量的患者报告结果显著改善,全因死亡率名义上显著降低17%(每100患者年发生一次事件的患者为7.9 vs 9.5),数据有利于Farxiga。该研究中,Farxiga的安全性与该药已确定的安全性一致。容量不足(7.5% vs 6.8%)和肾脏不良事件(6.5% vs 7.2%)的患者比例与安慰剂相当,这是在治疗心力衰竭时通常关注的事件。两个治疗组的重大低血糖事件(0.2% vs 0.2%)都很少见。

心力衰竭(HF)是一种危及生命的疾病,在该病中,心脏不能向身体泵入足够的血液。心衰影响到全球约6400万人(其中至少一半射血分数降低),这是一种慢性、退行性疾病,其中一半的病人将在确诊5年内死亡。心衰仍然与男性(前列腺癌和膀胱癌)和女性(乳腺癌)中最常见的癌症一样致命。心衰是65岁以上患者住院治疗的主要原因,代表了一个重大的临床和经济负担。
Farxiga的活性药物成分为dapagliflozin(达格列净),该药是一种首创的、每日口服一次的、选择性钠-葡萄糖协同转运蛋白(SGLT2)抑制剂,已被批准用于2型糖尿病成人患者改善血糖控制。该药独立于胰岛素发挥作用,在肾脏中选择性抑制SGLT2,可帮助患者从尿液中排出多余的葡萄糖。除了降糖之外,该药还具有减肥和降低血压的额外益处。
阿斯利康正在推进dapagliflozin一个庞大的临床开发项目,涉及超过35个已完成或正在进行的IIb/III期临床研究,入组患者超过3.5万例,并有超过250万患者年的临床使用经验。
值得一提的是,2019年3月,Forxiga(dapagliflozin的欧洲商品名)获欧盟和日本批准新适应症:作为胰岛素的口服辅助治疗药物,用于1型糖尿病(T1D)成人患者的治疗。该药是欧洲批准治疗T1D的首个SGLT2抑制剂,也是阿斯利康获得监管批准的首个T1D药物。该药具体适应症为:作为胰岛素的口服辅助治疗药物,用于接受胰岛素治疗但血糖水平控制不佳并且身体质量指数(BMI)≥27kg/m2(超重或肥胖)1型糖尿病(T1D)成人患者,改善其血糖控制。但在美国方面,该药治疗T1D因糖尿病酮症酸中毒(DKA)风险于2019年7月被FDA拒绝批准。
在中国,dapagliflozin(中文品牌名:安达唐)于2017年3月获批,作为一种单药疗法,用于2型糖尿病成人患者改善其血糖控制。此次批准,使dapagliflozin成为中国市场批准的首个SGLT2抑制剂。该药是一种口服片剂,每片含有5mg或10mg达格列净,推荐起始剂量为每次5mg,每日早上服用1次。(生物谷Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->