首创抗癌药!德琪医药向国家药监局提交Xpovio治疗子宫内膜癌全球3期临床试验申请!
来源:本站原创 2021-01-08 00:37
Xpovio是唯一批准的核输出抑制剂(SINE)。

2021年01月07日讯 /生物谷BIOON/ --德琪医药(Antengene)近日宣布,已向国家药品监督管理局(NMPA)提交Xpovio(selinexor, ATG-010)治疗子宫内膜癌的临床试验申请(IND)。该试验是一项全球性、多中心、随机、双盲3期临床试验(SIENDO),在晚期或复发性子宫内膜癌患者中开展,评估ATG-010与安慰剂在联合化疗后作为维持治疗的疗效及安全性。目前,该试验正在北美、欧洲以及亚洲的80多个研究中心开展。
子宫内膜癌是女性生殖道最常见的癌症之一,而对于初步化疗后仍出现疾病进展的晚期患者,治疗选择有限且预后较差。子宫内膜癌在发达国家及中国部分经济发达地区的发病率居妇科癌首位。近年来,随着肥胖、糖尿病、高血压的人数增多,子宫内膜癌的发病率及死亡率逐年上升并呈现年轻化的趋势。
Xpovio是同类首款且唯一一款口服型选择性核输出抑制剂(SINE),由Karyopharm Therapeutics开发。德琪医药与Karyopharm达成独家合作和授权,获得了Xpovio在多个亚太市场(包括大中华区、韩国、澳大利亚、新西兰和东盟国家)的独家开发和商业化权益。
Xpovio已被美国食品和药物管理局(FDA)批准用于治疗血液瘤领域的2大适应症——多发性骨髓瘤(MM)和弥漫性大B细胞淋巴瘤(DLBCL)。此外,Xpovio用于治疗子宫内膜癌患者的3期SIENDO试验已完成计划的中期分析,数据安全监查委员会(DSMB)推荐SIENDO试验按计划继续进行。
Xpovio的活性药物成分为selinexor,这是一种首创、口服、选择性核输出抑制剂(SINE)化合物,通过结合并抑制核输出蛋白XPO1(又名CRM1)发挥作用,导致肿瘤抑制蛋白在细胞核内积累,这将重新启动并放大它们的肿瘤抑制功能,导致癌细胞选择性凋亡,同时不会对正常细胞造成显著影响。
2019年7月,美国食品药品监督管理局(FDA)批准Xpovio联合低剂量地塞米松用于治疗复发难治性多发性骨髓瘤(rrMM)患者。2020年6月,美国FDA再次批准Xpovio作为单药口服疗法用于治疗复发难治性弥漫性大B细胞淋巴瘤(rrDLBCL)患者。2020年12月,美国FDA批准了Xpovio扩展适应症的补充新药申请(sNDA),用于治疗既往接受过至少一线治疗的多发性骨髓瘤(MM)患者。
值得一提的是,Xpovio是首个也是唯一一个获批的核输出抑制剂(SINE),该药也是自2015年以来首次针对骨髓瘤新靶点(XPO1)的批准药物。此外,Xpovio也是目前被批准用于治疗DLBCL的唯一一种单药口服疗法。
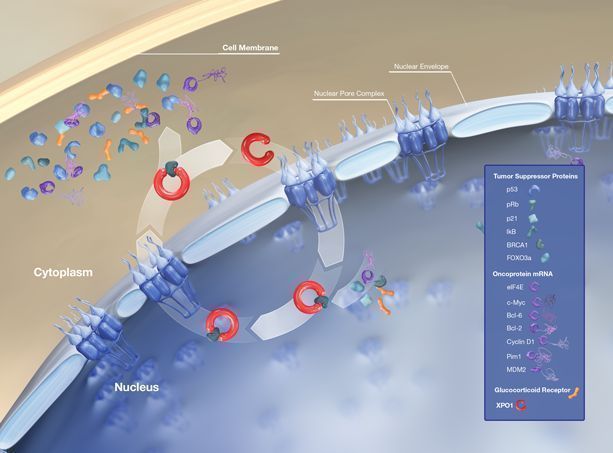
selinexor-XPO1介导核转运
就在最近,德琪医药向韩国食品医药品安全部(MFDS)递交了Xpovio的新药上市申请(NDA):(1)联合低剂量地塞米松用于治疗复发难治性多发性骨髓瘤(rrMM);(2)单药治疗既往接受过至少2线治疗的复发难治性弥漫性大B细胞淋巴瘤(rrDLBCL)。上月初,德琪医药还在多个亚太市场提交了Xpovio上市申请。
当前,德琪医药和Karyopharm正在多个中后期临床研究中评估selinexor治疗一系列血液系统恶性肿瘤和实体瘤的潜力,包括多发性骨髓瘤(MM)、弥漫性大B细胞淋巴瘤(DLBCL)、脂肪肉瘤(SEAL研究)、子宫内膜癌、复发性胶质母细胞瘤。(生物谷Bioon.com)
原文出处:Karyopharm/Antengene files application for ATG-010 in China for endometrial cancer
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->


