梳理肝癌研究进展
来源:本站原创 2019-06-29 17:38
2019年6月29日讯/生物谷BIOON/---肝癌是一类严重的癌症,尽管不少患者在疾病早期就得到了有效的诊断和治疗,但该病的复发率依然很高。尤其是对于病情已进入中晚期的患者而言,预后并不乐观,而且如果癌症扩散到了周边的淋巴结,患者的5年生存率只有11%;当癌症扩散到其他器官后,5年生存率更是只有3%。据美国CDC数据显示,在过去16年间美国肝癌死亡率上升了43%。肝癌发病率升高最多的年龄段为55
2019年6月29日讯/生物谷BIOON/---肝癌是一类严重的癌症,尽管不少患者在疾病早期就得到了有效的诊断和治疗,但该病的复发率依然很高。尤其是对于病情已进入中晚期的患者而言,预后并不乐观,而且如果癌症扩散到了周边的淋巴结,患者的5年生存率只有11%;当癌症扩散到其他器官后,5年生存率更是只有3%。
据美国CDC数据显示,在过去16年间美国肝癌死亡率上升了43%。肝癌发病率升高最多的年龄段为55-64岁,从2000年至2013年间上升了109%,此后保持平稳,诱发美国人群肝癌的风险因素包括HBV或HCV的慢性感染、肝硬化、遗传性肝病及过量饮酒。我国素有“肝癌大国”之称,全球有50%以上的新发和死亡肝癌患者在中国。据世界卫生组织发表的《全球癌症报告2014》显示,中国肝癌的新增病例和死亡人数均居世界首位。2015年我国新发肝癌46.6万例,肝癌死亡例数为42.2万例,是我国因肿瘤导致死亡的第三大致死原因。肝癌起病隐匿,尽管外科手术是肝癌的首选治疗方法,但因患者大多合并基础肝病,或者在确诊时大部分已达中晚期,能获得手术切除机会的患者仅有20%-30%。
我国的人口约占全球人口的1/5,但肝癌的发病率和死亡率都超过了全球一半(接近60%),我国的肝癌和西方不同,欧美肝癌患者发病原因多以丙型肝炎病毒为主,依靠现有的技术手段就可达到很高的治愈率,而中国肝癌患者多以乙型肝炎病毒为主,仍然是医学上的治疗难点。
近年来,科学家们在肝癌研究领域取得了重要的研究进展,在此针对肝癌领域近期取得的进展进行一篇梳理,以飨读者。
1.Cell Stem Cell:迷你器官有助于研究肝癌基因的功能
doi:10.1016/j.stem.2019.04.017
来自Hubrecht研究所和Radboud大学的研究人员开发了一种人体模型,他们使用类器官或小器官来研究肝癌中突变的特定基因的功能。使用这种方法,他们发现BAP1(一种通常在肝癌中发生突变的基因)的突变会改变细胞的行为,这可能使它们更容易被侵入。他们的研究结果发表在5月23日的《Cell Stem Cell》杂志上。

类器官是可以在实验室中生长的微型器官,来自各种器官的非常小的组织。它们已经在癌症研究中使用了几年,主要是通过比较源自健康器官的类器官与源自肿瘤的类器官。然而,该方法不适合于研究已知在癌症中发生突变的特定基因的功能和作用。为了更多地了解肿瘤形成,需要一种新的模型。
研究人员开发了一种新模型,其中使用CRISPR / Cas9对来自健康人肝脏的类器官进行遗传修饰,以研究肿瘤形成中遗传改变的功能。 “研究这种突变在肿瘤形成中的作用在肝癌中尤为重要,”研究人员Benedetta Artegiani说,“因为它是一种非常异质的癌症:不同基因中的各种突变都存在于不同的基因中。”到目前为止,许多这些基因在肿瘤发展中的功能仍然未知。因此,新开发的模型是解决肝癌形成中特定基因功能的有价值工具。
2.eLife:一种机体先天性免疫传感器分子或有望抑制肝癌进展
doi:10.7554/eLife.40396
近日,一项刊登在国际杂志eLife上的研究报告中,来自美国西南医学中心的科学家们通过研究发现,机体先天性免疫系统中对肠道微生物产生反应的一种特殊蛋白或能有效抑制常见肝癌的发生和进展,这种名为NLRP12的先天性免疫感受器或能有效帮助抵御肝细胞癌的发生。
NLRP12是NOD样模式识别受体家族的成员之一,该家族能帮助感知微生物和细胞内其它的刺激物,从而以多种方式来调节机体的先天性免疫反应,本文研究为越来越多的研究增加了证据,即炎症与肝脏肿瘤的发生直接相关。研究者Hasan Zaki教授说道,NLRP12能对肠道微生物产生反应,并在抑制常见肝癌中扮演着关键角色。
研究人员对携带和缺失Nlrp12基因的小鼠机体肿瘤细胞所释放的信号进行研究,他们发现,JNK信号通路(此前被认为与肝癌发生相关)在缺失Nlrp12的小鼠肝脏肿瘤中表现出了高度的活性;JNK通路能被细菌的脂多糖分子所激活,而机体中的有益和有害细菌都会释放脂多糖分子。脂多糖会通过血液从肠道流向肝脏啊中,最终通过激活JNK信号和其它信号通路来引发炎症,这种运输机制在遭受肝炎和脂肪肝的患者肝脏中非常常见。
研究结果表明,NLRP12能够抑制因肠道微生物和促癌信号引发的炎症,为了证实这种肠道-肝脏炎症-致癌假说,研究人员利用抗生素来治疗小鼠降低其肠道菌群的水平,结果发现,利用抗生素治疗剔除肠道菌群能够显著降低缺失Nlrp12的小鼠机体中肿瘤的生长,因此NLRP12或许是一种潜在的治疗靶点,而将当前的免疫检查点阻断剂疗法与增加肝脏中NLRP12的方法相结合或有望改善当前肝癌患者的治疗效果。免疫检查点阻断剂是一种新型疗法,其能通过机体免疫反应来杀灭癌细胞,当该策略开始发挥作用时其会变得非常有效,当通常情况下其并不是非常有效,因此研究人员就需要寻找其它方法来改善这种疗法的作用效果,本文研究中,研究人员就深入阐明了通过NLRP12来调节JNK通路的新型机制,后期或有望帮助开发治疗肝癌的新型疗法。
3.Nature:发现p38γ是肝癌的一个新的治疗靶标
doi:10.1038/s41586-019-1112-8
当前,肝癌几乎没有可用的治疗选择。一种参与细胞应激反应的酶可能成为治疗肝癌的新型药物靶点。在一项新的研究中,西班国立心血管病研究中心(CNIC)的Guadalupe Sabio及其团队发现作为p38激酶的四种类型之一的p38γ蛋白对肝细胞的细胞分裂起始至关重要。这表明“p38γ可能是肝癌的一种有用的治疗靶点”,Sabio说,“我们如今正在开发这种蛋白的抑制剂来测试这种癌症。”相关研究结果于2019年4月10日在线发表在Nature期刊上,论文标题为“p38γ is essential for cell cycle progression and liver tumorigenesis”。

Sabio对p38蛋白家族有着长期的兴趣,这些蛋白在遭受应激的细胞中被激活。如今,在这项新的研究中,她的研究团队证实p38γ在肝脏的细胞分裂起始中发挥着重要的作用。
“p38激酶家族的四个成员是如此相似以至于它们起初似乎具有重叠或冗余的功能”,Sabio说,“但是,由于与西班牙赫罗纳大学的Silvia Osuna和西班牙国家肿瘤研究中心(CNIO)的研究人员的合作,对它们的三维结构的详细分析显示,这四个成员中的p38γ也与另一个称为CDK的蛋白家族有着密切的相似之处。众所周知,这些蛋白是细胞分裂和细胞周期的的调节因子,并且在癌症产生中发挥着重要的作用。”
在研究与CDK的这种相似性的实验室研究中,这些研究人员发现CDK2抑制剂也降低了p38γ的活性。他们还发现p38γ和CDK2均作用于一种在调节细胞周期中起着重要作用的肿瘤抑制蛋白。
4.Cancers:鉴别出与肝细胞癌发生直接相关的关键基因
doi:10.3390/cancers11040486
肝细胞癌(HCC,Hepatocellular carcinoma)是一种常见的肝癌类型,这类癌症的发病率在过去十年中几乎翻了一翻,其成为了美国增长最快的癌症类型,同时也是全球人群因癌症死亡的第三大原因,近日,一项刊登在国际杂志Cancers上的研究报告中,来自美国转译基因组学研究院(TGen)的研究人员通过研究首次提出证据表明,酶AKR1B10或是肝细胞癌的潜在治疗靶点。
研究者Johanna DiStefano说道,如今研究者已经鉴别了基因(编码AKR1B10)和肝细胞癌之间的关联,AKR1B10不仅能作为治疗肝细胞癌的潜在靶点,还能帮助进行致死性疾病的早期诊断。更重要的是,AKR1B10在肝细胞癌的发生和进展过程中扮演着一种看似矛盾的角色,该基因的过量表达能够提示个体是否患有肝细胞癌,而一直该基因的表达似乎能够阻断癌症的进展和扩散。
如今美国每年大约有3.2万名患者死于肝癌,由于AKR1B10能作为肝细胞癌患者诊断和预后评估的潜在生物标志物,有研究表明,AKR1B10酶在肝细胞癌的发生及进展过程中扮演着关键角色;AKR1B10似乎能够影响肝细胞癌患者对当前化疗的耐受性,从而使得这类癌症非常难以治疗。与此同时研究者还发现,编码AKR1B10的基因发生高表达实际上与患者较好的预后、生存率增加及转移性癌症发生之间的关联是相互矛盾的,在肝细胞癌的不同阶段AKR1B10或许发挥着不同的功能。
5.JEM:突破!科学家从分子层面上解释为何男性更易患肝癌?
doi:10.1084/jem.20181288
近日,一项刊登在国际杂志Journal of Experimental Medicine上的研究报告中,来自西班牙国家心血管研究中心的科学家们通过研究发现,脂肪细胞分泌的一种特殊激素在女性机体中水平较高,这或能阻断女性机体肝脏细胞癌变,相关研究结果或能帮助解释为何肝细胞癌在男性群体中更常见,同时也有望帮助开发治疗肝癌的新型疗法。
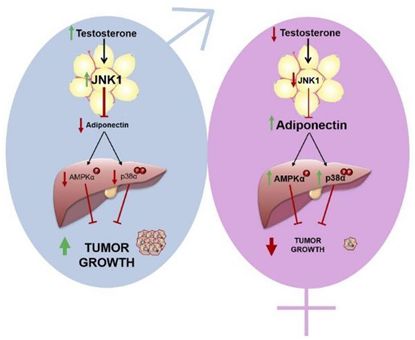
肝癌是全球第四大癌症相关死亡的原因,在美国男性患肝细胞癌的风险是女性的两倍,诱发这种性别差异的因素是一种名为脂联素(adiponectin)的激素,脂联素是脂肪细胞分泌,能够帮助控制机体的代谢,研究者Guadalupe Sabio解释道,相比男性而言,女性机体中循环的脂联素水平相对较高,然而脂联素在肝细胞癌发生过程中所扮演的关键角色目前在科学界仍然存在争议,还需要研究者进一步研究。
与人类相似,雄性小鼠也比雌性小鼠更易患肝细胞癌,这项研究中,研究者发现,雌性小鼠机体中脂联素水平的升高有助于帮助其抵御肝细胞癌的发生。脂联素能激活干细胞中两种特殊蛋白的表达,即p38α和AMPK,从而就能阻断细胞的增殖并抑制肿瘤生长。抑制雄性啮齿动物机体中睾酮的产生就能增加脂联素的水平并降低肿瘤的生长速度。研究者指出,睾酮能激活脂肪细胞中名为JNK1的蛋白的表达,而JNK1能够抑制脂联素的产生。
6.Hepatology:一种新型的组合性免疫疗法有望阻断肝癌的进展
doi:10.1002/hep.30528
近日,一项刊登在国际杂志Hepatology上的研究报告中,来自加利福尼亚大学Moores癌症研究中心的科学家们通过研究发现,将一种合成性的dsRNA聚胞苷酸(dsRNA-polylC)和程序性死亡配体1抗体(PD-L1抗体)相结合或有望有效阻断小鼠模型肝细胞癌的进展,并能促进部分小鼠模型机体中的肿瘤完全缓解以及保持无肿瘤存活状态。
这项研究中,研究者证实了此前在不同肝癌动物模型中的实验结果,他们发现,通过重编程巨噬细胞并激活自然杀伤细胞就能有效抑制肝脏肿瘤的开启,并能消除肿瘤开启细胞;此外研究者认为,通过增强先天性免疫力有望开发出一种肝癌预防性策略,这或将惠及很多肝癌高风险的慢性肝病患者。在分析为何polylC(聚胞苷酸)并不能产生肝癌的治疗效应上,研究者注意到,注射polylC能够潜在诱发肝脏中PD-L1的表达,随后研究人员将polylC与PD-L1抗体联合来检测这种组合性免疫疗法的作用效果。
当polylC与PD-L1抗体结合后,肝脏中活性CD8 T细胞的水平会明显增加,其会抑制肝脏中的肿瘤的进展,研究人员重点对原发性肝癌进行了研究,他们已经分析了这种组合性免疫疗法对转移性肝癌和晚期恶性疾病的影响,目前他们正在寻找最优的疗法剂量,同时还在考虑是否能通过加入额外的制剂来改善疗法的效率。
7.Cancer Prev Res:番茄中的番茄红素可减少脂肪肝、炎症和肝癌
doi:10.1158/1940-6207.CAPR-18-0188
在一项新的研究中,美国塔夫茨大学人类老年化营养研究中心副主任Xiang-Dong Wang及其团队研究了作为一种富含番茄红素的食物的番茄的癌症预防效果。在幼年时,小鼠感染了一种称为二乙基亚硝胺的肝脏致癌物,随后摄入不健康的高脂肪饮食,这种高脂肪饮食类似于西方饮食,含有或不含有含番茄红素的番茄粉。他们随后评估了番茄粉如何好地保护小鼠免受炎症和癌症。对人类来说,这相当于每天吃两到三个番茄或一份番茄酱意大利面。相关研究结果发表在2018年12月的Cancer Prevention Research期刊上,论文标题为“Dietary Tomato Powder Inhibits High-Fat Diet–Promoted Hepatocellular Carcinoma with Alteration of Gut Microbiota in Mice Lacking Carotenoid Cleavage Enzymes”。

这些研究人员首次证实富含番茄红素的番茄粉能够有效地降低这些小鼠摄入的高脂肪饮食促进的脂肪肝、炎症和肝癌产生。给小鼠喂食番茄粉增加了有益菌群的丰富度和多样性,并阻止了一些与炎症有关的细菌的过度生长。
有趣的是,他们观察到番茄粉要比同样剂量的纯化番茄红素补充剂更有效地预防肝癌产生。这可能是由于天然番茄中其他营养成分的潜在有益作用,如维生素E、维生素C、叶酸、矿物质、酚类化合物和膳食纤维。
下一步将是在人体中开展高质量的随机临床试验,以更多地了解番茄中的番茄红素在降低炎症和肝脏疾病风险中的作用。与此同时,这些研究人员认为摄入富含番茄红素的天然食物可能比分离或纯化的番茄红素更有效地预防癌症。
8.Ange Chem Int Ed:科学家开发出新型基于铂的纳米颗粒 有望高效杀灭肝癌细胞
doi:10.1002/anie.201813149
近日,一项刊登在国际杂志Angewandte Chemie International Edition上的研究报告中,来自苏黎世联邦理工学院的科学家们通过研究发现,相比当前药物而言,利用铂纳米颗粒(platinum nanoparticles)有望高效杀死肝癌细胞。
近些年来,靶向性癌症药物的数量持续上升,然而常规的化疗制剂仍然在癌症疗法中扮演着关键角色,其中就包括能攻击并杀灭癌细胞的基于铂的细胞毒性制剂,但这些制剂通常会损伤健康组织并诱发严重的副作用;因此这项研究中,研究人员就鉴别出了一种新方法来帮助筛选更具选择性的癌症疗法。
当铂(II)被氧化时其常常会携带细胞毒性,而通常其以常规基于铂的化疗形式存在,而非氧化状态的铂(0)则对细胞的毒性较小;研究人员通过研究找到乐一种新方法将铂(0)引入到靶向细胞中随后其就会被转化成为铂(II),为了实现该目的,研究人员使用了非氧化的铂纳米颗粒,其首先必须用肽类来稳定;研究者对包含数千种肽类的文库进行筛选鉴别出了一种特殊肽类,其能使铂纳米颗粒维持稳定状态数年时间。
对癌细胞培养物进行检测,结果表明,铂(0)纳米颗粒能够渗入细胞中,一旦进入肝癌细胞的特殊环境后其就会被氧化成为铂(II)纳米颗粒并产生细胞毒性效应。随后研究人员对10种不同的人类细胞进行研究后发现,这种肽包裹的纳米颗粒能够高度选择性地杀灭肝癌细胞,其与药物索拉非尼具有相同的毒性效应,索拉非尼是当前用来治疗原发性肝脏肿瘤的最常用药物,相比索拉非尼而言,新型纳米颗粒的选择性更强,而且比化疗药物顺铂更加有效。
9.Cell Metabol:抗排斥药物雷帕霉素或能有效治疗某些肝癌
doi:10.1016/j.cmet.2019.01.002
近日,一项刊登在国际杂志Cell Metabolism上的研究报告中,来自匹兹堡大学的科学家们通过对动物模型和患者组织进行研究鉴别出了肝脏中的一条新型的分子通路,研究者指出,一种常用的抗排斥药物或能被重新定向来治疗特定类型的肝癌。
研究者Satdarshan Monga说道,我们发现,β-连环蛋白基因发生突变的肝癌或许对雷帕霉素更加易感,而雷帕霉素是一种常用作器官移植过程中的抗排斥药物,这或许就能帮助研究者重新考虑雷帕霉素的新用途,利用其开发治疗肝癌(尤其是耐药性肝癌)的新型疗法。研究者指出,肝脏中中央静脉周围的一系列细胞中常常携带高水平的mTOR蛋白,mTOR蛋白作为对细胞新陈代谢非常重要的营养和能量传感器,其在β-连环蛋白处于活性状态的相同细胞中存在。
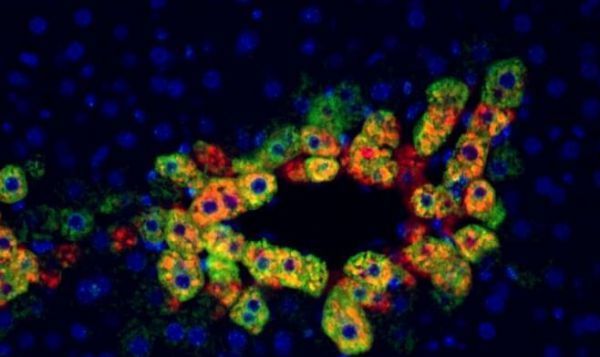
大约25%-30%的肝癌都携带β-连环蛋白基因突变,但研究人员并不是非常清楚这些突变如何以及为何会促进癌变细胞生长,因此当研究人员在β-连环蛋白基因突变的肝癌中发现高水平的活性mTOR时,他们就想知道是否这两种蛋白在功能上具有关联性。为了追踪mTOR激活的来源,研究者们开发了一种肝癌小鼠模型,使得小鼠机体中β-连环蛋白基因及名为Met的基因发生突变,随后研究者发现这些小鼠患肝癌的模式与人类非常相似。
当mTOR激活水平增加时,研究者通过对这些小鼠追踪后发现,β-连环蛋白能通过一种名为谷氨酰胺合成酶(GS)的中间酶类来激活mTOR,这些分子通路与能量摄入有关,作为快速生长的癌细胞,其往往能表现出更高活性的谷氨酰胺合成酶和mTOR。研究者Monga说道,这些肿瘤或许具有mTOR成瘾性,激活mTOR就能刺激细胞中蛋白质制造工厂的进程,从而给予癌细胞足够的能量分裂和生长。
当给遗传修饰的小鼠喂食雷帕霉素时,小鼠机体肿瘤的尺寸会下降,而当加入了另外一种抑制Met的药物时,肿瘤几乎被完全杀灭了,这就说明,mTOR在促进肿瘤生长上扮演着关键角色。研究者表示,此前在对肝癌患者的临床试验中并未发现雷帕霉素的明显有益效应,但本文研究结果表明,如果限定于携带β-连环蛋白突变和mTOR成瘾性肿瘤的患者,那么这种疗法或许会非常有效。
10.Hepatology:科学家发现PI3Kδ在肝细胞癌中发挥重要作用 或可成为新治疗靶点
doi:10.1002/hep.30307
I类PI3K信号途径是人类癌症发育和进展中一个重要的信号途径。在PI3K的四个亚型中,PI3Kα和PI3Kβ是普遍表达的,而PI3Kγ和PI3Kδ主要发现于白细胞中。在实体瘤中靶向PI3K的治疗策略主要是针对PI3Kα和PI3Kβ介导的癌细胞内PI3K活性。PI3Kδ在实体瘤中的作用还不清楚。最近来自韩国的学者们利用RNA测序、芯片和液相色谱-串联质谱等方法对肝细胞癌(HCC)细胞、晚期HCC病人来源的肝癌细胞和小鼠模型等进行了分析以建立PI3Kδ在HCC中发挥的作用。相关研究结果发表在国际学术期刊Hepatology上。
在这项研究中,研究人员首先建立了一个化合物诱导肝癌模型来反映晚期HCC的恶性表型和体内环境,在这个晚期HCC模拟系统中,用双氧水处理HCC细胞,发现双氧水能够特异性增加PI3Kδ的活性而降低I类PI3K其他亚型的活性。利用抑制剂或小干扰RNA介导PI3Kδ基因沉默阻断PI3Kδ活性能够显著抑制HCC细胞增殖并减弱恶性HCC的一些关键特征,包括上调TERT(telomerase reverse transcriptase)的表达。
从机制上来说,双氧水诱导SERPINA3发生氧化修饰,阻止其泛素依赖性降解过程,并增强其作为PI3Kδ和TERT转录激活因子的活性。进一步的研究发现HCC中PI3Kδ的高表达与病人的不良生存率存在关联,而且晚期HCC进展与发生氧化修饰的SERPINA3,PI3Kδ和TERT的蛋白水平存在正相关关系。(生物谷 Bioon.com)
据美国CDC数据显示,在过去16年间美国肝癌死亡率上升了43%。肝癌发病率升高最多的年龄段为55-64岁,从2000年至2013年间上升了109%,此后保持平稳,诱发美国人群肝癌的风险因素包括HBV或HCV的慢性感染、肝硬化、遗传性肝病及过量饮酒。我国素有“肝癌大国”之称,全球有50%以上的新发和死亡肝癌患者在中国。据世界卫生组织发表的《全球癌症报告2014》显示,中国肝癌的新增病例和死亡人数均居世界首位。2015年我国新发肝癌46.6万例,肝癌死亡例数为42.2万例,是我国因肿瘤导致死亡的第三大致死原因。肝癌起病隐匿,尽管外科手术是肝癌的首选治疗方法,但因患者大多合并基础肝病,或者在确诊时大部分已达中晚期,能获得手术切除机会的患者仅有20%-30%。
我国的人口约占全球人口的1/5,但肝癌的发病率和死亡率都超过了全球一半(接近60%),我国的肝癌和西方不同,欧美肝癌患者发病原因多以丙型肝炎病毒为主,依靠现有的技术手段就可达到很高的治愈率,而中国肝癌患者多以乙型肝炎病毒为主,仍然是医学上的治疗难点。
近年来,科学家们在肝癌研究领域取得了重要的研究进展,在此针对肝癌领域近期取得的进展进行一篇梳理,以飨读者。
1.Cell Stem Cell:迷你器官有助于研究肝癌基因的功能
doi:10.1016/j.stem.2019.04.017
来自Hubrecht研究所和Radboud大学的研究人员开发了一种人体模型,他们使用类器官或小器官来研究肝癌中突变的特定基因的功能。使用这种方法,他们发现BAP1(一种通常在肝癌中发生突变的基因)的突变会改变细胞的行为,这可能使它们更容易被侵入。他们的研究结果发表在5月23日的《Cell Stem Cell》杂志上。

图片来自图片来源:www.pixabay.com。
类器官是可以在实验室中生长的微型器官,来自各种器官的非常小的组织。它们已经在癌症研究中使用了几年,主要是通过比较源自健康器官的类器官与源自肿瘤的类器官。然而,该方法不适合于研究已知在癌症中发生突变的特定基因的功能和作用。为了更多地了解肿瘤形成,需要一种新的模型。
研究人员开发了一种新模型,其中使用CRISPR / Cas9对来自健康人肝脏的类器官进行遗传修饰,以研究肿瘤形成中遗传改变的功能。 “研究这种突变在肿瘤形成中的作用在肝癌中尤为重要,”研究人员Benedetta Artegiani说,“因为它是一种非常异质的癌症:不同基因中的各种突变都存在于不同的基因中。”到目前为止,许多这些基因在肿瘤发展中的功能仍然未知。因此,新开发的模型是解决肝癌形成中特定基因功能的有价值工具。
2.eLife:一种机体先天性免疫传感器分子或有望抑制肝癌进展
doi:10.7554/eLife.40396
近日,一项刊登在国际杂志eLife上的研究报告中,来自美国西南医学中心的科学家们通过研究发现,机体先天性免疫系统中对肠道微生物产生反应的一种特殊蛋白或能有效抑制常见肝癌的发生和进展,这种名为NLRP12的先天性免疫感受器或能有效帮助抵御肝细胞癌的发生。
NLRP12是NOD样模式识别受体家族的成员之一,该家族能帮助感知微生物和细胞内其它的刺激物,从而以多种方式来调节机体的先天性免疫反应,本文研究为越来越多的研究增加了证据,即炎症与肝脏肿瘤的发生直接相关。研究者Hasan Zaki教授说道,NLRP12能对肠道微生物产生反应,并在抑制常见肝癌中扮演着关键角色。
研究人员对携带和缺失Nlrp12基因的小鼠机体肿瘤细胞所释放的信号进行研究,他们发现,JNK信号通路(此前被认为与肝癌发生相关)在缺失Nlrp12的小鼠肝脏肿瘤中表现出了高度的活性;JNK通路能被细菌的脂多糖分子所激活,而机体中的有益和有害细菌都会释放脂多糖分子。脂多糖会通过血液从肠道流向肝脏啊中,最终通过激活JNK信号和其它信号通路来引发炎症,这种运输机制在遭受肝炎和脂肪肝的患者肝脏中非常常见。
研究结果表明,NLRP12能够抑制因肠道微生物和促癌信号引发的炎症,为了证实这种肠道-肝脏炎症-致癌假说,研究人员利用抗生素来治疗小鼠降低其肠道菌群的水平,结果发现,利用抗生素治疗剔除肠道菌群能够显著降低缺失Nlrp12的小鼠机体中肿瘤的生长,因此NLRP12或许是一种潜在的治疗靶点,而将当前的免疫检查点阻断剂疗法与增加肝脏中NLRP12的方法相结合或有望改善当前肝癌患者的治疗效果。免疫检查点阻断剂是一种新型疗法,其能通过机体免疫反应来杀灭癌细胞,当该策略开始发挥作用时其会变得非常有效,当通常情况下其并不是非常有效,因此研究人员就需要寻找其它方法来改善这种疗法的作用效果,本文研究中,研究人员就深入阐明了通过NLRP12来调节JNK通路的新型机制,后期或有望帮助开发治疗肝癌的新型疗法。
3.Nature:发现p38γ是肝癌的一个新的治疗靶标
doi:10.1038/s41586-019-1112-8
当前,肝癌几乎没有可用的治疗选择。一种参与细胞应激反应的酶可能成为治疗肝癌的新型药物靶点。在一项新的研究中,西班国立心血管病研究中心(CNIC)的Guadalupe Sabio及其团队发现作为p38激酶的四种类型之一的p38γ蛋白对肝细胞的细胞分裂起始至关重要。这表明“p38γ可能是肝癌的一种有用的治疗靶点”,Sabio说,“我们如今正在开发这种蛋白的抑制剂来测试这种癌症。”相关研究结果于2019年4月10日在线发表在Nature期刊上,论文标题为“p38γ is essential for cell cycle progression and liver tumorigenesis”。

图片来自CNIC。
Sabio对p38蛋白家族有着长期的兴趣,这些蛋白在遭受应激的细胞中被激活。如今,在这项新的研究中,她的研究团队证实p38γ在肝脏的细胞分裂起始中发挥着重要的作用。
“p38激酶家族的四个成员是如此相似以至于它们起初似乎具有重叠或冗余的功能”,Sabio说,“但是,由于与西班牙赫罗纳大学的Silvia Osuna和西班牙国家肿瘤研究中心(CNIO)的研究人员的合作,对它们的三维结构的详细分析显示,这四个成员中的p38γ也与另一个称为CDK的蛋白家族有着密切的相似之处。众所周知,这些蛋白是细胞分裂和细胞周期的的调节因子,并且在癌症产生中发挥着重要的作用。”
在研究与CDK的这种相似性的实验室研究中,这些研究人员发现CDK2抑制剂也降低了p38γ的活性。他们还发现p38γ和CDK2均作用于一种在调节细胞周期中起着重要作用的肿瘤抑制蛋白。
4.Cancers:鉴别出与肝细胞癌发生直接相关的关键基因
doi:10.3390/cancers11040486
肝细胞癌(HCC,Hepatocellular carcinoma)是一种常见的肝癌类型,这类癌症的发病率在过去十年中几乎翻了一翻,其成为了美国增长最快的癌症类型,同时也是全球人群因癌症死亡的第三大原因,近日,一项刊登在国际杂志Cancers上的研究报告中,来自美国转译基因组学研究院(TGen)的研究人员通过研究首次提出证据表明,酶AKR1B10或是肝细胞癌的潜在治疗靶点。
研究者Johanna DiStefano说道,如今研究者已经鉴别了基因(编码AKR1B10)和肝细胞癌之间的关联,AKR1B10不仅能作为治疗肝细胞癌的潜在靶点,还能帮助进行致死性疾病的早期诊断。更重要的是,AKR1B10在肝细胞癌的发生和进展过程中扮演着一种看似矛盾的角色,该基因的过量表达能够提示个体是否患有肝细胞癌,而一直该基因的表达似乎能够阻断癌症的进展和扩散。
如今美国每年大约有3.2万名患者死于肝癌,由于AKR1B10能作为肝细胞癌患者诊断和预后评估的潜在生物标志物,有研究表明,AKR1B10酶在肝细胞癌的发生及进展过程中扮演着关键角色;AKR1B10似乎能够影响肝细胞癌患者对当前化疗的耐受性,从而使得这类癌症非常难以治疗。与此同时研究者还发现,编码AKR1B10的基因发生高表达实际上与患者较好的预后、生存率增加及转移性癌症发生之间的关联是相互矛盾的,在肝细胞癌的不同阶段AKR1B10或许发挥着不同的功能。
5.JEM:突破!科学家从分子层面上解释为何男性更易患肝癌?
doi:10.1084/jem.20181288
近日,一项刊登在国际杂志Journal of Experimental Medicine上的研究报告中,来自西班牙国家心血管研究中心的科学家们通过研究发现,脂肪细胞分泌的一种特殊激素在女性机体中水平较高,这或能阻断女性机体肝脏细胞癌变,相关研究结果或能帮助解释为何肝细胞癌在男性群体中更常见,同时也有望帮助开发治疗肝癌的新型疗法。

图片来源:Manieri et al., 2019。
肝癌是全球第四大癌症相关死亡的原因,在美国男性患肝细胞癌的风险是女性的两倍,诱发这种性别差异的因素是一种名为脂联素(adiponectin)的激素,脂联素是脂肪细胞分泌,能够帮助控制机体的代谢,研究者Guadalupe Sabio解释道,相比男性而言,女性机体中循环的脂联素水平相对较高,然而脂联素在肝细胞癌发生过程中所扮演的关键角色目前在科学界仍然存在争议,还需要研究者进一步研究。
与人类相似,雄性小鼠也比雌性小鼠更易患肝细胞癌,这项研究中,研究者发现,雌性小鼠机体中脂联素水平的升高有助于帮助其抵御肝细胞癌的发生。脂联素能激活干细胞中两种特殊蛋白的表达,即p38α和AMPK,从而就能阻断细胞的增殖并抑制肿瘤生长。抑制雄性啮齿动物机体中睾酮的产生就能增加脂联素的水平并降低肿瘤的生长速度。研究者指出,睾酮能激活脂肪细胞中名为JNK1的蛋白的表达,而JNK1能够抑制脂联素的产生。
6.Hepatology:一种新型的组合性免疫疗法有望阻断肝癌的进展
doi:10.1002/hep.30528
近日,一项刊登在国际杂志Hepatology上的研究报告中,来自加利福尼亚大学Moores癌症研究中心的科学家们通过研究发现,将一种合成性的dsRNA聚胞苷酸(dsRNA-polylC)和程序性死亡配体1抗体(PD-L1抗体)相结合或有望有效阻断小鼠模型肝细胞癌的进展,并能促进部分小鼠模型机体中的肿瘤完全缓解以及保持无肿瘤存活状态。
这项研究中,研究者证实了此前在不同肝癌动物模型中的实验结果,他们发现,通过重编程巨噬细胞并激活自然杀伤细胞就能有效抑制肝脏肿瘤的开启,并能消除肿瘤开启细胞;此外研究者认为,通过增强先天性免疫力有望开发出一种肝癌预防性策略,这或将惠及很多肝癌高风险的慢性肝病患者。在分析为何polylC(聚胞苷酸)并不能产生肝癌的治疗效应上,研究者注意到,注射polylC能够潜在诱发肝脏中PD-L1的表达,随后研究人员将polylC与PD-L1抗体联合来检测这种组合性免疫疗法的作用效果。
当polylC与PD-L1抗体结合后,肝脏中活性CD8 T细胞的水平会明显增加,其会抑制肝脏中的肿瘤的进展,研究人员重点对原发性肝癌进行了研究,他们已经分析了这种组合性免疫疗法对转移性肝癌和晚期恶性疾病的影响,目前他们正在寻找最优的疗法剂量,同时还在考虑是否能通过加入额外的制剂来改善疗法的效率。
7.Cancer Prev Res:番茄中的番茄红素可减少脂肪肝、炎症和肝癌
doi:10.1158/1940-6207.CAPR-18-0188
在一项新的研究中,美国塔夫茨大学人类老年化营养研究中心副主任Xiang-Dong Wang及其团队研究了作为一种富含番茄红素的食物的番茄的癌症预防效果。在幼年时,小鼠感染了一种称为二乙基亚硝胺的肝脏致癌物,随后摄入不健康的高脂肪饮食,这种高脂肪饮食类似于西方饮食,含有或不含有含番茄红素的番茄粉。他们随后评估了番茄粉如何好地保护小鼠免受炎症和癌症。对人类来说,这相当于每天吃两到三个番茄或一份番茄酱意大利面。相关研究结果发表在2018年12月的Cancer Prevention Research期刊上,论文标题为“Dietary Tomato Powder Inhibits High-Fat Diet–Promoted Hepatocellular Carcinoma with Alteration of Gut Microbiota in Mice Lacking Carotenoid Cleavage Enzymes”。

鲜红的西红柿,图片来自flagstaffotos/wikipedia。
这些研究人员首次证实富含番茄红素的番茄粉能够有效地降低这些小鼠摄入的高脂肪饮食促进的脂肪肝、炎症和肝癌产生。给小鼠喂食番茄粉增加了有益菌群的丰富度和多样性,并阻止了一些与炎症有关的细菌的过度生长。
有趣的是,他们观察到番茄粉要比同样剂量的纯化番茄红素补充剂更有效地预防肝癌产生。这可能是由于天然番茄中其他营养成分的潜在有益作用,如维生素E、维生素C、叶酸、矿物质、酚类化合物和膳食纤维。
下一步将是在人体中开展高质量的随机临床试验,以更多地了解番茄中的番茄红素在降低炎症和肝脏疾病风险中的作用。与此同时,这些研究人员认为摄入富含番茄红素的天然食物可能比分离或纯化的番茄红素更有效地预防癌症。
8.Ange Chem Int Ed:科学家开发出新型基于铂的纳米颗粒 有望高效杀灭肝癌细胞
doi:10.1002/anie.201813149
近日,一项刊登在国际杂志Angewandte Chemie International Edition上的研究报告中,来自苏黎世联邦理工学院的科学家们通过研究发现,相比当前药物而言,利用铂纳米颗粒(platinum nanoparticles)有望高效杀死肝癌细胞。
近些年来,靶向性癌症药物的数量持续上升,然而常规的化疗制剂仍然在癌症疗法中扮演着关键角色,其中就包括能攻击并杀灭癌细胞的基于铂的细胞毒性制剂,但这些制剂通常会损伤健康组织并诱发严重的副作用;因此这项研究中,研究人员就鉴别出了一种新方法来帮助筛选更具选择性的癌症疗法。
当铂(II)被氧化时其常常会携带细胞毒性,而通常其以常规基于铂的化疗形式存在,而非氧化状态的铂(0)则对细胞的毒性较小;研究人员通过研究找到乐一种新方法将铂(0)引入到靶向细胞中随后其就会被转化成为铂(II),为了实现该目的,研究人员使用了非氧化的铂纳米颗粒,其首先必须用肽类来稳定;研究者对包含数千种肽类的文库进行筛选鉴别出了一种特殊肽类,其能使铂纳米颗粒维持稳定状态数年时间。
对癌细胞培养物进行检测,结果表明,铂(0)纳米颗粒能够渗入细胞中,一旦进入肝癌细胞的特殊环境后其就会被氧化成为铂(II)纳米颗粒并产生细胞毒性效应。随后研究人员对10种不同的人类细胞进行研究后发现,这种肽包裹的纳米颗粒能够高度选择性地杀灭肝癌细胞,其与药物索拉非尼具有相同的毒性效应,索拉非尼是当前用来治疗原发性肝脏肿瘤的最常用药物,相比索拉非尼而言,新型纳米颗粒的选择性更强,而且比化疗药物顺铂更加有效。
9.Cell Metabol:抗排斥药物雷帕霉素或能有效治疗某些肝癌
doi:10.1016/j.cmet.2019.01.002
近日,一项刊登在国际杂志Cell Metabolism上的研究报告中,来自匹兹堡大学的科学家们通过对动物模型和患者组织进行研究鉴别出了肝脏中的一条新型的分子通路,研究者指出,一种常用的抗排斥药物或能被重新定向来治疗特定类型的肝癌。
研究者Satdarshan Monga说道,我们发现,β-连环蛋白基因发生突变的肝癌或许对雷帕霉素更加易感,而雷帕霉素是一种常用作器官移植过程中的抗排斥药物,这或许就能帮助研究者重新考虑雷帕霉素的新用途,利用其开发治疗肝癌(尤其是耐药性肝癌)的新型疗法。研究者指出,肝脏中中央静脉周围的一系列细胞中常常携带高水平的mTOR蛋白,mTOR蛋白作为对细胞新陈代谢非常重要的营养和能量传感器,其在β-连环蛋白处于活性状态的相同细胞中存在。

图片来源:Cell Reports/University of Pittsburgh。
大约25%-30%的肝癌都携带β-连环蛋白基因突变,但研究人员并不是非常清楚这些突变如何以及为何会促进癌变细胞生长,因此当研究人员在β-连环蛋白基因突变的肝癌中发现高水平的活性mTOR时,他们就想知道是否这两种蛋白在功能上具有关联性。为了追踪mTOR激活的来源,研究者们开发了一种肝癌小鼠模型,使得小鼠机体中β-连环蛋白基因及名为Met的基因发生突变,随后研究者发现这些小鼠患肝癌的模式与人类非常相似。
当mTOR激活水平增加时,研究者通过对这些小鼠追踪后发现,β-连环蛋白能通过一种名为谷氨酰胺合成酶(GS)的中间酶类来激活mTOR,这些分子通路与能量摄入有关,作为快速生长的癌细胞,其往往能表现出更高活性的谷氨酰胺合成酶和mTOR。研究者Monga说道,这些肿瘤或许具有mTOR成瘾性,激活mTOR就能刺激细胞中蛋白质制造工厂的进程,从而给予癌细胞足够的能量分裂和生长。
当给遗传修饰的小鼠喂食雷帕霉素时,小鼠机体肿瘤的尺寸会下降,而当加入了另外一种抑制Met的药物时,肿瘤几乎被完全杀灭了,这就说明,mTOR在促进肿瘤生长上扮演着关键角色。研究者表示,此前在对肝癌患者的临床试验中并未发现雷帕霉素的明显有益效应,但本文研究结果表明,如果限定于携带β-连环蛋白突变和mTOR成瘾性肿瘤的患者,那么这种疗法或许会非常有效。
10.Hepatology:科学家发现PI3Kδ在肝细胞癌中发挥重要作用 或可成为新治疗靶点
doi:10.1002/hep.30307
I类PI3K信号途径是人类癌症发育和进展中一个重要的信号途径。在PI3K的四个亚型中,PI3Kα和PI3Kβ是普遍表达的,而PI3Kγ和PI3Kδ主要发现于白细胞中。在实体瘤中靶向PI3K的治疗策略主要是针对PI3Kα和PI3Kβ介导的癌细胞内PI3K活性。PI3Kδ在实体瘤中的作用还不清楚。最近来自韩国的学者们利用RNA测序、芯片和液相色谱-串联质谱等方法对肝细胞癌(HCC)细胞、晚期HCC病人来源的肝癌细胞和小鼠模型等进行了分析以建立PI3Kδ在HCC中发挥的作用。相关研究结果发表在国际学术期刊Hepatology上。
在这项研究中,研究人员首先建立了一个化合物诱导肝癌模型来反映晚期HCC的恶性表型和体内环境,在这个晚期HCC模拟系统中,用双氧水处理HCC细胞,发现双氧水能够特异性增加PI3Kδ的活性而降低I类PI3K其他亚型的活性。利用抑制剂或小干扰RNA介导PI3Kδ基因沉默阻断PI3Kδ活性能够显著抑制HCC细胞增殖并减弱恶性HCC的一些关键特征,包括上调TERT(telomerase reverse transcriptase)的表达。
从机制上来说,双氧水诱导SERPINA3发生氧化修饰,阻止其泛素依赖性降解过程,并增强其作为PI3Kδ和TERT转录激活因子的活性。进一步的研究发现HCC中PI3Kδ的高表达与病人的不良生存率存在关联,而且晚期HCC进展与发生氧化修饰的SERPINA3,PI3Kδ和TERT的蛋白水平存在正相关关系。(生物谷 Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->


