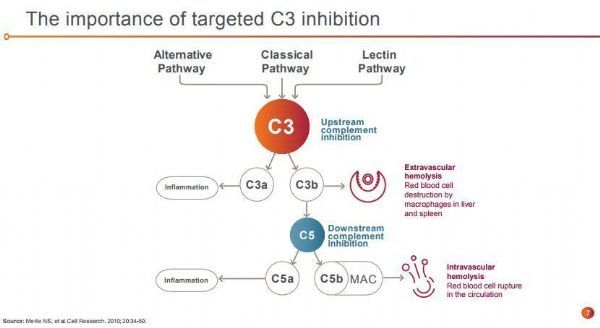
罕见病新药!C3抑制剂pegcetacoplan治疗阵发性睡眠性血红蛋白尿症(PNH)疗效击败Soliris!
来源:本站原创 2021-03-18 22:42
Soliris是Alexion开发的PNH标准护理疗法,阿斯利康豪掷390亿美元将其收购。

2021年03月18日讯 /生物谷BIOON/ --Apellis Pharma是C3靶向疗法开发方面的领导者,致力于通过开创性的靶向C3方法开发首创和同类最佳疗法,用于治疗由补体级联反应的不受控或过度激活所驱动的广泛疾病,包括血液学、眼科学和肾脏学领域的疾病。
近日,Apellis与瑞典制药公司Swedish Orphan Biovitrum AB(SOBI)联合宣布,评估pegcetacoplan(APL-2,一种C3抑制剂)治疗的阵发性睡眠性血红蛋白尿症(PNH)头对头3期PEGASUS研究(NCT03500549)的结果,已发表于国际医学期刊《新英格兰医学杂志》(NEJM)。该研究在接受PNH标准护理药物Soliris(eculizumab,一种C5抑制剂)但仍存在持续性贫血的成人患者中开展。结果显示,治疗16周,与Soliris相比,pegcetacoplan显示出优越性:血红蛋白水平在统计学上显著改善、关键临床结果也表现出改善。这些数据证实了pegcetacoplan提升PNH护理标准的潜力,有望重新定义PNH的治疗。
pegcetacoplan是一种C3抑制剂,治疗PNH的新药申请(NDA)正在接受美国FDA的优先审查,目标行动日期为2021年5月14日。此外,pegcetacoplan治疗PNH的营销授权申请(MAA)也正在接受欧洲药品管理局(EMA)的审查。
Soliris是Alexion公司的一款重磅C5补体抑制剂,已被批准治疗多种罕见病,是治疗PNH的标准护理疗法。2020年12月,阿斯利康以390亿美元巨资将Alexion收购,进军罕见病领域。
当前,PNH治疗仍然需要新的治疗方法。因为许多接受C5抑制剂治疗的PNH患者仍然贫血,导致中重度疲劳,还有一部分患者继续需要输血。来自3期PEGASUS研究的数据,强调了pegcetacoplan作为PNH护理一项重大进步的潜力。如果获得批准,pegcetacoplan有潜力通过提供更全面的疾病控制来提高PNH的护理标准。
PEGASUS是一项多中心、随机、开放标签、阳性药物对照、头对头3期研究,在80例PNH成人患者中开展,评估了pegcetacoplan相对于Soliris的疗效和安全性。该研究中,受试者必须一直在接受Soliris治疗(稳定治疗至少3个月),并且在筛查访视时血红蛋白水平<10.5g/dL。在为期4周的导入期,患者接受每周2次1080mg剂量pegcetacoplan,同时接受其当前剂量的Soliris治疗。在16周的随机对照期内,患者随机分配接受1080mg剂量pegcetacoplan(每周2次)或其当前剂量的Soliris。所有完成16周随机对照期的受试者(n=77)进入开放标签期,从第17周至第48周接受pegcetacoplan治疗。
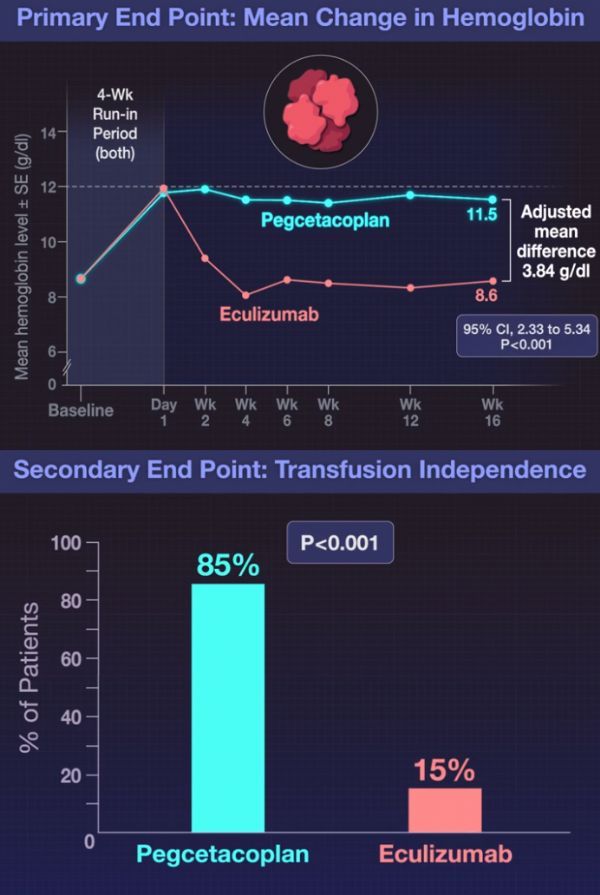
发表于NEJM上的结果证实,pegcetacoplan达到了研究的主要疗效终点:在第16周,显示出pegcetacoplan相对于Soliris的优越性,2个治疗组血红蛋白水平校正平均值为3.84g/dL,在统计学上显著改善。此外,pegcetacoplan治疗组有85%的患者在16周内无输血,而Soliris治疗组为15%。通过慢性病治疗功能评估(FACT)-疲劳评分测量,疾病的关键标志物如绝对网织红细胞计数、乳酸脱氢酶(LDH)和疲劳有显著改善。
在该研究中,pegcetacoplan和Soliris的安全性具有可比性。pegcetacoplan组41例患者中有7例(17%)出现严重不良反应(SAE),Soliris组39例患者中有6例(15%)出现SAE。2个治疗组均无脑膜炎病例和死亡报告。在为期16周的随机对照治疗期间,pegcetacoplan组和Soliris组最常见的不良反应分别为注射部位反应(37% vs 3%)、腹泻(22% vs 3%)、突破性溶血(10% vs 23%)、头痛(7% vs 23%)和疲劳(5% vs 15%)。
PEGASUS研究的48周顶线结果于最近公布:显示疾病的关键标志物持续改善,安全性与先前报道的数据一致。
值得一提的是,pegcetacoplan是第一个在血红蛋白水平上显示出优于Soliris的研究性疗法,高达85%接受pegcetacoplan治疗的患者没有输血。而目前接受Soliris治疗的PNH患者中,大多数都患有持续性贫血。PEGASUS研究的结果显示,pegcetacoplan有潜力成为PNH患者的新护理标准。
pegcetacoplan是一种研究性、靶向性C3抑制剂,旨在调节补体过度激活,这是导致许多严重疾病发生和发展的原因。pegcetacoplan是一种合成的环肽,与一种聚乙二醇聚合物结合,特异性地与C3和C3b结合。目前,pegcetacoplan正被开发用于治疗多种疾病,包括PNH、地图样萎缩(GA)和C3肾小球病。在美国,FDA已授予pegcetacoplan治疗PNH和GA的快速通道资格。
Soliris是Alexion公司销售的一款药物,这是一种首创的补体抑制剂,通过抑制补体级联反应终端部分的C5蛋白发挥作用。补体级联反应是免疫系统的一部分,其不受控激活在多种严重的罕见病和超级罕见病中发挥了重要作用。Soliris于2007年首次获准上市,之前已获批多种超级罕见病:PNH、非典型溶血尿毒症综合征(aHUS)、抗AchR抗体阳性全身性重症肌无力(gMG)、抗水通道蛋白-4(AQP4)抗体阳性的视神经脊髓炎谱系障碍(NMOSD)。
Soliris是全球最畅销的孤儿院之一。目前,Alexion公司也正在开发Soliris的升级版产品Ultomiris,后者已于2018年12月获得FDA批准PNH适应症。2019年10月,Ultomiris获FDA批准新适应症:治疗aHUS儿童和成人患者。Ultomiris是第一种也是唯一一种每8周给药一次的长效C5补体抑制剂,在治疗PNH的III期临床研究中,Ultomiris每2个月(8周)输注一次与Soliris每2周输注一次在全部11个终点方面均达到了非劣效性。(生物谷Bioon.com)
原文出处:The NEJM publishes phase 3 PEGASUS study results comparing pegcetacoplan to eculizumab for PNH
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->