近期肠道微生物重要研究成果解读!
来源:本站原创 2020-09-25 20:40
本文中,小编汇总了多篇重要研究成果,共同解读近期科学家们在微生物组研究领域的新发现!与大家一起学习!图片来源:CC0 Public Domain【1】Science:新发现!肠道微生物或会影响机体的代谢过程!doi:10.1126/science.abd6176生活在我们机体消化系统中的10万亿个细菌或许并不是人类的,但他们似乎会像机体的心脏或肝脏一样,是我
本文中,小编汇总了多篇重要研究成果,共同解读近期科学家们在微生物组研究领域的新发现!与大家一起学习!
图片来源:CC0 Public Domain
【1】Science:新发现!肠道微生物或会影响机体的代谢过程!
doi:10.1126/science.abd6176
生活在我们机体消化系统中的10万亿个细菌或许并不是人类的,但他们似乎会像机体的心脏或肝脏一样,是我们机体不可或缺的一部分,近年来越来越多的研究报告指出,肠道微生物会直接影响从肠道运动到机体行为等多方面的生物过程;近日,一项刊登在国际杂志Science上的研究报告中,来自洛克菲勒大学等机构的科学家们通过对小鼠进行研究揭示了肠道微生物塑造机体代谢的分子机制,文章中,研究人员识别出了一种特殊类型的肠道神经元或能控制机体的血糖水平并影响机体食欲,相关研究结果或有望帮助开发治疗诸如肥胖和糖尿病等机体代谢障碍,这些疾病与机体血糖水平密切相关,同时也与肠道菌群的组成有关。
研究者Paul Muller博士指出,我们都知道,肠道微生物会产生特殊的代谢产物,其能够模拟神经递质并被肠道中的神经元细胞所检测到,如今我们发现了肠道微生物活性和宿主行为(比如进食)之间的直接关联。肠道被神经元包围着,就其本身而言,其可以被看作是一种神经系统,而肠道常常因为复杂而被研究者称之为人体的第二大脑,这些神经元能通过关注多种分子线索来帮助机体进行消化和运动,其中大部分被认为来自我们日常的饮食或肠道微生物。
【2】Physiol Geno:揭示睡眠质量不佳、高血压和机体肠道微生物组之间的神秘关联!
doi:10.1152/physiolgenomics.00039.2020
近日,一项刊登在国际杂志Physiological Genomics上的研究报告中,来自伊利诺伊大学等机构的科学家们通过研究揭示了睡眠干扰、高血压和肠道微生物组改变之间的关联,文章中,研究人员旨在确定是否为期28天的睡眠干扰会改变大鼠体内的微生物组,肠道微生物组指的是生活在肠道中的微生物集合,研究者想通过研究识别出与动脉血压变化不良相关的生物学特性。
利用大鼠进行研究,研究人员干扰了大鼠的睡眠周期,大鼠是夜行动物,因此研究者所设计的实验能干扰其白天的睡眠周期,研究者使用遥测发射机(telemetry transmitters)测定了大鼠的大脑活性、血压和心率,同时还对其粪便进行分析来发现肠道菌群的改变情况;研究者Maki表示,当大鼠的睡眠周期或计划发生异常时,其血压就会增加,即使当其睡眠周期回归至正常时,其机体血压依然会维持升高水平,这就表明,功能失调的睡眠或会一段时间内损伤机体健康。
【3】Nature:新发现!机体感染病原体之前 肠道微生物或会塑造机体多种抗体的产生!
doi:10.1038/s41586-020-2564-6
B细胞是一种能发育产生抗体的白细胞,其所产生的抗体/免疫球蛋白能与有害的外来颗粒(病毒或致病菌等)结合并阻断其对宿主的入侵及对机体细胞的感染,每一个B细胞都会携带单一的B细胞受体(BCR)其能帮助确定所结合的外源性物质,这就好像每个锁子能接受一个不同的钥匙一样。机体中拥有数百万个携带不同受体的B细胞,B细胞的巨大多样性源于编码受体基因的重新排列,所以每个B细胞表面的受体都会略有不同,从而就会使其能够识别数十亿种不同的有害性分子;此外,肠道微生物还能诱发这些B细胞群体的扩张和抗体的产生,但直到现在,研究人员并不清楚是否这是一个随机的过程,还是肠道微生物的分子自身影响了结果。
近日,一项刊登在国际杂志Nature上的研究报告中,来自伯尔尼大学等机构的科学家们通过研究分析了该系统中编码抗体产生的数十亿个基因的表达情况,该系统能让科学家们了解基因对单个良性肠道微生物的反应。肠道内生存的良性微生物的数量与体内的细胞数量大致相同,大部分细菌都会停留在肠道内而无法穿透机体组织,但不幸的是,肠道菌群的有些渗透过程是无法避免的,因为肠道仅仅拥有一层细胞,其能将我们吸收食物营养所需要的血管与血管内部分开/隔绝开。
【4】Immunity:肠道微生物组或能将压力转换为镰刀细胞病
doi:10.1016/j.immuni.2020.06.025
日前,一篇刊登在国际杂志Immunity上的研究报告中,来自阿尔伯特-爱因斯坦医学院等机构的科学家们通过度小鼠进行研究揭示了慢性心理压力如何导致痛苦的血管阻塞发作,血管阻塞发作是镰刀状细胞病(SCD, sickle-cell disease)的常见并发症,同时也是诱发患者入院治疗的主要原因;研究者表示,肠道微生物组或在诱发血管阻塞发作上扮演着关键角色,相关研究结果或能帮助研究人员开发有效预防这种疾病的新型疗法。
SCD在非洲裔美国人群中的比例大约为1/365,患者机体通常会携带一种基因突变,该突变会导致异常血红蛋白的产生,同时会促进红细胞变成镰刀状并且变得不再灵活,而镰刀状红细胞如何阻塞小血管,阻碍血液流动以及氧气达到组织中,这或许就会导致疼痛和衰弱的血管闭塞发作(VOE),且会持续数天;目前并没有疗法能够逆转VOE,而且随着时间推移,其就会对内脏造成严重的损伤,这也是严重的SCD患者预期寿命要比非SCD患者短20-30年的主要原因。
doi:10.1016/j.cell.2020.05.036
如果不及时治疗,霍乱会在数小时内导致患者死亡,每年患病人数多达400万。在一项新的研究中,来自美国加州大学河滨分校的研究人员描述了肠道细菌如何帮助人们抵抗这种疾病。相关研究结果发表在Cell期刊上;细菌生活在地球上的各个角落--甚至是人体内部。加州大学河滨分校微生物学家Ansel Hsiao研究生活在我们体内的细菌(统称为人类微生物组)是否可以保护人们免受霍乱弧菌等外部细菌引起的疾病。霍乱弧菌生活在水道中并引起霍乱。
Hsiao的研究团队研究了孟加拉国人们的肠道微生物组,在这个国家,许多人因食物、水受污染和卫生设施差而患上霍乱。Hsiao解释说,“当人们生病时,腹泻会被冲入人们饮用的水系统中,这是一个负循环。他的团队想看看之前的感染或其他压力,如营养不良,是否使人们更容易受到影响,相比之下,美国人没有面临这些相同的压力。

图片来源:Janie Kim. Published in Cell
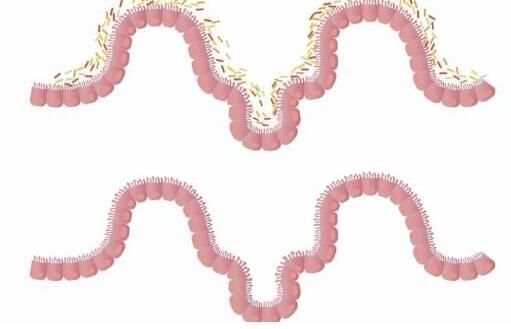
【6】Nature子刊:肠道微生物穿过破损肠道壁造成结直肠癌!
doi:10.1038/s43018-020-0070-2
来自比利时佛兰德斯生物技术研究院VIB-UGent炎症研究中心和根特大学的研究小组进行的一项合作研究揭示了导致结直肠癌的一种新机制。研究人员发现,Zeb2蛋白的异常表达会影响肠壁或'上皮'的完整性。"正常情况下,这种上皮细胞起到屏障的作用,防止肠道微生物渗透。"Zeb2破坏了这一屏障,并允许渗透细菌引起炎症,从而导致癌症进展。重要的是,科学家证明了控制免疫系统或去除微生物群可以防止癌症的发展。这些发现可能会带来新的治疗方法,并发表在Nature Cancer杂志上。
结直肠癌是第三种最常见的癌症,第四种最致命的癌症。不幸的是,包括免疫疗法在内的抗癌疗法在结直肠癌中疗效相对较低。除了遗传因素,与西方生活方式相关的环境因素(如饮食、肥胖和久坐的生活方式)也会增加患结肠直肠癌的风险。这种疾病起源于肠道上的上皮细胞。随着时间的推移,这些"屏障"细胞积累突变并获得恶性特性。更好地理解负责结直肠癌发展的分子机制对于开发新的治疗方法来有效地对抗这一致命疾病是至关重要的。
doi:10.1016/j.cell.2020.05.001
普林斯顿大学(Princeton University)的研究人员开发了一种系统的方法,用于评估我们肠道中的微生物群落如何以化学方式转化或代谢口服药物,从而影响其安全性和有效性;新的方法提供了肠道细菌如何代谢药物的更完整的图像,并可能有助于开发更有效、副作用更少、个性化的药物,这项研究发表在Cell杂志上;之前的研究已经考察了单一种类的肠道细菌是如何代谢口服药物的。新的框架可以一次性评估一个人的整个肠道微生物群落。
研究者表示,基本上,我们不会逃避微生物群的复杂性,而是欣然接受它。这种方法允许我们获得微生物对药物代谢的整体和更现实的看法。研究小组用这种方法来评估肠道微生物对市场上数百种常见药物的影响。肠道是药丸和液体药物被人体吸收的主要部位。研究人员发现了57种肠道细菌可以改变现有的口服药物。其中80%以前没有报道过,这强调了该方法揭示未知药物-微生物组相互作用的潜力。
【8】Nature:肠道微生物组或会影响肌萎缩侧索硬化症患者的预后
doi:10.1038/s41586-020-2288-7
近日,一项刊登在国际杂志Nature上的研究报告中,来自哈佛大学等机构的科学家们通过研究在神经退行性疾病肌萎缩性侧所硬化症(ALS)中识别出了一种新型的肠-脑连接,通过对常见ALS基因突变的小鼠进行研究,研究者发现,利用抗生素或粪便移植的方式来改变肠道微生物组或能抑制会改善机体的疾病症状。
相关研究结果或能帮助解释为何某些个体会携带诱发ALS的突变,同时基于微生物组研究人员或许也能开发出一种可能性的治疗性手段。研究者Kevin Eggan表示,本文研究中我们重点对ALS患者机体中最常见的突变基因进行研究,结果发现,相同的小鼠模型(相同的遗传特性)在不同的实验设施条件下或许会表现出显著不同的健康结果;随后研究者追踪了这些小鼠机体中不同肠道菌群的不同结局,他们假设,为何携带突变的某些个体会患上ALS,而其他个体则不会?
【9】深度剖析!肠道微生物组如何与免疫系统互联来诱发胆汁淤积性肝病的发生?
doi:10.1002/hep.31228
如今,越来越多的研究证据表明,胆汁淤积性肝病(cholestatic liver disease)与机体微生物组组成的改变之间存在一定关联,然而研究人员并不清楚微生物组在这种疾病发病机制中所扮演的关键角色;日前,一项刊登在国际杂志Hepatology上题为“Intestinal microbiome-macrophage crosstalk contributes to cholestatic liver disease by promoting intestinal permeability”的研究报告中,来自Quadram生物科学研究所等机构的科学家们就通过研究深入解析了肠道微生物如何与免疫系统细胞相互作用来诱发胆汁淤积性肝病的发生。
机体肠道是一道选择性屏障,其能阻断致病菌进入体内,同时又能促进机体对营养的吸收,在肠道中,微生物组、免疫细胞和上皮细胞之间的串扰互联对于维持机体肠道屏障功能至关重要;肠道通透性会受到免疫系统的严格调节,因为诸如TNF和IFNγ等细胞因子能调节紧密连接蛋白(TJ 蛋白,tight junction proteins)的表达。在肠道中,微生物组会塑造免疫系统从而为微生物和宿主细胞共存提供一个耐受的环境,反之,炎性则会决定肠道微生物组的组成,从而为肠道通透性和屏障功能的调节增加另一层复杂性。
【10】Science:新发现!母亲机体的肠道微生物或能塑造后代机体的代谢状况
doi:10.1126/science.aaw8429
近日,一项刊登在国际杂志Science上的研究报告中,来自东京农工大学等机构的科学家们通过对小鼠进行研究发现,目前的肠道微生物或能塑造后代后期生活中机体的代谢状况,文章中,研究人员描述了他们对小鼠的研究结果以及该研究结果的意义。
研究者表示,目前研究人员进行了大量研究来阐明母亲机体肠道微生物组对婴儿健康的影响,但却很少有人研究母亲肠道微生物组和婴儿肠道微生物组之间的关联,基于此,研究人员就想通过研究来阐明母亲机体微生物组在后代后期生活中患代谢性疾病(与母亲孕期微生物组所发生的改变相关)上所扮演的关键角色,研究人员对生活在正常和无菌状况下的怀孕小鼠进行研究来观察其二者之间是否存在差异。(生物谷Bioon.com)
生物谷更多精彩盘点!敬请期待!
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


