镰状细胞病(SCD)基因疗法!蓝鸟生物Zynteglo获欧盟授予优先药物资格(PRIME)!
来源:本站原创 2020-09-24 16:33
Zynteglo已在欧洲上市,定价1210万人民币!

2020年09月24日讯 /生物谷BIOON/ --蓝鸟生物(bluebird)是一家行业领先的基因治疗公司。近日,该公司宣布,欧洲药品管理局(EMA)已授予Zynteglo(LentiGlobin,bb1111,含βA-T87Q珠蛋白编码基因的自体CD34+细胞)治疗镰状细胞病(SCD)的优先药物资格(PRIME)。此前,EMA还授予了Zynteglo治疗SCD的孤儿药资格(ODD)。在美国,FDA还授予了Zynteglo治疗SCD的ODD、快速通道资格(FTD)、再生医学先进疗法资格(RMAT)、罕见儿科疾病资格(RPDD)。
Zynteglo是一种一次性基因疗法,开发用于治疗SCD和β地中海贫血。2019年5月,Zynteglo获得欧盟有条件批准,用于适合造血干细胞(HSC)移植但没有人类白细胞抗原(HLA)匹配的HSC供体、年龄在12岁以上、非β0/β0基因型输血依赖性β地中海贫血(transfusion-dependent β-thalassemia,TDT)患者的治疗。
值得一提的是,Zynteglo是全球首个治疗TDT的基因疗法,可解决TDT的内在基因病因,有潜力使患者摆脱输血依赖(输血非依赖),一旦实现这一点,预计将持续终身。目前,蓝鸟生物也正在推进Zynteglo在美国的监管审查。
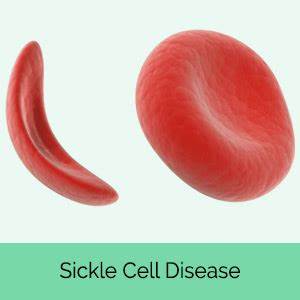
SCD(图片来源:nursingcrib.com)
PRIME是EMA在2016年3月推出的一个快速审批项目,与美国FDA的BTD项目相似,旨在加速医药短缺领域重点药品的审评进程,尽早使患者受益。入围PRIME的实验性药物,将在临床试验及药品开发方面获得EMA的大力支持,以加速真正创新药物的开发及审批,来满足对有前景新药的医疗需求。获得PRIME资格的药物,必须有初步临床证据和非临床证据表明该药与现有治疗药物相比能够实质性改善病情。
已完成的1/2期HGB-205研究、正在进行的1/2期HGB-206研究和正在进行的长期安全性和有效性随访研究LTF-303的临床数据,支持了EMA授予Zynteglo治疗SCD的PRIME资格认定。
SCD是一种严重的、进行性的、使人衰弱的遗传性疾病,由β-珠蛋白基因突变导致异常镰状血红蛋白(HbS)的产生。HbS使红细胞变得病态和脆弱,导致慢性溶血性贫血、血管病变、难以捉摸的和痛苦的血管阻塞危象(VOC)。对于患有SCD的成人和儿童来说,这意味着痛苦的危机和其他改变生命或威胁生命的急性并发症,如急性胸腔综合征(ACS)、中风和感染。如果患者在急性并发症、血管病变和终末器官损害中存活,由此产生的并发症可导致肺动脉高压、肾功能衰竭和早期死亡。
Zynteglo将改良版本的β珠蛋白基因(βA-T87Q-珠蛋白基因)的功能拷贝添加到患者自身的造血干细胞(HSC)中,一旦回输体内后,患者就拥有了βA-T87Q-珠蛋白基因,其红细胞就能够产生抗镰状血红蛋白HbAT87Q,降低HbS的比例,从而减少镰状红血球、溶血等并发症。

输血依赖性β地中海贫血(TDT)也是一种严重的遗传病,由β-珠蛋白基因突变引起,导致成人血红蛋白(HbA)显著减少或缺失。为了生存,TDT患者通过终生慢性输血维持血红蛋白水平。由于不可避免的铁超载,这些输血有进行性多器官损害的风险。
Zynteglo将改良版本的β珠蛋白基因(βA-T87Q-珠蛋白基因)的功能拷贝添加到患者自身的造血干细胞(HSC)中,一旦回输体内后,患者就拥有了βA-T87Q-珠蛋白基因,有潜力在体内产生足够水平的HbAT87Q,这是一种基因治疗来源的血红蛋白,从而消除或显著减少输血需求。
Zynteglo是一种一次性的基因治疗方法,可解决TDT的内在基因病因,有潜力使患者摆脱输血依赖(输血非依赖),一旦实现这一点,预计将持续终身。在临床试验中,高达75%-80%的患者摆脱了对输血的依赖,并且所有已摆脱输血依赖的患者均维持输血非依赖,已有患者超过6年没有接受输血。和过去频繁的输血相比,是一个重大进步。

目前,Zynteglo已在欧洲上市,其价格高达157.5万欧元(约合1210万人民币),是继诺华脊髓性肌萎缩症(SMA)一次性基因疗法Zolgensma之后全球第二贵药物,后者的官宣定价为212.5万美元,约合人民币1460万元。
不过,蓝鸟生物提出了创新付款模式,患者可分五期进行分期付款。首次付款是在Zynteglo输注时支付。只有在患者此后不需要输血治疗TDT的情况下,才支付剩余的四次分期付款,每年一付。(生物谷Bioon.com)
原文出处:bluebird bio’s LentiGlobin™ for Sickle Cell Disease Gene Therapy (bb1111) Granted Priority Medicines (PRIME) Designation by European Medicines Agency
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->


