多篇重要成果解读肿瘤微环境研究新进展!
来源:本站原创 2020-02-29 09:21
本文中,小编对近年来科学家们在肿瘤微环境研究领域取得的新成果进行整理,分享给大家!图片来源:www.pixabay.com【1】Cell Rep:靶向肿瘤微环境有助于抑制癌症doi:10.1016/j.celrep.2020.01.011人类免疫系统调节并控制了识别微生物感染以及外界异物的入侵。这种天然的免疫反应依赖于重要的新陈代谢和细胞过程,从而达到抵抗感
本文中,小编对近年来科学家们在肿瘤微环境研究领域取得的新成果进行整理,分享给大家!
图片来源:www.pixabay.com
doi:10.1016/j.celrep.2020.01.011
人类免疫系统调节并控制了识别微生物感染以及外界异物的入侵。这种天然的免疫反应依赖于重要的新陈代谢和细胞过程,从而达到抵抗感染和其他疾病的目的。然而,免疫系统的相关反应也参与了全身性疾病和癌症的发展。因此,进一步了解免疫系统细胞反应中涉及的基本生化过程至关重要,并且有助于开发针对系统性疾病和癌症的新疗法。
免疫系统的复杂性包括其含有不同的细胞类型。其中,巨噬细胞有两种类型:M1和M2型,它们参与了炎症防御机制(M1),也参与了愈合过程(M2)。M2型巨噬细胞还与癌细胞结合并促进其生长(肿瘤相关巨噬细胞,TAM)。这项新研究中,研究人员发现了一种新型的“生化开关”,涉及M2巨噬细胞的极化和增殖。这个生化检查点从糖酵解途径分支出来,为快速细胞增殖和分化提供原材料。如果该途径被抑制,则M2极化和增殖会受到抑制。这一现象对理解TAM和治疗癌症有着直接的影响。
【2】Science子刊:揭示GCN2抑制肿瘤微环境中的抗肿瘤免疫反应
doi:10.1126/sciimmunol.aax8189
肿瘤相关巨噬细胞(TAM)和髓样抑制细胞(MDSC)抑制肿瘤微环境中的T细胞功能。蛋白GCN2(general control nonderepressible 2)是一种环境传感蛋白,可根据营养供应情况控制转录和翻译。虽然GCN2是免疫肿瘤学中的一种潜在的治疗靶点,但是它在塑造肿瘤免疫反应中的作用尚不清楚。在一项新的研究中,来自加拿大、美国、巴西和意大利的研究人员通过使用质谱流式细胞技术(mass cytometry)、转录组学和转录因子结合分析来确定GCN2对黑色素瘤中的髓样抑制细胞表型和免疫反应的功能性影响,相关研究结果近期发表在Science Immunology期刊上。
研究者发现,髓样抑制细胞中的GCN2缺失促进肿瘤相关巨噬细胞和髓样抑制细胞的表型转变,从而促进了抗肿瘤免疫反应;飞行时间质谱流式细胞技术(time-of-flight mass cytometry, CyTOF)和单细胞RNA测序表明这是由于肿瘤微环境的变化:巨噬细胞和髓样抑制细胞的促炎性活化的增加和肿瘤内CD8+ T细胞中的干扰素-γ表达。
【3】Cancer Res:揭秘癌基因改变肿瘤微环境促进肿瘤进展的关键角色
doi:10.1158/0008-5472.CAN-18-3604
肿瘤微环境(TME,tumor microenvironment)是液体、免疫细胞及包裹肿瘤的血管所组成的混合体,肿瘤细胞与TME之间的相互作用能够帮助决定肿瘤的进展和命运;因此,理解TME的组成和功能对于有效抑制癌症进展至关重要,尽管多种遗传突变会增加癌症的发病率,但研究人员并不清楚TME对癌症发病的影响,近日,一项刊登在国际杂志Cancer Research上的研究报告中,来自日本金泽大学的科学家们通过研究报道了抗癌基因RB所扮演的关键角色。
视网膜母细胞瘤基因(RB,Retinoblastoma gene)是一种肿瘤抑制基因,其突变后会促进肿瘤生长;文章中,研究人员首先在患肉瘤的小鼠机体中失活RB,随后观察其对肿瘤生长的效应,结果表明,这些小鼠机体中的肿瘤的确增大了。当研究人员对TME进行分析后发现,新生血管的存在会滋养癌细胞,同时研究者还在TME中发现了新招募的免疫抑制性细胞,这些细胞能够克服机体的天然防御系统,同时RB基因的失活还会帮助TME促进癌症进展。
【4】Lasers Surg Med:低剂量光动力学疗法可以调控肿瘤微环境
doi:10.1002/lsm.23069
一项新的研究揭示了低剂量光动力疗法影响血管微结构的机制。通过体外共培养周细胞和内皮细胞,研究人员发现低剂量光动力疗法通过Rho、肌球蛋白轻链和局灶性粘附激酶磷酸化(MLC‐P, FAK‐P)来激活周细胞。这导致细胞骨架重构,导致周细胞更有效地收缩三维胶原凝胶。
在发现这些体外现象之后,研究人员在两个体内恶性胸膜间皮瘤模型中证实了他们的发现。他们发现,低剂量光动力疗法可引起周细胞的MLC-P,这与内皮细胞的周细胞覆盖率增加有关。血管结构的这种变化与肿瘤间质液压力的降低和肿瘤中大分子分布的增强有关。
【5】PLoS Pathog:引起卡波西肉瘤的病毒会劫持外泌体调控肿瘤微环境
doi:10.1371/journal.ppat.1007596
一项由北卡罗莱纳大学(University of North Carolina,UNC)莱恩伯格综合癌症研究中心的研究人员完成的最新研究表明一种和癌症相关的病毒可以劫持宿主的细胞包裹,从而促进肿瘤周围环境的改变。这项研究于近日发表在《PLOS Pathogens》上,该研究表明卡波西肉瘤相关的疱疹病毒能够霸占宿主细胞用于输送物质到周围环境的包裹系统。这些包裹叫做细胞外囊泡(或者外泌体),其中包含的物质可以引起周围细胞发送信号的方式、移动方式以及其他效应的改变。
研究者表示,我们的研究表明卡波西肉瘤相关的疱疹病毒使用外泌体对肿瘤周围的环境进行了重塑;这种病毒可以在不感染细胞的情况下完成这个过程。相反的是,肿瘤环境周围的细胞会被这些病毒修饰后的外泌体攻击。这导致信号传递被激活、细胞因子释放以及细胞基因表达谱的重置。卡波西肉瘤是一种癌细胞位于血管或者淋巴管壁的癌症,由卡波西肉瘤相关的疱疹病毒感染导致;最常见的卡波西肉瘤发生在感染了HIV或者免疫系统功能被削弱的人体内,感染KSHV还会引起其他癌症,包括原发性积液淋巴瘤,这是一种生成抗体的B细胞瘤。
图片来源:Advanced Materials
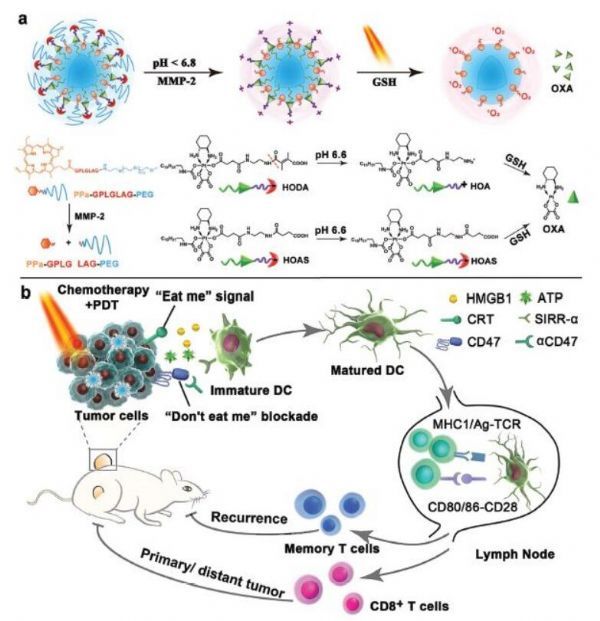
【6】Adv Mat:科学家开发肿瘤微环境响应纳米前药递送系统克服肿瘤免疫抑制
doi:10.1002/adma.201805888
据报道化学免疫疗法可以通过刺激产生免疫原性细胞死亡(immunogenic cell death,ICD)来激活产生强烈的T细胞抗癌免疫反应,基于此目前已经有数个相关的临床试验正在进行中;但是现在的化学免疫疗法仅应用于一小部分病人,主要原因是药物递送效率低以及肿瘤微环境的免疫抑制效应。为了解决这个些问题,近日来自中科院上海药物研究所等机构的研究人员开发了一种肿瘤微环境激活的前药系统利用ICD进行肿瘤的化学免疫治疗,相关研究成果于近日发表在Advanced Materials杂志上。
这个前药系统将奥沙利铂前药和聚乙二醇化的光敏剂整合在一起,展现出了针对肿瘤酸性和酶微环境相应的肿瘤特异性的富集、活化和深度渗透等特点。研究人员发现共递送奥沙利铂前药和光敏剂和以促使肿瘤细胞发生免疫原性细胞死亡。而这种前药系统与抑制CD47的抗体联合使用可以进一步增强树突状细胞的成熟,促进树突状细胞呈递抗原,最终增强抗肿瘤免疫反应。
【7】Cell:令人吃惊!成功的免疫检查点疗法广泛地重塑肿瘤微环境
doi:10.1016/j.cell.2018.09.030
如今,免疫检查点疗法彻底改变了临床治疗转移性黑色素瘤患者的方式,而且自2011年首次被批准以来,它们给那些预后非常差(平均生存期低于一年)的和具有很少治疗方法的患者带来了新的希望。即便黑色素瘤对免疫检查点抑制具有较高的反应率:大约40%的患者对PD-1免疫检查点疗法作出反应,但是大多数患者要么没有作出反应,要么在治疗后会复发。
之前针对肿瘤对PD-1或其他免疫检查点抑制剂作出反应的研究主要集中在肿瘤相关因子,包括肿瘤中的突变数量、PD-L1(一种与受体PD-1结合的配体)水平、CD8 T细胞丰度和炎性基因表达。在治疗开始前或治疗后不久,检测这些肿瘤相关因子,但是它们具有有限的预测患者治疗结果的能力。在一项新的研究中,来自美国华盛顿大学医学院的研究人员通过对利用免疫检查点疗法成功治疗的荷瘤小鼠进行高维分析,发现免疫检查点疗法诱导肿瘤内部的骨髓细胞和淋巴细胞发生变化,肿瘤相关的单核细胞/巨噬细胞表现出复杂的细胞因子驱动的表型,此外,不同的细胞因子作用于肿瘤浸润性的单核细胞,从而驱动巨噬细胞极化,即成熟的巨噬细胞在各种因素诱导下表现出表型和功能分化,相关研究结果发表在Cell期刊上。
doi:10.1038/s41586-018-0519-y
肝癌是全球癌症死亡的第二大原因。两种形式的原发性肝癌覆盖了大多数肝癌病例:大约10%~20%的患者在肝脏内产生胆管癌,即肝内胆管细胞癌(intrahepatic cholangiocellular carcinoma, ICC),大约80%~90%的肝癌病例是肝细胞癌(hepatocellular carcinoma, HCC)。特别是近年来,患有高侵袭性ICC的患者数量明显增加,尽管这两种类型的肝癌在风险因素方面存在着重叠。
在一项新的研究中,来自德国等国的研究人员完美地证实垂死的肝细胞周围的细胞环境决定着肿瘤细胞所采取的路径,相关研究结果发表在Nature期刊上。虽然早期检测和治疗方面的进展导致许多其他类型癌症的死亡率降低,但是肝癌患者的死亡率却急剧上升。特别是在西方国家越来越常见的脂肪肝如今导致许多患者具有慢性预损伤的肝脏(chronically pre-damaged liver),这是肝癌的一种风险因素。引人注目的是,具有相同易感性或肝脏损伤风险因素的患者患上ICC或HCC。
【9】Adv Sci:科学家创建新型配位响应型磁共振成像策略,实现肿瘤微环境标志物的探测
doi:10.1002/advs.201800021
肿瘤微环境与肿瘤的发生、发展、侵袭、转移等密切相关。因此,肿瘤微环境的研究目前成为肿瘤研究的一个重要研究方向,近年来吸引了来自不同学科背景的大量优秀研究人员关注。肿瘤微环境调控以及标志物探测有助于提高肿瘤治疗效率以及诊断精度,特别是采用非侵入成像手段实现活体层面上肿瘤标志物的探测有望为良恶性判断、肿瘤的分级提供重要的理论依据。但由于缺少有效的成像策略,这一方面的研究目前仍是一个难点。
近日,来自同济大学附属第十人民医院等机构的研究人员通过研究创建了一种配位响应纵向弛豫调节策略,使得利用非侵入的MRI作为一种通用的传感方法探测肿瘤微环境特异性标志物称为可能,相关研究发表在Advanced Science杂志上;利用基于Mn2+"供体"和Mn2+"受体"之间发生的依赖于协调的纵向弛豫调整(CLRT)原理,设计了MON-FA-Mn和HMSN-NH2-Mn两个量身定制的模型系统,成功地用于恶性肿瘤生物靶标的特异性检测。
【10】APL Bioengine:电离辐射或能软化肿瘤细胞微环境 有望成功治疗多种类型癌症
doi:10.1063/1.5018327
近乎一半的癌症患者都接受过放射疗法来抑制恶性癌细胞的生长,但很少有人知道电离辐射到底是如何影响细胞外基质(ECM)的,细胞外基质是围绕在细胞周围的蛋白质和其它生物分子的混合物,其在细胞的形状、运动及信号传输功能上扮演着关键的角色,近日一项刊登在国际杂志APL Bioengineering上的研究报告中,来自范德堡大学的研究人员通过研究阐明了电离辐射改变肿瘤微环境中机械特性的分子机制。
研究者表示,电离辐射能降低肿瘤细胞外基质及胶原纤维混合物的硬度,这就提示,科学家们或能利用电离辐射来开发具有特殊性质的基质,从而使得放射疗法在干扰癌细胞DNA的同时还会给患者带来其它有益效应。研究者Cynthia Reinhart-King说道,我们都想知道肿瘤细胞周围组织的放疗效应是如何产生的,尤其是放疗如何改变肿瘤细胞基质的硬度,在肿瘤生长期间组织硬度的改变非常明显。(生物谷Bioon.com)
生物谷更多精彩盘点!敬请期待!
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。