免疫“双子星”获国家药品监督管理局批准用于恶性胸膜间皮瘤一线治疗
2021年6月11日,百时美施贵宝宣布,纳武利尤单抗注射液联合伊匹木单抗注射液获中国国家药品监督管理局批准用于不可手术切除的、初治的非上皮样恶性胸膜间皮瘤成人患者。这是双免疫联合治疗在国内获批的第一个适应证,标志着全球首个CTLA-4抑制剂伊匹木单抗注射液正式登陆中国。
华领医药新型降糖药dorzagliatin(多扎格列艾汀)上市申请获国家药监局受理!
dorzagliatin是全球首个提交新药上市申请的葡萄糖激酶激活剂类(GKA)类降糖药,有望成为在中国首先上市的全球首创新药(FIC)。
华领医药糖尿病首创新药多扎格列艾汀NDA获NMPA受理! 为全球首个葡萄糖激酶激活剂
华领医药(「公司」,香港联交所股份代号:2552.HK)今天宣布,糖尿病首创新药多扎格列艾汀(dorzagliatin)递交的NDA申请已获国家药品监督管理局(NMPA)新药审评中心(CDE)受理。多扎格列艾汀成为全球范围内首个提交新药上市申请的葡萄糖激酶激活剂类(GKA)糖尿病治疗药物,并有望成为在中国首先上市的全球首创新药(FIC)。独创“修复传感,重塑
复星医药提交帕金森病新药奥匹卡朋上市申请
3月10日,国家局官网显示,复星医药提交的帕金森病新药奥匹卡朋胶囊的上市申请正式获CDE受理。奥匹卡朋 (opicapone) 为新一代外周儿茶酚O-甲基转移酶 (COMT) 抑制剂, 由葡萄牙Bial-Portela公司开发, 于2016年6月首次获欧盟批准,作为左旋多巴/多巴脱羧酶抑制剂(DDCI,如卡比多巴)的辅助疗法,以治疗出
复星医药子公司YP01001胶囊获批开展针对晚期实体瘤的临床试验
3月17日,复星医药发布公告称,近日,其控股子公司重庆药友制药有限责任公司(以下简称“重庆药友”)收到国家药监局关于同意YP01001胶囊用于晚期实体瘤治疗开展临床试验的批准。重庆药友拟于近期条件具备后于中国境内(不包括港澳台地区,下同)开展该新药的I期临床试验。YP01001胶囊为创新型小分子化学药物,拟用于治疗晚期实体瘤;YP01
脱发“星人”感动哭!礼来JAK抑制剂在3期临床中成功促进头发再生
礼来公司和 Incyte宣布,由双方共同开发的JAK抑制剂OLUMIANT (Baricitinib)片剂治疗成人重度斑秃(AA)的3期临床试验达到主要终点。在脱发量≥50%的AA患者中,2-mg和4-mg剂量的Baricitinib在治疗的第36周均能显着改善患者头发再生情况。这是首个在AA患者的3期临床试验中被证明有效的JAK抑制
Front Neurosci:星型脑细胞与口吃有关
加利福尼亚大学河滨分校领导的一项研究发现,星形胶质细胞,这种存在与大脑中并且活跃参与大脑功能的星形细胞,可能在口吃中起重要作用。
“领雁金奖”获得者章张:建立生物大数据中心
2018年7月,炎夏初至,蝉鸣骤起,牛广艺完成了她在《Nucleic Acids Research》杂志的投稿。同年,牛广艺所在的中国科学院北京基因组研究所共在该杂志发表7篇重要研究成果,在这张优异的成绩单中,有4篇是在牛广艺师从的章张老师带领下完成的。章张,曾在美国耶鲁大学从事博士后研究、在沙特阿卜杜拉国王科技大学担任研究科学家,是首位入选国际生物审编学会
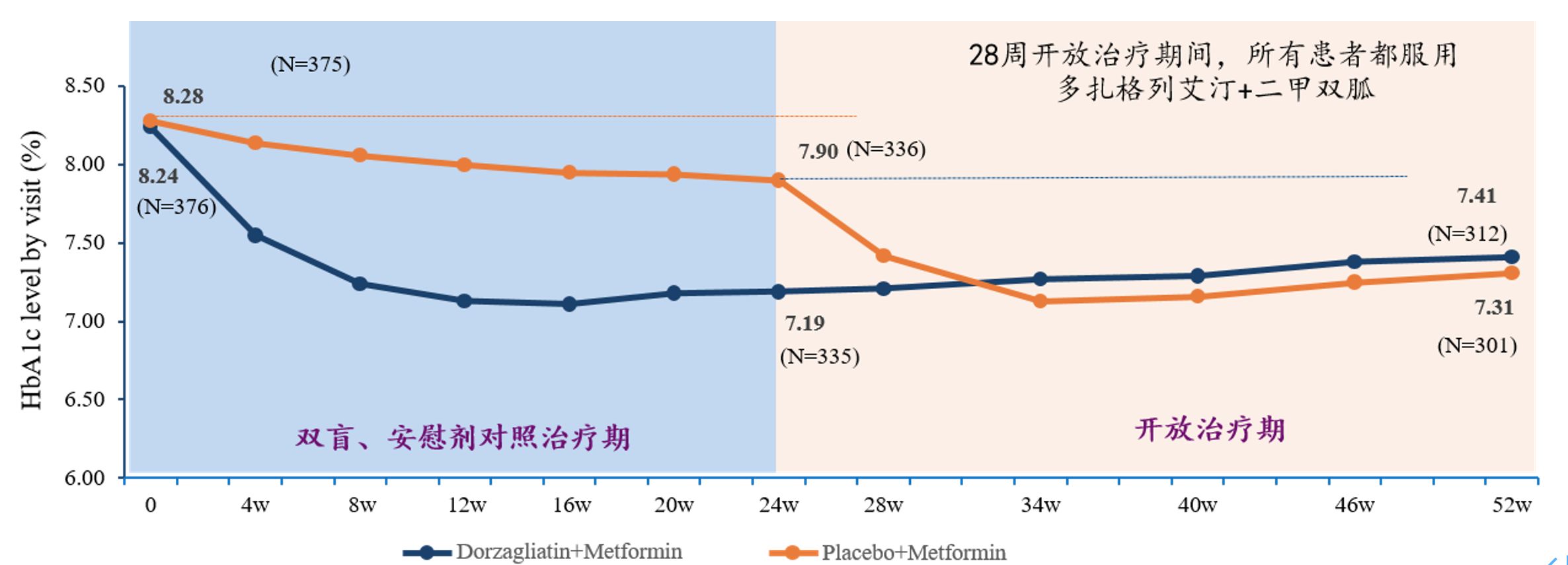
华领医药成功完成III期注册临床研究 公布多扎格列艾汀与二甲双胍联合用药临床试验DAWN研究(HMM0302)的52周结果
2020年12月18日,中国,上海 华领医药(「公司」,香港联交所股份代号:2552.HK)今天宣布其第二项III期注册临床研究DAWN(黎明研究,也称HMM0302)28周安全评估阶段的核心结果。 ü 在超过1200例中国患者中,成功完成两项53周III期注册临床研究。在新冠疫情全球大流行情况下,DAW