强生四合一HIV新药Symtuza在美国批准上市,集三大特性于一体的单一片剂
2018年7月18日讯 /生物谷BIOON/ --美国医药巨头强生(JNJ)近日宣布,四合一HIV新药Symtuza(D/C/F/TAF,800mg/150mg/200mg/10mg)已获美国食品和药物管理局(FDA)批准,作为一种完整治疗方案,用于既往未接受治疗(初治)以及某些已实现病毒学抑制的HIV-1成人感染者。Symtuza是一种新的基于darunavir的每日一次单一片剂方案(STR),
EJMC:科学家利用枸杞果开发出了一种能有效治疗血吸虫病和肝片吸虫病的新型药物
2018年7月8日 讯 /生物谷BIOON/ --近日,一项刊登在国际杂志European Journal of Medicinal Chemistry上的研究报告中,来自卡迪夫大学和阿伯里斯特维斯大学的研究人员通过研究发现,源于植物中的一种新型药物或能有效治疗两种威胁人类生命的热带疾病。文章中,研究者利用枸杞果开发了一种新型的药物化合物,其能够有效抵御诱发血吸虫病和肝片吸虫病的寄生虫。图片来源:
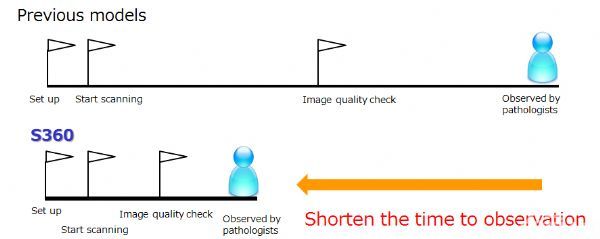
数字病理技术又一次突破边界 82片/小时!
数字病理是一项针对于病理切片数字化的新兴技术。在医院的诊断、数据储存和共享、科研、会议、教学,以及第三方诊断机构的病理会诊中逐渐崭露头角,潜力巨大。就中国来讲,数字病理进入的十年余年中,引入数字病理的医疗机构也从几乎为零,到了现在的600-800家。滨松数字病理技术于2006年进入中国,首台在国内投入使用的NanoZoomer数字病理切片扫描仪已经在北京协和医院持续稳定地工
海思科帕金森药物盐酸普拉克索缓释片获受理
5月7日海思科医药集团股份有限公司(简称“海思科”)公告称,其全资子公司四川海思科制药有限公司于近日收到国家食品药品监督管理总局下发的《受理通知书》(受理号:CYHS1800082国、CYHS1800083国),盐酸普拉克索缓释片申报材料符合《中华人民共和国行政许可法》第三十二条的规定,予以受理。基本情况如下:帕金森(PD)是一种临床常见的慢性进行性神经系统疾病,多发于中老年人。PD的
华海药业坎地沙坦酯氢氯噻嗪片获得美国FDA批准文号
今天,浙江华海药业股份有限公司(以下简称“华海药业”)发布公告称,近日,收到美国食品药品监督管理局(以下简称“美国 FDA”)的通知,公司向美国FDA申报的坎地沙坦酯氢氯噻嗪片的新药简略申请已获得批准,意味着华海药业可以生产并在美国市场销售该产品。药品的基本情况药物名称:坎地沙坦酯氢氯噻嗪片ANDA 号:207455剂型:片剂规格:16mg/12.5mg、32mg/12.5mg、32mg/25mg
人福医药氨酚氢可酮片获美国FDA批准文号
近日,人福医药集团股份公司(简称“人福医药”)全资子公司Epic Pharma, LLC收到美国食品药品监督管理局关于氨酚氢可酮片的批准文号。药品名称:Hydrocodone Bitartrate and Acetaminophen Tablet(氨酚氢可酮片)申请事项:ANDA(美国新药简略申请,即美国仿制药申请。ANDA获得美国FDA 审评批准意味着申请者可以生产并在美国市场销售该产品。)AN
石墨烯基纳米复合材料的合成与抗菌性能研究获得进展
虽然当今已步入医疗技术高度发达、健康促进行业多元发展的时代,但是病原菌感染仍然是人类面临的重要健康威胁之一,每年导致数以百万计的感染患者出现。近年来,抗生素的不合理应用已引起严重的细菌耐药问题,日益增多的耐药菌致使抗生素疗效不断下降,尤其是“超级细菌”的出现更使临床治疗几乎陷入了无药可用的境地。此外,由于新药研发滞后同时缺乏理想的抗生素替代疗法,细菌耐药迫使抗生素用量持续攀升,然而抗生素的过量使用
艾伯维维建乐®(奥比帕利片)联合易奇瑞®(达塞布韦钠片)丙肝治疗方案8周新疗程在华获批
- 维建乐®联合易奇瑞®用于治疗基因1b型、初治、轻度至中度肝纤维化(F0-F2)慢性丙型肝炎患者,疗程可缩短至8周。- 此新疗程的获批,基于GARNET临床研究的数据。数据表明,无肝硬化(F0—F2)的初治基因1b型慢性丙型肝患者在接受为期8周的维建乐®联合易奇瑞®方案治疗后,持续病毒学应答率(SVR12)为99% (n=14
总局发布关于修订甲巯咪唑片说明书的公告
根据药品不良反应评估结果,为进一步保障公众用药安全,国家食品药品监督管理总局决定对甲巯咪唑片说明书【不良反应】、【禁忌】、【注意事项】、【孕妇及哺乳期妇女用药】等项进行修订。现将有关事项公告如下:一、所有甲巯咪唑片生产企业均应依据《药品注册管理办法》等有关规定,按照甲巯咪唑片说明书修订要求(见附件),提出修订说明书的补充申请,于2018年4月15日前报省级食品药品监管部门备案。修订内容
总局发文修订海珠喘息定片说明书
食品药品监管总局发布公告,决定对海珠喘息定片说明书增加警示语,并对【不良反应】【禁忌】【注意事项】和特殊人群用药等项进行修订。有关事项公告如下:一、所有海珠喘息定片生产企业均应依据《药品注册管理办法》等有关规定,按照海珠喘息定片说明书修订要求(见附件),提出修订说明书的补充申请,于2018年3月25日前报省级食品药品监管部门备案。修订内容涉及药品标签的,应当一并进行修订;说明书及标签其他内容应当与