我国首个原创型基因治疗载体问世,打通基因编辑体内治疗的最后一公里
上海交通大学系统生物医学研究院的蔡宇伽团队在《自然-生物医学工程》(Nature Biomedical Engineering)杂志上发表了一篇题为:Lentiviral delivery of co-packaged Cas9 mRNA and a Vegfa-targeting guide RNA prevents wet age
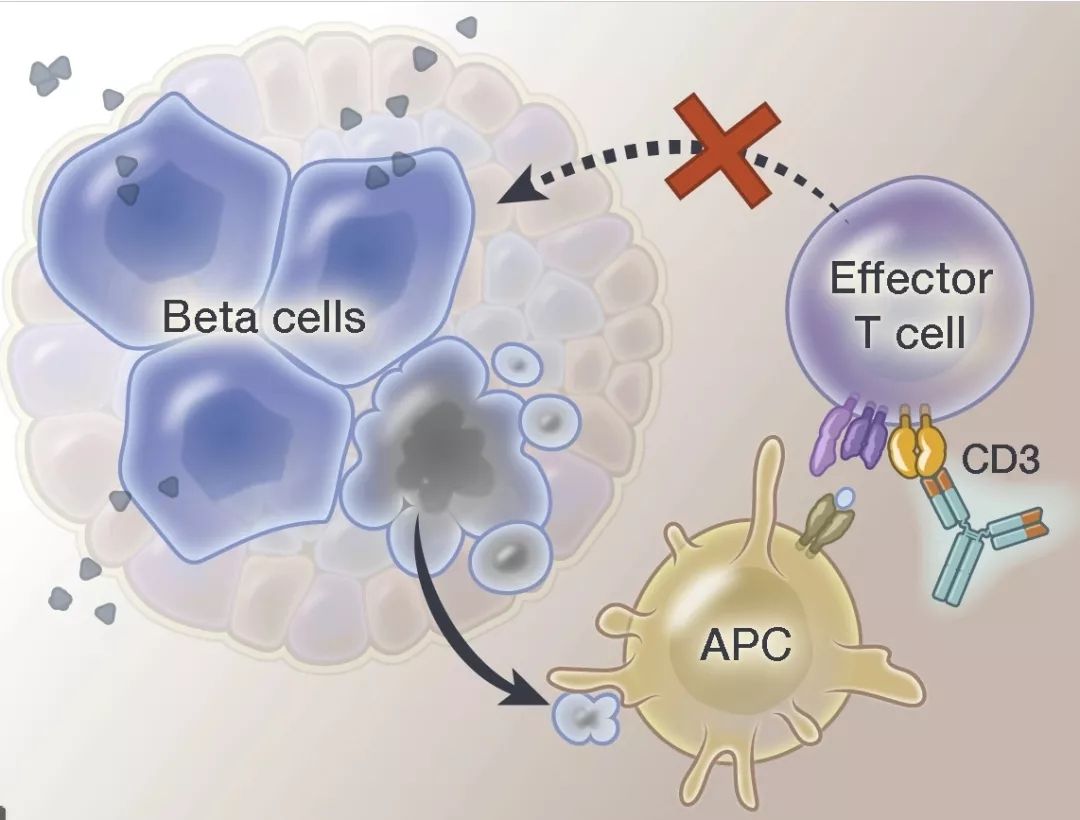
治疗14天,1型糖尿病风险降低59%!突破性疗法teplizumab获FDA优先审评资格
1月4日,Provention Bio公司宣布已向FDA递交CD3单克隆抗体teplizumab的生物制品许可申请(BLA),用于延迟或预防高危患者的临床1型糖尿病(T1D)。FDA已授予teplizumab上市申请优先审评资格,PDUFA预定审批期限为2021年7月2日。被授予优先审评的药物意味着其在治疗、诊断或预防严重疾病安全性或有效性方面与
B型血友病基因疗法!uniQure公司AMT-061关键3期成功:一次治疗,FIX替代疗法年使用量减少97%!
AMT-061是一款基于腺相关病毒5(AAV-5)的一次性基因疗法。
天士力治疗2型糖尿病化学1类新药获批临床试验
天士力发布公告称,其子公司江苏帝益近日收到国家药监局核准签发用于治疗2型糖尿病的化学1类新药TSL-1806胶囊《药物临床试验批准通知书》,并将于近期开展临床试验。药品名称:TSL-1806剂型:胶囊规格:100 mg申请人:江苏天士力帝益药业有限公司受理号:CXHL2000413通知书编号:2020LP00664注册分类:化药1类审批结论:根据
1型糖尿病重磅!预防性免疫治疗单抗teplizumab将2021年上市:疾病风险降低50%,发病推迟≥2年
teplizumab将成为第一种可预防/延缓高危人群发展为临床1型糖尿病(T1D)的疗法。
基因疗法PBGM01获EMA孤儿药认定 用于治疗GM1神经节苷脂贮积症
专注于开发罕见单基因中枢神经系统疾病转化疗法的Passage Bio公司(NASDAQ: PASG) 于26号宣布,欧盟委员会(EC)已授予该公司用于治疗GM1神经节苷脂贮积症(GM1)的先导基因治疗候选药物PBGM01孤儿药称号。PBGM01是一种腺相关病毒载体(AAV)基因递送疗法,用于治疗婴儿GM1。PBGM01将编码β-gal的功能性GL