科学家揭示了PPD是一种靶向CMA抑制剂,是非小细胞肺癌治疗的好策略
来源:生物谷原创 2023-06-20 11:44
自噬是细胞中的一种“自噬”现象,自噬小体包裹错误折叠的蛋白质或受损的细胞器,随后与溶酶体融合形成自溶酶体。被包裹的内容物被自溶酶体降解,以实现细胞内环境的稳定和细胞器的更新。
自噬是细胞中的一种“自噬”现象,自噬小体包裹错误折叠的蛋白质或受损的细胞器,随后与溶酶体融合形成自溶酶体。被包裹的内容物被自溶酶体降解,以实现细胞内环境的稳定和细胞器的更新。根据自噬的发生过程,自噬可分为巨型自噬、伴侣介导型自噬和微型自噬。
其中,CMA是一种选择性的以Lys-Phe-Glu-Arg-Gln(KFERQ)样五肽基序为靶向的蛋白质降解自噬。KFERQ类基序要么存在于初级氨基酸序列中,要么通过翻译后修饰产生,如磷酸化或乙酰化。
胞内伴侣热休克同源蛋白70(HSC70)可以识别含有KFERQ样基序的底物蛋白,随后底物-伴侣复合体通过与溶酶体膜蛋白2A型(LAMP2A)结合转移到溶酶体膜上,并驱动LAMP2A型多聚体形成易位复合体,底物通过该复合体进入溶酶体进行降解。

图片来源:https://pubmed.ncbi.nlm.nih.gov/37311689/
近日,来自中国药科大学的研究者们在Br J Pharmacol杂志上发表了题为“Discovery of a potent inhibitor of chaperone-mediated autophagy that targets the HSC70-LAMP2A interaction in non-small cell lung cancer therapy”的文章,该研究揭示了PPD是一种靶向CMA抑制剂,可以阻断HSC70LAMP2A相互作用和LAMP2A同源多聚化。抑制CMA而不增加巨噬细胞自噬的调节补偿是非小细胞肺癌治疗的好策略。
伴侣介导的自噬(CMA)是一种选择性的针对蛋白质降解的自噬,在多种恶性肿瘤中保持高活性。抑制HSC70和LAMP2A的结合可以有效地阻断CMA。目前,抑制CMA的最具特异性的方法仍然是下调LAMP2A,目前还没有发现抑制CMA的化学抑制剂。
用酪胺信号放大(TSA)双免疫荧光法检测NSCLC组织中CMA的表达水平。根据CMA活性进行高含量筛选,以确定潜在的CMA抑制剂。通过药物亲和反应靶标稳定性-质谱法(DARTS-MS)确定了该抑制剂的靶点,并用蛋白质质谱仪进行了验证。通过对CMA的抑制和激活来阐明CMA抑制剂的分子机制。
研究者发现,抑制HSC70和LAMP2A之间的相互作用可以阻断非小细胞肺癌中的CMA,并抑制肿瘤的生长。PPD通过干扰HSC70-LAMP2A相互作用首次被确定为CMA的靶向小分子抑制剂。
PPD的结合位点分别位于HSC70的核苷酸结合区E129和LAMP2A的C末端T278。PPD通过抑制HSC70-LAMP2a-eIF2α信号轴,加速蛋白质合成,诱导ROS积累。此外,PPD还通过阻断STX17-SNAP29-VAMP8信号轴,阻止了CMA抑制引起的巨噬细胞自噬的调节补偿。
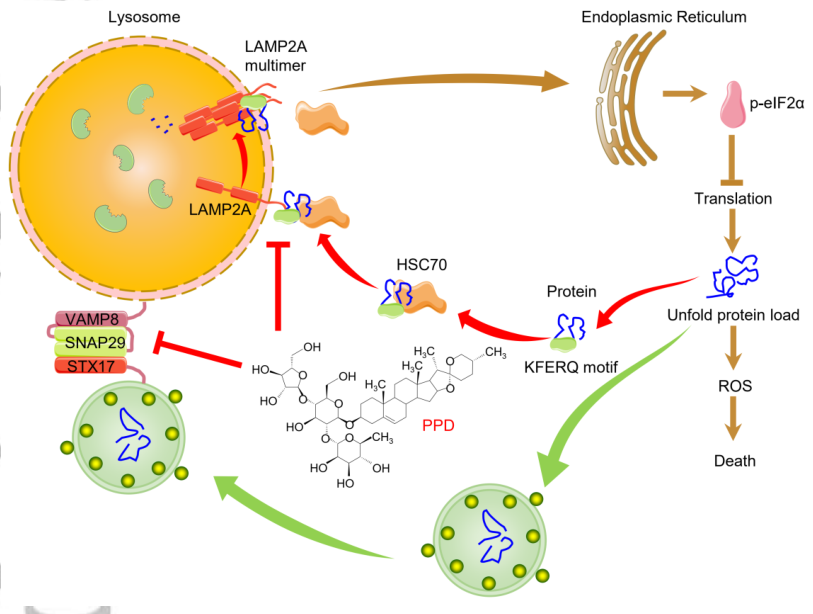
图片来源:https://pubmed.ncbi.nlm.nih.gov/37311689/
PPD阻断非小细胞肺癌CMA的作用机制
综上所述,研究者首次报道PPD是非小细胞肺癌中CMA的靶向抑制剂。更重要的是,本研究为开发CMA抑制剂提供了新的策略。靶向抑制HSC70-LAMP2A相互作用或LAMP2A同源多聚化对非小细胞肺癌的治疗具有很强的疗效。(生物谷 Bioon.com)
参考文献
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


