Cell重磅:华人团队首次从iPSC构建出高度血管化的肺和肠道类器官,一作已回国加入中科院
来源:生物世界 2025-07-08 13:34
在这项最新研究中,研究团队利用发育原理建立了一个体外血管化类器官平台,该平台真实地再现了中胚层和内胚层谱系的协同发育,该方法可实现内胚层衍生物与器官型内皮/间充质细胞群的高效分化与谱系特化。
2009 年,荷兰 Hubrecht 研究所的 Hans Clevers 等人使用来自小鼠肠道的成体干细胞培育出首个肠道类器官,开创了类器官研究时代。此后,类器官领域研究成果不断,许多新型类器官和更复杂的类器官不断涌现,这些研究新药开发、精准治疗、再生医学等领域带来了更强大的工具。
然而,目前的类器官中普遍缺乏器官特异性和功能性的血管网络,尤其是肺和肠道等内胚层器官,缺乏有效的血管化方法,导致肺和肠道类器官结构和功能的不成熟,极大地限制了它们在疾病建模和治疗应用方面的应用。
2025 年 6 月 30 日,辛辛那提儿童医院/加州大学洛杉矶分校顾名夏团队和辛辛那提儿童医院郭敏哲团队合作,在国际顶尖学术期刊 Cell 上发表了题为:Co-development of Mesoderm and Endoderm Enables Organotypic Vascularization in Lung and Gut Organoids 的研究论文。
该研究首次通过人类诱导多能干细胞(iPSC)成功构建了高度血管化的肺类器官和肠道类器官。这些类器官模型不仅模拟了人类胚胎早期多胚层协同发育的复杂过程,更突破了传统类器官缺乏功能性血管和器官特异性间充质的瓶颈,为研究人类器官发育和疾病中的复杂细胞间通讯以及再生医学提供了一个先进的平台。
论文第一作者兼共同通讯作者苗一非博士,现为中国科学院动物研究所人类器官生理病理模拟装置(HOPE)研究员;共同第一作者谈诚博士现为北京大学人民医院妇产科主治医师。


论文第一作者苗一非
苗一非博士,2012 年毕业于北京大学医学部基础医学八年制专业,获病理生理学博士学位。之后于美国休斯顿大学、加州大学圣地亚哥分校、希望之城医学中心从事博士后研究。2018年先后加入斯坦福大学和辛辛那提儿童医院,以讲师、助理教授身份进行干细胞以及类器官研究工作。2025 年 1 月,全职加入中国科学院动物研究所,参与人类器官生理病理模拟装置(HOPE)建设,主要研究方向为利用胚胎干细胞和诱导多能干细胞分化的多种细胞和类器官模型,进行血管以及心肺系统的生理病生理体外模拟和疾病机制的探索。
人体的血管系统(尤其是毛细血管床)在不同器官中表现出显著的特化,以满足局部生理需求。这种功能特化在转录组水平上也很明显,正如最近的人类胎儿和成人细胞图谱所展示的那样,在这些图谱中,来自不同器官系统的内皮细胞(EC)形成单独的细胞簇,突显了独特的基因特征。
已有研究表明,每个器官内独特的微环境在驱动器官特异性血管内皮细胞和间充质发育方面发挥着关键作用。然而,在人类发育过程中器官血管化这一复杂且高度互动的过程在空间和时间上的动态变化仍知之甚少。要解决这一知识空白,就需要体外平台不仅包含相关的细胞谱系,还要整合具有精准细胞构型的器官型血管系统。
类器官(Organoid)是一种三维(3D)组织结构,能够模拟器官的细胞组成和功能,营造出适合研究人类发育和疾病(尤其是器官特异性血管发育)的微环境。
已有多个研究团队专注于涉及多种细胞类型在各自分化后融合的类器官组装方法。例如,之前有研究尝试通过引入诸如人脐静脉内皮细胞(HUVEC)等原代内皮细胞来使肝脏类器官和大脑类器官血管化。然而,这种方法导致内皮细胞缺乏明确的器官特异性和结构,从而限制了类器官的形态形成和功能成熟。这些组装方法无法准确地体现血管细胞在体内器官发生过程中的发育情况。
相比之下,在早期发育过程中,由形态发生模式信号引导的多个胚层之间的协调相互作用,对于器官特异性内皮细胞和间充质细胞的特化和分化至关重要。因此,重现这些复杂的发育相互作用,对于建立类器官的生理相关血管化至关重要。
然而,源自非中胚层谱系(例如外胚层和内胚层)的类器官的血管化一直特别具有挑战性。这是因为将人类诱导多能干细胞(iPSC)分化为中胚层谱系与非中胚层谱系需要不同的(有时甚至是相互对立的)信号通路。因此,研究人员们为诸如肠道类器官和肺类器官等内胚层类器官的血管化所做的努力,仍未取得实质性突破。
为解决这一问题,之前的研究尝试通过引入诸如骨形态发生蛋白-4(BMP4)、血管内皮生长因子 A(VEGFA)、成纤维细胞生长因子(FGF)或表皮调节素(EREG)等促血管生成因子,来扩增在内胚层分化过程中偶然出现的少量内源性内皮祖细胞,从而生成血管化的肠道类器官。尽管这些方法培养出的内皮细胞部分反映了人类胎儿小肠内皮细胞的基因特征,但由此生成的血管在数量上仍然有限,结构和功能也都不成熟,而且常常缺乏器官特异性特征和完整的功能。更重要的是,现有的肺类器官生成方法尚未成功重现人类肺泡毛细血管界面,而这一结构对于气体交换至关重要。这些限制也是意料之中的,因为大多数从诱导多能干细胞(iPSC)分化出前肠和肺类器官的方案都依赖于强烈抑制骨形态发生蛋白(BMP)和转化生长因子-β(TGF-β)信号通路。虽然这些条件对内胚层模式形成有效,但与血管和间充质谱系的特化不相容。因此,肠道类器官和肺类器官中缺乏健全的血管化,极大地限制了它们在疾病建模和治疗应用方面的生理相关性。
在这项最新研究中,研究团队利用发育原理建立了一个体外血管化类器官平台,该平台真实地再现了中胚层和内胚层谱系的协同发育,该方法可实现内胚层衍生物与器官型内皮/间充质细胞群的高效分化与谱系特化。
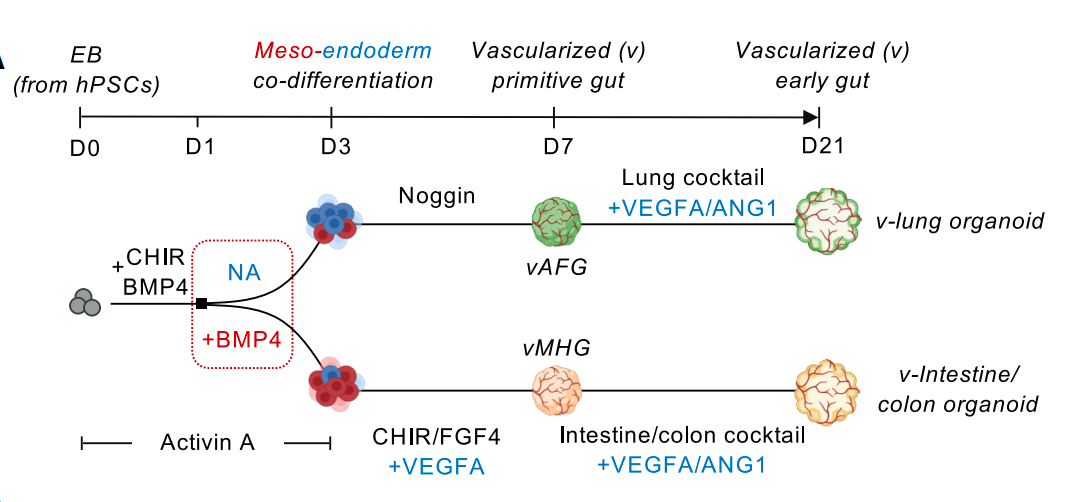
传统构建方法通常需要添加十余种因子,而在该方法中,培育肺类器官仅需 1 种抑制剂——Noggin,培育肠道类器官仅需 3 种激活剂——CHIR99021、FGF4 和 VEGFA。3D培养球内细胞会自发分泌血管生长必需的信号分子,从而自然形成血管网络。由此产生的血管化肺类器官和肠道类器官具有器官特异性内皮和间充质,表现出细胞类型多样性增强、三维结构、细胞存活率和成熟度提高的特点,并展现出真实生理功能——肺血管形成紧密屏障(模拟气体交换),肠道血管则呈现高渗透性(利于营养吸收),移植到小鼠体内后,类器官血管与宿主循环系统结合,同时保持了器官特异性,进一步促进了类器官成熟,成功实现了血液灌注,这标志着类器官血管首次具备了体内循环能力。
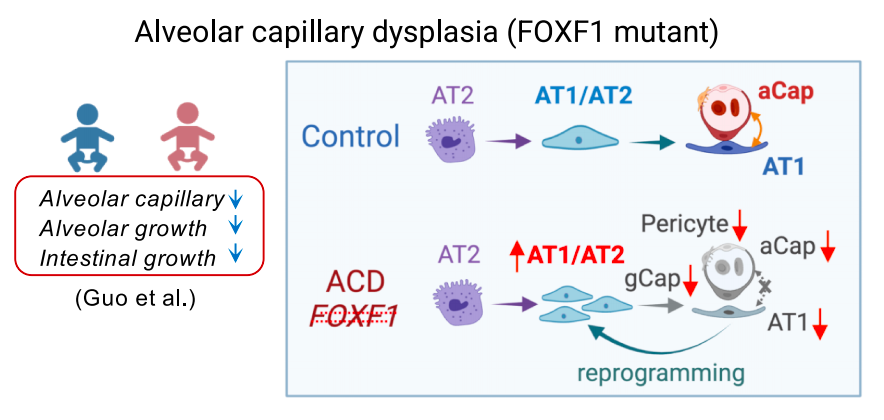
这种多谱系类器官系统可用于研究不同疾病背景下异常的细胞间相互作用。肺泡毛细血管发育不良伴肺静脉错位(ACDMPV)是一种先天性肺部疾病,由中胚层 FOXF1 基因突变引起。然而,传统的肺上皮类器官缺乏表达 FOXF1 的间充质细胞和内皮细胞,这限制了这些模型模拟这种肺部疾病的能力。研究团队通过将携带 FOXF1 基因突变的患者来源的 iPSC 分化为血管化的肺类器官,能够重现该疾病中由内皮-上皮相互作用中断所导致的原发性内皮缺陷以及继发性上皮异常。同步构建的肠类器官更重现患者伴发的肠旋转不良,首次实现同一平台模拟多器官互作疾病,这为传统模型无法破解的复杂病症带来曙光。
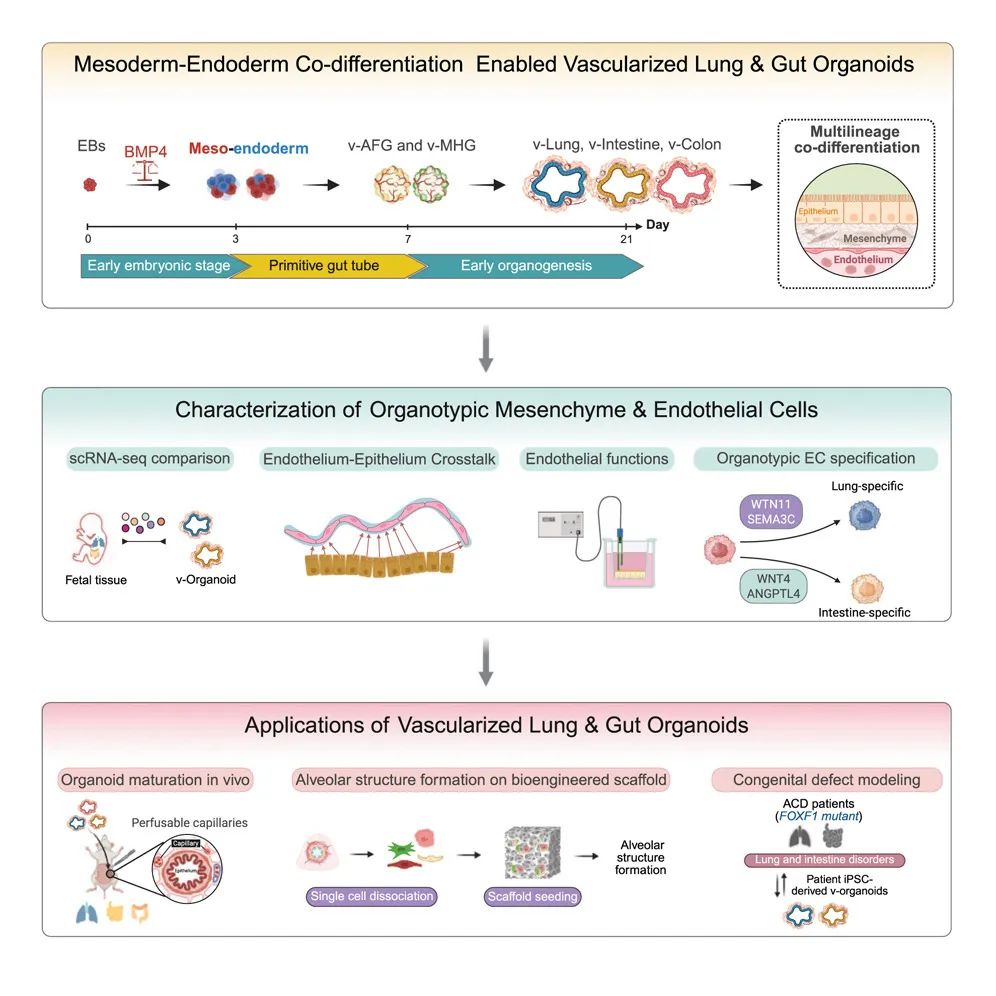
该研究的亮点:
BMP 介导的中胚层-内胚层共分化对于器官特异性血管系统至关重要;
器官特异性血管系统支持内胚层类器官的发育和成熟;
血管化类器官具有人类胎儿肺和肠的特征;
血管化类器官模型模拟了 FOXF1 疾病中异常的内皮-上皮细胞间相互作用。
论文链接:
https://www.cell.com/cell/abstract/S0092-8674(25)00628-2
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。



