肺癌免疫新辅助治疗收获**重要成果,早期肺癌向治愈又迈出重要一步
来源:奇点糕 2022-04-10 12:52
如果说内科医生的理想是药到病除,那“刀到病除”就是外科医生永远的目标,不过要实现这个目标,单靠手术刀是不够的,所以才需要“以手术为中心的综合治疗”。
如果说内科医生的理想是药到病除,那“刀到病除”就是外科医生永远的目标,不过要实现这个目标,单靠手术刀是不够的,所以才需要“以手术为中心的综合治疗”。
以有力的系统性治疗方案辅助手术治疗,在手术前或手术后对癌症展开打击,是临床上常用的策略,但既往的新辅助或辅助化疗有着明显的局限性。变革了晚期肺癌诊疗格局的免疫治疗,下一个进军的战场正是这里。
近期,非小细胞肺癌(NSCLC)免疫新辅助治疗的代表性临床研究——CheckMate-816再传捷报,成功达到第二个主要终点:在化疗的基础上加用PD-1抑制剂纳武利尤单抗,能将患者的中位无事件生存期(EFS)延长50%,美国FDA也正式批准了纳武利尤单抗新辅助治疗的适应证!
免疫治疗,它又赢了!
在既往化疗缩瘤降期、降低手术难度的基础上,免疫新辅助治疗有望清除微转移灶,成功延长中位EFS,接下来还可能实现总生存期(OS)获益的终极目标,这种全方位的治疗获益,足以变革早期肺癌的治疗。
而也许只有外科医生们才最清楚,这样不断升级的成功有多重要。那么免疫新辅助治疗,又为何如此优秀呢?
新辅助化疗,“想说爱你不容易”
面对凶残又狡猾的NSCLC,只靠手术刀实现刀到病除实在不易。即使进入21世纪,围手术期化疗尤其是辅助化疗得到普遍应用,可手术的早期NSCLC患者术后仍有复发或远处转移风险,且超过50%的复发/转移发生在术后2年内,这显然不利于患者的长期生存[1-3]。
导致复发和远处转移的元凶,往往是癌症的“微转移灶”(Micrometastases),即随着循环系统潜藏到淋巴结、骨髓等处的一小撮癌细胞。它们无法被肉眼察觉,手术刀也对它们无可奈何,而且它们还可能通过“休眠”,躲避免疫系统和辅助治疗的追杀。
这些难以发现、更难以消灭的微转移灶,就给癌症的卷土重来埋下了伏笔,一些转入休眠的癌细胞,可能因为内外环境的改变,突然“从睡梦中醒来”,从而导致患者的术后复发风险呈现出“双高峰”的状态[4-5]。
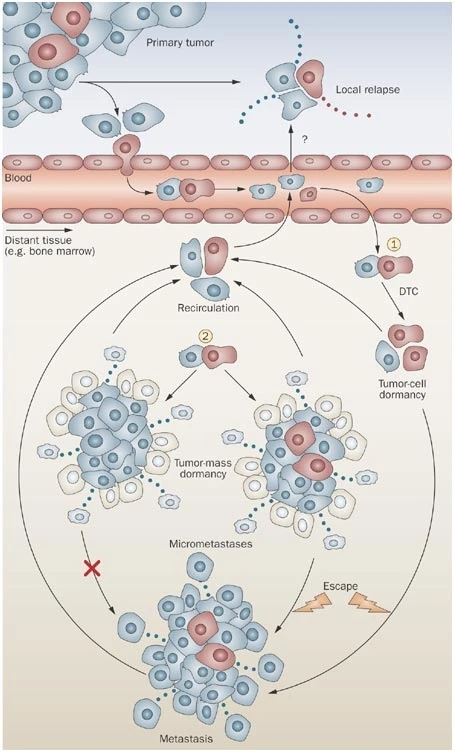
癌症微转移的前因后果
(图片来源:Nature Reviews Clinical Oncology)
现有的围手术期新辅助/辅助治疗,就将清除微转移灶作为治疗目标的一部分,然而无论新辅助或辅助化疗的表现都不算优秀。2010、2014年相继发表在《柳叶刀》的两项权威Meta分析显示,辅助化疗仅能将NSCLC患者的5年生存率提高约4%,新辅助化疗也只能将5年生存率提高5%[6-7]。
改善5年生存率效果有限,意味着新辅助化疗在疗效上还有很大的提升空间。而且传统化疗的副作用,也可能导致手术延迟,部分患者甚至因化疗期间病情进展无法手术,这些同样是临床上需要权衡的因素。
因此在既往的国内外权威指南和共识中,新辅助化疗的使用基本都局限于IIIA期患者,很多外科医生只把新辅助治疗视为术前缩瘤降期、便于手术切除的一种手段,认为它改善长期预后的价值有限。
不过进入免疫治疗时代后,NSCLC的新辅助/辅助治疗也迎来了转机,真正走上了发展的快车道。
“众望所归”,免疫新辅助治疗一路飞驰
众所周知,以免疫检查点抑制剂为代表的免疫治疗,通过激活机体免疫应答来抗击癌症,作用机制与放疗、化疗等传统治疗手段并不相同。正是这种不同使免疫治疗脱颖而出,也正是这种不同,使它被视为NSCLC新辅助治疗的“破壁人”。
在多种PD-1/L1抑制剂取得关键临床研究成功,全面改写晚期NSCLC的治疗格局后,学界的探索方向很快转向了早期NSCLC的免疫治疗。一系列临床前研究从不同的角度,为免疫新辅助治疗的作用机制和优势提供了理论依据。
现有研究提出了免疫新辅助治疗的几大优势,例如术前肿瘤仍然完整,因此肿瘤新抗原数量更多,免疫治疗就能充分调动肿瘤微环境内的T细胞等免疫细胞杀伤肿瘤;同时更多数量、更多亚群的T细胞也会被激活,进入外周血乃至全身各处清除微转移灶。而且术前患者免疫系统更完善,激活的免疫应答就相对更强[8]。
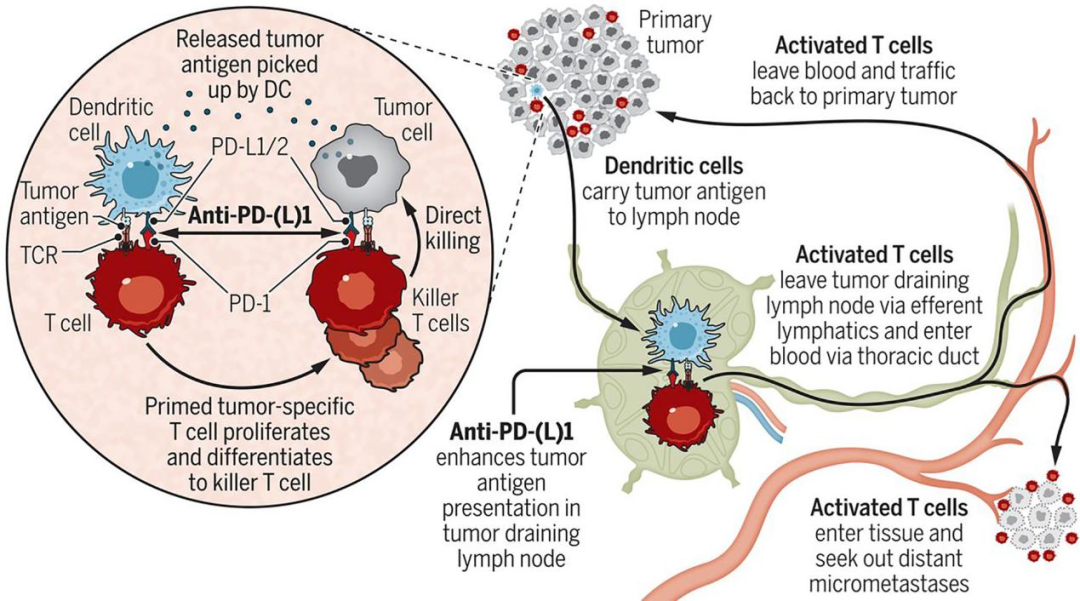
免疫新辅助治疗激活免疫应答的机制
(图片来源:Science)
2016年发表在Cancer Discovery上的一项标志性实验室研究,就专门对比了术前/术后使用免疫治疗,发现术前用药能更好地激活外周CD8+ T细胞,从而以更强的抗肿瘤免疫应答清除转移灶[9]。
而且,外科手术必然伴随着创伤、失血和麻醉,这往往会导致患者免疫系统在术后一段时间内处于抑制状态,对免疫辅助治疗可能不利[10];同时新辅助治疗的疗程一般只需3-4个周期,在依从性上可能也优于需长期用药的辅助治疗[11]。此外从外科角度出发,以有效的新辅助治疗实现缩瘤降期,也有利于手术切除。
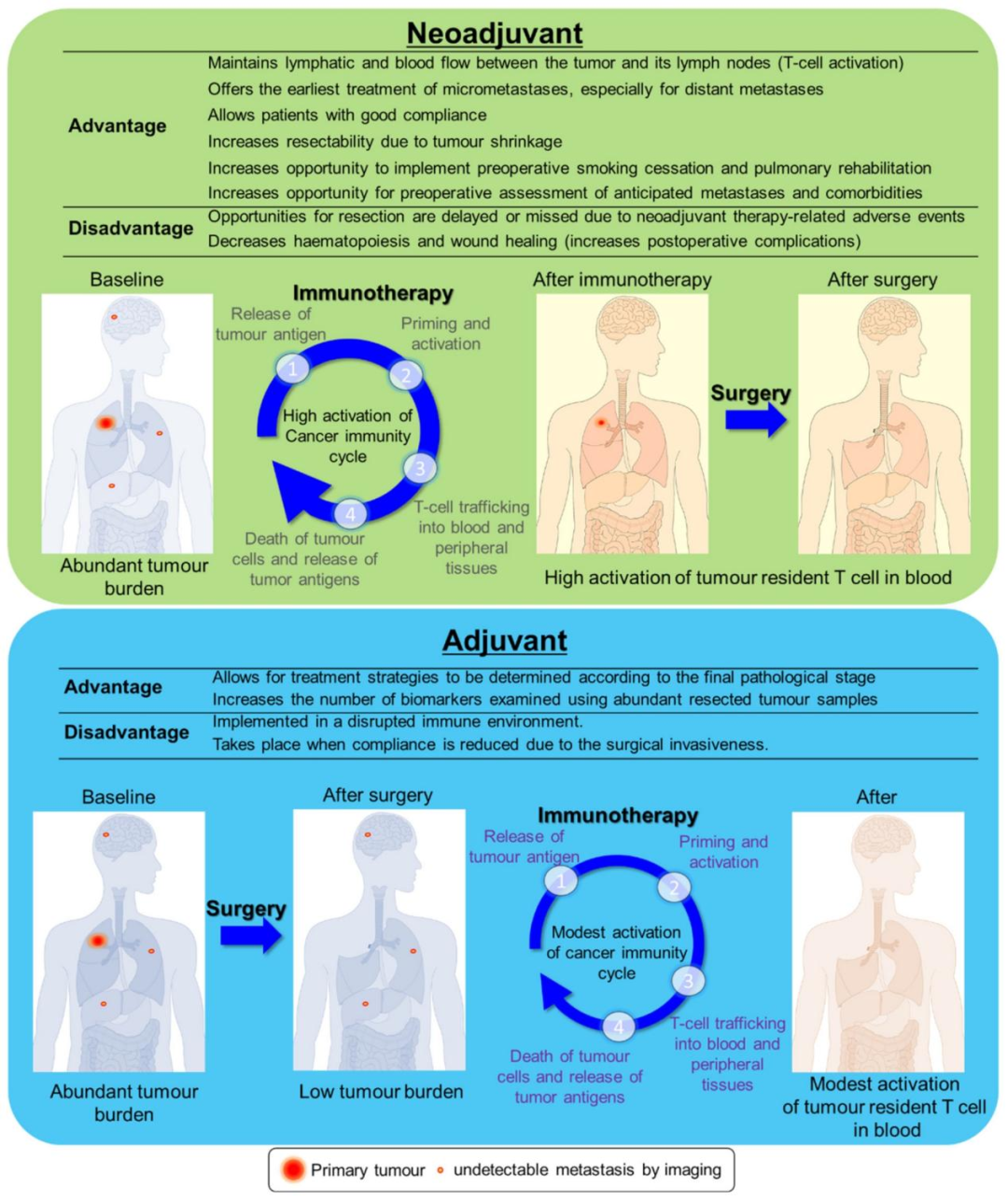
免疫新辅助治疗与辅助治疗的部分特点对比
(图片来源:Cancers)
综合考虑以上种种因素的话,免疫新辅助治疗“众望所归”,成为早期NSCLC免疫治疗的探索热点也就顺理成章了。多项采用免疫单药或免疫+化疗联合方案的临床I/II期研究,已报告了可喜的早期疗效数据。
例如多次亮相重要学术会议的临床II期NADIM研究,采用术前纳武利尤单抗+紫杉醇+卡铂治疗三个周期,接续术后纳武利尤单抗辅助用药一年的方案,治疗IIIA期NSCLC患者,初步报告的pCR率就达到63%,3年随访结果则显示,意向治疗人群(ITT)PFS和OS率分别达到69.6%和81.9%,有望实现长期生存[12-13]。
与IIIA期患者的历史生存数据相比[14-15],NADIM研究的免疫新辅助+辅助治疗全程方案,得到了堪称飞跃式提升的生存获益。不过其它早期研究大多未报告长期生存数据,免疫新辅助治疗的生存获益和对外科手术的影响,也需要通过更大样本量的随机对照临床研究再度确证。
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


