Cell:新研究发现一些snoRNA可促进蛋白分泌
来源:生物谷原创 2024-11-26 13:55
在这项新的研究中,研究人员测试了一种名为“snoKARR-seq”的新工具,它能将snoRNA与其靶标结合RNA连接起来。
DNA 和 RNA 的动态可逆修饰调节着基因的表达和转录方式,从而影响着细胞过程、疾病发展和整体机体健康。小核糖体 RNA(snoRNA)是一类常见但被忽视的引导性 RNA 分子,它们引导对细胞核糖体 RNA(rRNA)靶标进行化学修饰,就像引导员带观众到剧院的座位一样。

如今,在一项新的研究中,来自芝加哥大学的研究人员开发出一种新方法,用于识别 snoRNA 的新型细胞 RNA 靶标。他们在人体细胞和小鼠脑组织中发现了数千种以前未知的 snoRNA 靶标,其中许多靶标除了引导 rRNA 修饰外,还具有其他功能。相关研究结果于2024年11月22日在线发表在Cell期刊上,论文标题为“snoRNA-facilitated protein secretion revealed by transcriptome-wide snoRNA target identification”。
他们新发现的一些与信使核糖核酸(mRNA)的相互作用促进了蛋白分泌,这是一个重要的细胞过程,可用于潜在的治疗和生物技术应用。
论文共同通讯作者、芝加哥大学生物化学与分子生物学教授Chuan He博士说,“一旦你看到这些 snoRNA有这么多靶点,你就会意识到还有很多东西需要了解。我们已看到它们在蛋白分泌中发挥作用,这对生理学有重大影响,而且这也为研究数百种其他snoRNA指明了道路。”
用于蛋白分泌的分子胶水
人类基因组中有1000多种已知的编码snoRNA的基因,但科学家们只确定了其中约300种snoRNA的作用靶标。这些靶标大多涉及rRNA 和参与 mRNA 剪接的小核 RNA 的引导修饰。
自 snoRNA 首次被发现以来的数十年间,科学家们基本上对其余 700 种snoRNA置之不理,认为它们发挥着类似的功能。然而,与诸如microRNA之类的具有相似长度的其他引导RNA分子不同,snoRNA的长度差异很大,从50到250个碱基不等,这表明它们可以做很多不同的事情。
在过去的12年里,He实验室开发了多种生化和测序技术,用于研究转录、DNA修饰和RNA修饰。
在这项新的研究中,He与论文共同通讯作者、芝加哥大学生物化学与分子生物学教授Tao Pan博士合作,测试了一种名为“snoKARR-seq”的新工具,它能将snoRNA与其靶标结合RNA连接起来。
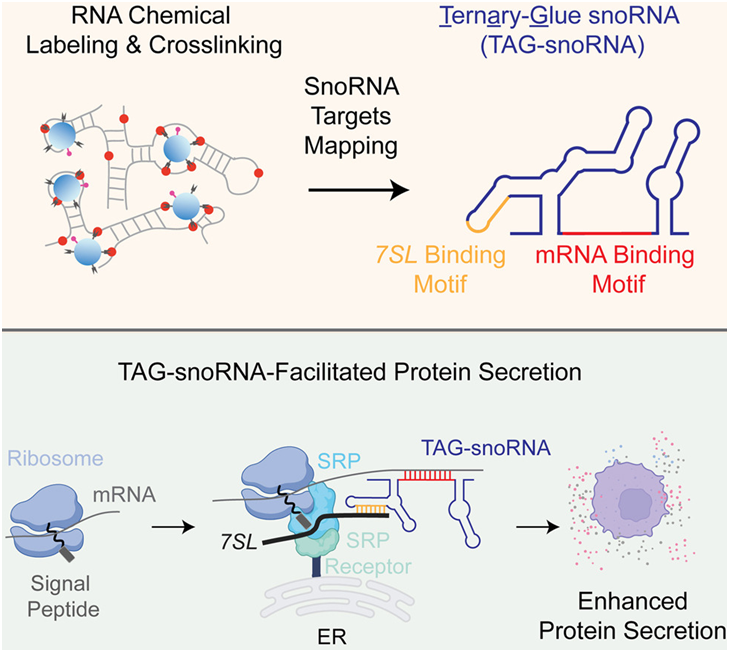
Pan说,“He实验室开发了这项杀手级技术,可以在转录组水平准确地观察每种snoRNA与哪些RNA相互作用。如今有了很大的空间,可以全面了解这1000种[编码snoRNA的]人类基因在做什么。”
这些新发现的大多数 snoRNA靶标与已知的 RNA 修饰位点并不重叠,这表明 snoRNA 在细胞中可能具有更广泛的功能。一个意外的发现是,一种名为SNORA73的snoRNA能与编码分泌蛋白和细胞膜蛋白的mRNA相互作用。
蛋白分泌是一个基本的生物过程,通过这个过程,蛋白从细胞运输到细胞外空间,这对细胞间的交流、免疫反应和消化等各种功能至关重要。作者发现SNORA73 是 mRNA 和蛋白合成机制之间的“分子胶水”,有助于促进这一过程。
对SNORA73如何与mRNA结合的进一步分析表明,可以设计合成snoRNA序列来影响蛋白分泌。作者通过调整绿色荧光蛋白(GFP)与 SNORA73 的相互作用来验证这一假设。GFP通常被引入细胞,使其在特定条件下发光,这样科学家们就能看到实验的效果。
当他们让可从细胞中分泌的工程化GFP与SNORA73基因表达时,蛋质分泌量比对照组增加了30%到50%。
这些实验表明,他们可以利用 snoRNA 机制操纵特定蛋白的分泌,这对开发治疗药物很有帮助。例如,如果人类疾病涉及分泌蛋白的缺乏,那么生物工程人员就可以劫持该系统,递送人工 snoRNA 以增加该蛋白的分泌。
广阔的领域
虽然合成 snoRNA 并将其递送到正确位置的技术还没有准备就绪,但He和Pan都坚信这些挑战可以解决,因为它建立在以前使用其他形式 RNA 的技术进步之上。他们还认为,由于snoRNA对细胞类型具有特异性,因此它们在其他地方可能具有更多样化的功能和治疗可能性。
He说,“想想神经细胞、干细胞或癌细胞。我们可以研究的细胞类型实在太多了。因此,我认为这个领域是广阔的。”(生物谷Bioon.com)
参考资料:
Bei Liu et al. SnoRNA-facilitated protein secretion revealed by transcriptome-wide snoRNA target identification. Cell, 2024, doi:10.1016/j.cell.2024.10.046.
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


