Cell论文绘制HIV的“天敌”图谱:科学家首次全面破译人类基因如何抵御HIV
来源:生物谷原创 2026-05-20 12:33
这项研究不仅绘制了HIV与人类基因互作的首张“高分辨率地图”,更重要的是,它发现了两个此前完全未知的天然抗病毒战士PI16和PPID。
人类免疫缺陷病毒(HIV)是艾滋病的病原体,它是一位伪装大师,仅用9个基因就能劫持人体复杂的细胞机器。然而,即使经过数十年的病毒复制和潜伏研究,研究人员仍未解开究竟哪些人类基因会影响HIV感染这个谜团。

如今,格莱斯顿研究所和加州大学旧金山分校(UCSF)的科学家创建了首个全面的遗传学“路线图”,揭示了病毒如何与真实人类细胞相互作用,从而开启了理解HIV的新大门。在一项发表于《Cell》期刊的研究中,团队鉴定出了大量要么帮助病毒增殖、要么阻止病毒的人类蛋白。
该研究负责人、Gladstone-UCSF基因组免疫学研究所Connie and Bob Lurie主任、医学博士、哲学博士Alex Marson说:“40多年来,HIV一直是全球性危机。通过研究病毒的主要靶标——人类T细胞,我们终于绘制出了影响这些细胞能否被HIV感染的基因图谱。其中许多基因此前是未知的。”
Marson受过传染病医生培训,曾在旧金山的一家HIV诊所工作。在这项研究中,他与Nevan Krogan(哲学博士)密切合作。Krogan是HIV辅助与调节复合物(HARC)中心主任,该项目旨在更好地理解HIV与人类细胞之间的相互作用。
Krogan表示:“这是首个全基因组范围的工作,展示了人类基因如何影响直接从人类血液样本中获取的细胞的HIV感染。我们的发现最终可能催生帮助人体免疫系统抵抗病毒的新疗法。”
在真实人类细胞中研究HIV
HIV主要感染CD4+ T细胞,这些细胞负责协调人体的免疫反应。然而,历史上大多数HIV研究都是在所谓的“永生”细胞系中进行的——本质上是在实验室中容易培养的癌细胞。但由于这些细胞并非直接来自人类捐献者,它们与人体的真实情况相关性较差。因此,科学家对细胞如何应对HIV攻击的认识一直不完整。
过去十年中,Marson实验室(包括Ujjwal Rathore博士)的一个科学家团队一直在努力克服这一局限。他们逐步推进在真实人类T细胞中释放CRISPR基因编辑的力量,以研究基因组中的每一个基因,并确定哪些基因对HIV至关重要。
Rathore说:“使用真实人类T细胞进行研究的一个挑战是,它们很难被HIV感染;在整个培养皿的细胞中,通常只有1%到2%会被感染。我们花了很多年摸索如何优化这些细胞中的HIV感染,现在我们可以让高达70%的细胞被病毒感染。”
一旦实现这一点,科学家们找到了一种方法,一次性测试所有2万个人类基因,以确定哪些基因被病毒劫持,哪些基因进行反击。
他们采用了两步法利用CRISPR基因编辑:首先,破坏每一个人类基因,以确定HIV生存所需的基因;然后,分别增强每个基因的活性,使其过量产生蛋白,从而使科学家能够发现那些擅长防御病毒的蛋白。
Marson实验室科学家、研究第一作者Eli Dugan说:“过度激活基因为我们提供了丰富的信息。我们发现了一些天然抗病毒蛋白,由于病毒能有效沉默它们,此前它们一直未被发现。通过提高T细胞中这些基因的水平,我们终于看到它们赢得了对抗HIV的战斗。”
两种新的细胞守卫者
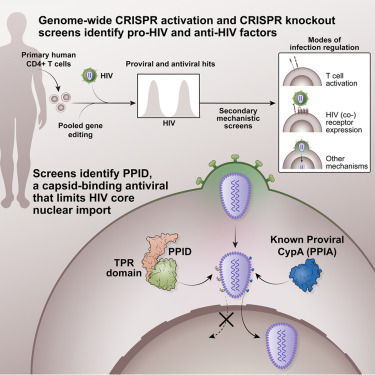
通过这些努力,科学家们鉴定出数百种在人类T细胞中起促进或抑制HIV感染作用的蛋白。随后他们深入研究了这些蛋白的功能。其中两种蛋白以其强大的抗病毒特性脱颖而出——它们被称为“PI16”和“PPID”,此前从未与HIV感染联系起来。
研究团队发现,增加PI16的水平可以阻断HIV与T细胞的融合,从而在感染开始之前就阻止它。而PPID则在病毒进入细胞后发挥作用,限制HIV到达细胞核并开始复制自身的能力。
Dugan说:“我们在实验室找到了调节PPID的方法,使其阻止HIV的效果提高了10倍。”
团队联系了UCSF名誉教授Jay Levy(医学博士),他曾在1983年协助鉴定出HIV病毒。他分享了艾滋病危机早期从患者体内分离出的罕见病毒样本。
Rathore说:“我们发现,增加PPID或PI16的水平可以减少这些人类T细胞中的HIV感染,证明这两种新蛋白甚至能够阻止最具攻击性的天然HIV毒株。”
研究HIV的新途径
虽然目前通过抗逆转录病毒治疗通常可以控制HIV,但一旦治疗停止,病毒就会卷土重来。这是因为即使在接受治疗的患者体内检测不到HIV,病毒也从未真正消失;它隐藏在全身体内的“角落”里。团队在人类T细胞中的先进筛选方法可以提供新数据,以更好地应对这一关键但知之甚少的问题。
Rathore说:“我们此前缺乏一个良好的模型来识别HIV潜伏中的关键参与者。现在我们有了平台,可以提出该领域最大的问题,并有希望学会如何清除当前药物无法触及的潜伏HIV。”
这项新研究还为科学家提供了一个强大的新工具来研究该疾病,开辟了广阔的研究可能性。
Marson说:“这项研究为人类基因如何塑造HIV感染提供了新的视角。我们希望这能成为HIV研究界的基础性资源,并且作为理解其他人类细胞类型中传染病的一个原型。”
临床应用展望与未来方向
(1)新型抗病毒疗法开发:PI16和PPID的发现为设计“宿主导向”药物提供了全新靶点。传统抗HIV药物多直接攻击病毒本身(如逆转录酶抑制剂、蛋白酶抑制剂),但病毒易突变产生耐药。增强宿主自身防御蛋白(例如通过小分子上调PI16或PPID表达)则不易诱导耐药,可作为联合治疗的补充。
(2)潜伏病毒清除策略:当前最大挑战是“激活并杀死”潜伏病毒库。利用PPID变异体(实验室中已获得10倍效力增强版本)联合潜伏逆转剂,可能使藏匿的病毒无法进入细胞核或复制,最终被免疫系统清除。
(3)基因编辑疗法:基于CRISPR技术,在患者造血干细胞中敲入增强型PPID或PI16基因,再回输体内,可能使所有新生T细胞天生对HIV具有抵抗力。这类似于已经成功的CCR5敲除策略(“柏林病人”和“伦敦病人”),但靶点更上游——直接阻断病毒进入或核转运。
(4)广谱抗病毒潜力:由于PI16和PPID作用于病毒生命周期的基础环节(融合和核进入),它们或许对多种HIV亚型甚至其他包膜病毒(如流感、埃博拉)也有抑制作用,值得进一步测试。
(5)诊断和预后标志物:人群中的PI16/PPID表达水平差异可能部分解释为什么有些HIV感染者能长期不进展为艾滋病(即“精英控制者”)。检测这些蛋白的水平或基因型,或可用于预测疾病进展风险。
总而言之,这项研究不仅绘制了HIV与人类基因互作的首张“高分辨率地图”,更重要的是,它发现了两个此前完全未知的天然抗病毒战士PI16和PPID。下一步的研究将聚焦于:这些蛋白能否在动物模型中保护机体免受HIV攻击?是否可以通过药物或基因手段安全地提高它们在人体内的水平?这为最终“治愈”艾滋病带来了全新的希望。(生物谷Bioon.com)
参考文献:
Ujjwal Rathore et al, Systematic Discovery of Pro- and Anti-HIV Host Factors in Primary Human CD4+ T Cells, Cell (2026). DOI: 10.1016/j.cell.2026.03.046.
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


