GPBAR1和CYSLTR1的组合靶向研究揭示了胆汁酸和白三烯在药物性肝损伤中的机制作用
来源:生物谷原创 2022-09-29 14:46
药物性肝损伤(DILI)是一种较为常见的肝损伤原因,由于药物、草药和替代药物等外来生物制剂的使用。
药物性肝损伤(DILI)是一种较为常见的肝损伤原因,由于药物、草药和替代药物等外来生物制剂的使用。从机制上讲,DILI是由于内在毒性,这是剂量依赖性的,并在异源性暴露后的短时间内发展,或特异毒性,这是间接的,可能在异源性暴露后的任何时间间隔发展。
药物性肝损伤(DILI)是一种常见的疾病,涉及直接肝细胞毒性和免疫激活。胆汁酸受体GPBAR1 (TGR5)和半胱基白三烯受体(cyysltr)1是G蛋白偶联受体,由胆汁酸和白三烯激活,对细胞间粘附、炎症和免疫细胞激活产生相反的作用。

图片来源: https://pubmed.ncbi.nlm.nih.gov/36107019/
近日,来自意大利佩鲁贾大学的研究者们在Hepatology杂志上发表了题为“Combinatorial targeting of GPBAR1 and CYSLTR1 reveals a mechanistic role for bile acids and leukotrienes in drug induced liver injury”的文章,该研究证实了GPBAR1和CYSLTR1在DILI的发生发展中相互作用。一种旨在激活GPBAR1同时抑制CYSLTR1的组合方法可逆转DILI模型中的肝损伤。
肝脏外组织RNAseq分析显示APAP中毒正向调节白三烯通路CYSLTR1、ALOX5和ALOX5AP,而GPBAR1基因表达不变。在小鼠中,口服剂量为500 mg/kg的APAP诱导的急性肝损伤在Gpbar1基因消融后严重加重,在抗cysltr1 siRNA预处理后减弱。
研究者用CHIN117治疗给药的野生型小鼠逆转了APAP引起的肝损伤,并调节了多达1300个基因,包括38个趋化因子和受体,这些基因是GPBAR1激动剂或CYSLTR1拮抗剂给药小鼠所不具有的。
在肝窦细胞(LSEC)、单核细胞和Kupffer细胞中检测到两种受体的共表达,而组合调控CYSLTR1和GPBAR1可以有效逆转LSEC-单核细胞的相互作用。CHIN117逆转CCL4给药小鼠的肝损伤和肝纤维化。
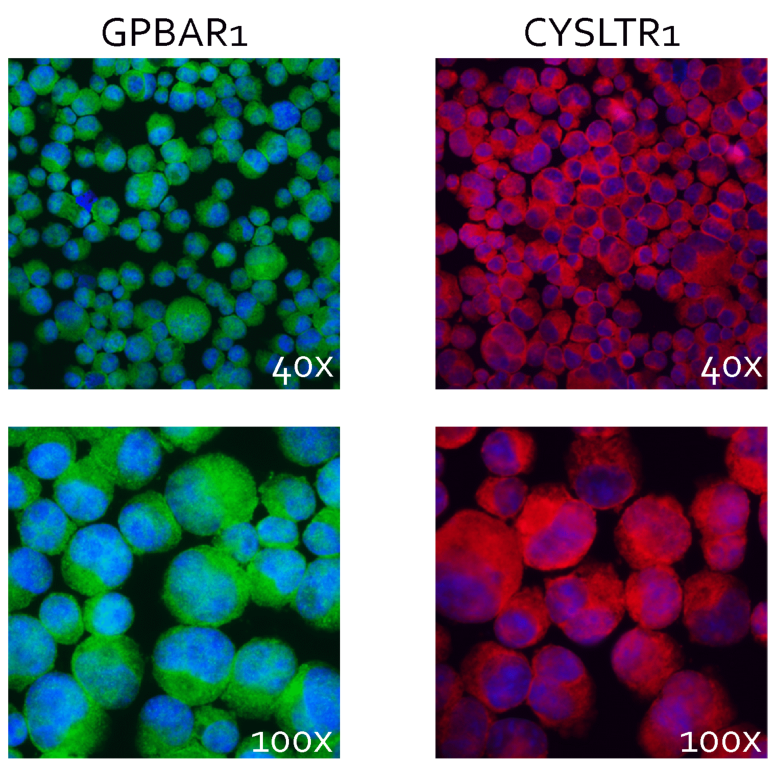
CHIN117对Lx-2细胞活化的药理作用
图片来源: https://pubmed.ncbi.nlm.nih.gov/36107019/
总之,本研究已经证明了GPBAR1和CYSLTR1由LSEC、循环单核细胞和肝脏巨噬细胞共同表达,并且设计了一种以CYSTLR1和GPBAR1为靶点的组合方法,这种混合的、口服活性的小分子有效地挽救了肝脏损伤的啮齿类动物模型。(生物谷 Bioon.com)
参考文献
Michele Biagioli et al. Combinatorial targeting of GPBAR1 and CYSLTR1 reveals a mechanistic role for bile acids and leukotrienes in drug induced liver injury. Hepatology. 2022 Sep 15. doi: 10.1002/hep.32787.
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


