Immunity:科学家发现驱动细胞死亡和炎症发生的“分子”罪魁祸首
来源:本站原创 2022-02-27 16:56
来自沃尔特伊丽莎医学研究所等机构的科学家们通过研究识别出了一种在体内负责引起破坏性细胞死亡和炎症发生的分子“罪魁祸首”,相关研究结果有望帮助改善一系列炎性细胞死亡所驱动的疾病的治疗性策略,包括SARS-CoV-2病毒等。
2022年2月27日 讯 /生物谷BIOON/ --细胞死亡在病原体感染过程中扮演着关键角色,近日,一篇发表在国际杂志Immunity上题为“Interferon-γ primes macrophages for pathogen ligand-induced killing via a caspase-8 and mitochondrial cell death pathway”的研究报告中,来自沃尔特伊丽莎医学研究所等机构的科学家们通过研究识别出了一种在体内负责引起破坏性细胞死亡和炎症发生的分子“罪魁祸首”,相关研究结果有望帮助改善一系列炎性细胞死亡所驱动的疾病的治疗性策略,包括SARS-CoV-2病毒等。
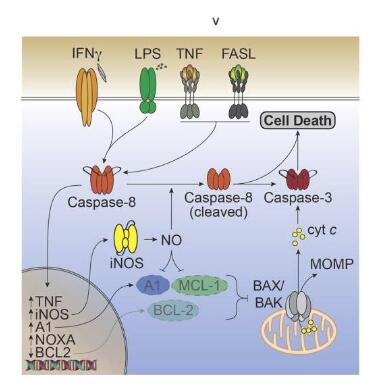
图解摘要。
图片来源:DOI:10.1016/j.immuni.2022.01.003
细胞死亡是机体免疫系统应对感染的重要部分,当其失控时,就会在机体其它健康器官和组织中引起有害的炎症反应,本文中,研究人员揭示了一氧化氮分子的过量产生如何引起危险水平的细胞死亡,蛋白质caspase-8能帮助产生一氧化氮,阻断caspase-8的功能或许能帮助防止未受控制的细胞死亡和炎症发生。
这篇研究报告中,研究人员强调了开发新型药物来阻断caspase-8和一氧化氮来预防这种新型炎性细胞死亡过程的潜力,而通过操控细胞死亡通路或许有望帮助开发新型改进型疗法来治疗炎性疾病患者。尽管一氧化氮对于机体的循环和神经系统非常重要,但最近的研究结果将这种分子的过量产生与细胞死亡和炎症的过度水平关联了起来,细胞死亡对于机体健康的免疫反应至关重要,然而过多的细胞死亡或会使得机体免疫系统进入超速状态并诱发炎性疾病发生。
研究者James Vince教授说道,他们惊讶地发现,一氧化氮或许是在新发现的炎性细胞死亡通路中驱动过度细胞死亡的罪魁祸首,本文中,我们对细胞死亡过程中病原体和宿主炎性分子的联合行动的研究或许直接导致了对一氧化氮的研究。研究者揭示了一氧化氮到底是如何以特殊的途径成为细胞死亡的主要驱动力,本文研究结果表明,当免疫细胞感觉到病毒和病原体威胁时,这种分子的水平就会急剧上升,制造的一氧化氮越多,细胞就越有可能发生死亡。
研究者认为,阻断一氧化氮和细胞死亡蛋白caspase-8的产生或许会降低临床前SARS-CoV-2感染模型机体中疾病的严重程度。移除这些模型机体中的caspase-8或一氧化氮很可能会阻断细胞死亡并引起组织损伤,从而就强调了利用caspase-8作为一种药物靶点来阻断过度的细胞死亡和随后的炎性反应的重要性。尽管目前研究人员得到了临床前的研究数据,但他们相信,阻断caspase-8或一氧化氮的产生或许会预防炎症的损伤水平。
图片来源:https://www.cell.com/immunity/fulltext/S1074-7613(22)00032-2?_returnURL=https%3A%2F%2Flinkinghub.elsevier.com%2Fretrieve%2Fpii%2FS1074761322000322%3Fshowall%3Dtrue
研究人员利用CRISPR技术系统对新的细胞死亡通路进行了遗传分析,并进一步理解了其中关键基因所扮演的关键角色。DNA编辑技术能被用来在基因中产生突变从而确定哪种基因在这种细胞死亡通路中会促进一氧化氮的产生。与COVID-19模型相结合,这种新技术或能促进研究人员理解caspase-8所扮演的确切角色;能够理解并操控这一途径中的关键基因或许有望帮助研究人员开发新型疗法选择,并用于治疗已经被确认会发生损伤性一氧化氮的疾病,比如哮喘症、炎性肠病和SARS-CoV-2病毒感染等。
综上,本文研究结果表明,诱导性的一氧化氮合酶或能选择性地许可程序性细胞死亡过程,这或许就能够解释在SARS-CoV-2感染和其它一氧化氮合酶相关的炎性疾病状况下,一氧化氮如何影响宿主机体的疾病严重程度。(生物谷Bioon.com)
原始出处:
Daniel S. Simpson,Jiyi Pang,Ashley Weir, et al. Interferon-γ primes macrophages for pathogen ligand-induced killing via a caspase-8 and mitochondrial cell death pathway, Immunity (2022). DOI:10.1016/j.immuni.2022.01.003
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。



