PNAS:李博文团队开发向肌肉特异性递送mRNA的新型LNP
来源:生物世界 2023-12-15 16:37
尽管iso-A11B5C1引发体液免疫的能力有限,但它通过肌肉注射能够有效启动细胞免疫反应,通过iso-A11B5C1观察到的显著抗肿瘤效果强调了其可作为癌症疫苗开发的可行候选者。
近日,多伦多大学李博文团队(博士生Jingan Chen、博士后Yue Xu为共同第一作者)在《美国国家科学院院刊》(PNAS)发布了题为:Combinatorial design of ionizable lipid nanoparticles for muscle-selective mRNA delivery with minimized off-target effects 的研究论文。
该研究提出了一个快速创建化学多样性脂质构建LNP的平台,并成功地识别了一种可电离脂质——iso-A11B5C1,将其加入LNP后,能够实现高效的肌肉特异性mRNA递送,同时最小化对其他组织(例如肝脏和脾脏)的脱靶递送。
尽管这种新型LNP在淋巴结中的转染有限,但肌肉注射后可以引发强大的细胞免疫反应,在黑色素瘤小鼠模型中进一步验证。使用这种新型LNP开发的mRNA黑色素瘤疫苗,在黑色素瘤小鼠模型中显示了强大的抗肿瘤效果。这项研究推进了肌肉特异性的mRNA递送的方法,并促使人们重新思考mRNA疫苗的设计。

论文通讯作者李博文表示,这项研究首次展示了mRNA-LNP仍然可以有刺激细胞免疫反应,产生强大的抗肿瘤效果,即使没有直接靶向或转染淋巴结。这一发现挑战了传统的理解,并表明免疫细胞中的高转染效率可能不是开发有效的癌症mRNA疫苗的唯一途径。
经典的LNP配方由四种成分组成,分别是:可电离脂质、辅助磷脂、胆固醇和聚乙二醇化脂质,这也是目前临床上使用的mRNA递送系统。这四种组分中,可电离脂质至关重要,但是,合成这些成分仍然是一个复杂、耗时和昂贵的过程,因此需要开发出快速、简化的方法。为了实现这一目标,采用多组分反应的组合化学已成为高通量合成广泛和化学上多样化的脂质库的有效工具。
在这项研究中,李博文团队开发了一种先进的合成平台,可以在室温下一步高效制造生物可降解的不对称可电离脂质。他们使用这个平台鉴定了一种新型可电离脂质——iso-A11B5C1,这是一种特别适合肌肉特异性mRNA递送的可电离脂质。与现在临床中使用的mRNA新冠疫苗的LNP对比,iso-A11B5C1表现出高水平的肌肉特异性mRNA递送效率。
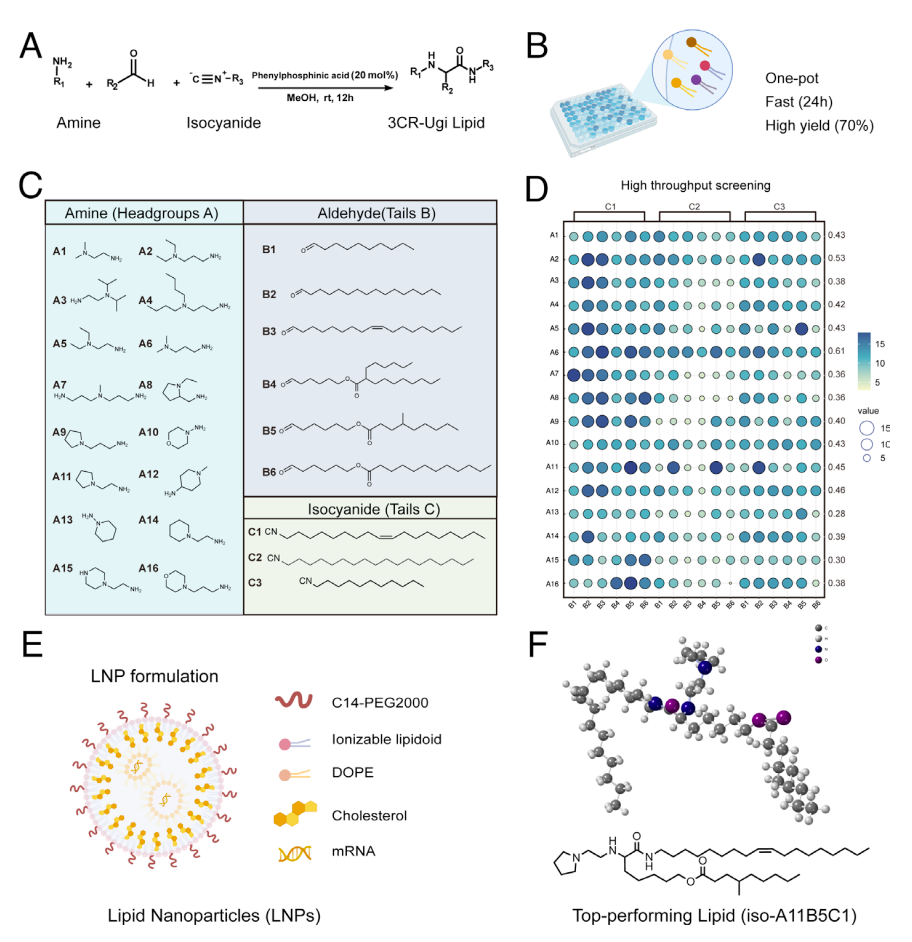
李博文表示,与传染病疫苗产生的以抗体中重点的免疫反应不同,iso-A11B5C1引发了较低的体液免疫反应,但引发了相当水平的细胞免疫反应。这一发现促使团队进一步探索它作为一种潜在的癌症疫苗候选者,在细胞免疫发挥关键作用的黑色素瘤模型中进行测试。
在小鼠黑色素瘤模型中的测试表明,iso-AB11B5C1 LNP表现出了强大的抗肿瘤效果,显著减缓了肿瘤生长,抗原特异性CD8+ T细胞水平升高,并且CD8+ T细胞大量浸润到肿瘤中,这些效果优于目前常用的MC3 LNP配方。这些结果证实了iso-A11B5C1 LNP作为治疗性癌症疫苗递送载体的卓越效果。
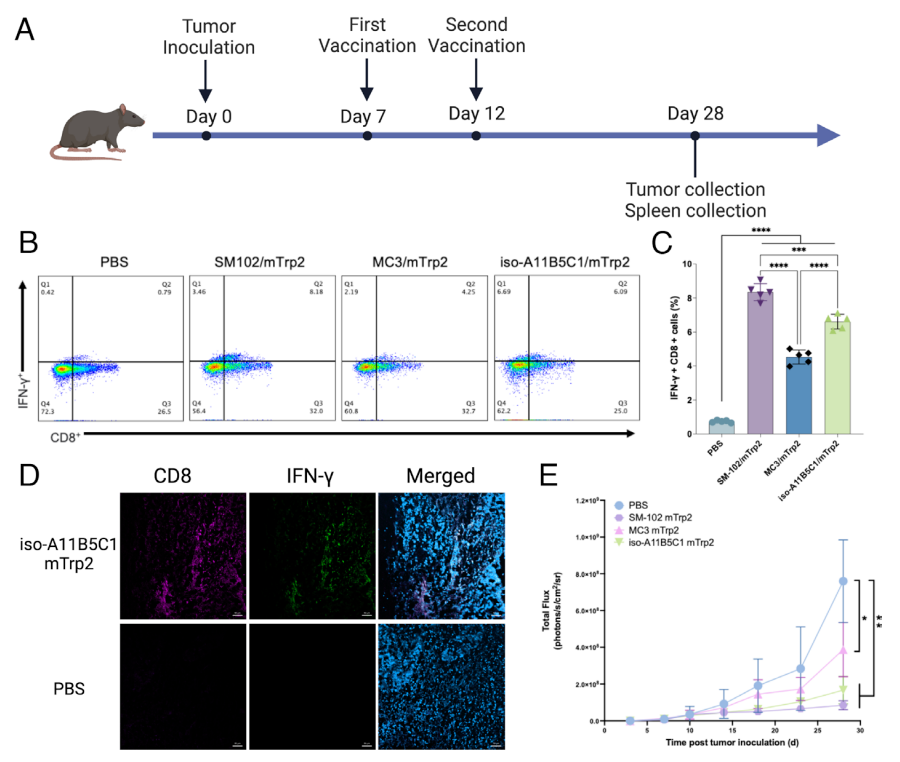
尽管iso-A11B5C1引发体液免疫的能力有限,但它通过肌肉注射能够有效启动细胞免疫反应,通过iso-A11B5C1观察到的显著抗肿瘤效果强调了其可作为癌症疫苗开发的可行候选者。
最后,研究团队表示,这项研究让我们重新思考了mRNA疫苗的设计原则,表明实现高水平的免疫细胞转染可能不是开发有效mRNA疫苗的唯一标准。重要的是,这项研究强调了iso-A11B5C1可在最小脱靶效应的情况下进行高效肌肉特异性基因编辑的能力,从而为针对肌肉疾病的安全和有效的基因治疗提供了一种有前途的方法。
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


