Cell:新的图谱绘制了衰老大脑中8个区域和36种细胞类型的表观遗传变化
来源:生物谷原创 2026-03-13 11:39
对脑细胞进行整体分析会丢失细胞类型特异性,这使得单细胞分析成为一种强大的工具。因此,索尔克研究所的研究人员着手创建迄今为止最全面的单细胞、多组学脑成像数据集。
神经退行性疾病影响着全球超过5700万人。从阿尔茨海默病到帕金森病,再到肌萎缩侧索硬化症等,这些疾病的发病率预计每20年翻一番。尽管科学家们知道衰老是神经退行性疾病的主要风险因素,但衰老影响的完整机制仍不清楚。
衰老的一个主要机制性影响是表观遗传变化:我们基础遗传密码上的小化学标签随时间推移而改变基因表达的方式。
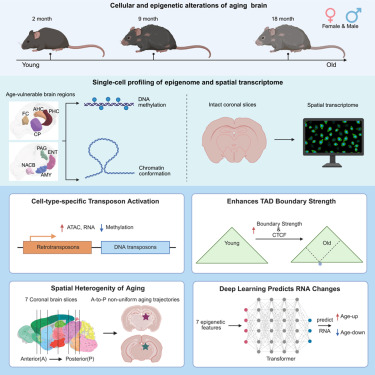
索尔克研究所的研究人员创建了迄今为止最全面的衰老小鼠大脑表观遗传变化单细胞图谱,揭示了DNA甲基化、基因组结构和基因活性如何跨脑区和细胞类型发生变化。这份新图谱代表了八个脑区和36种不同的脑细胞类型,通过甲基化和染色质构象分析描绘了超过20万个单细胞,并利用空间转录组学捕获了近90万个细胞。该图谱的内容已经揭示了不同年龄组之间的明显表观遗传差异,并使研究人员能够开发出预测年龄相关基因表达变化的新型深度学习模型。

该图谱发表在《细胞》期刊上,现已在亚马逊网络服务和基因表达综合库上公开,它将作为解释人类大脑数据集的关键参考框架,包括由美国国立卫生研究院通过推进创新神经技术进行大脑研究计划生成的数据集。
"与年龄相关的大脑变化,尤其是在负责注意力、记忆、情感和运动功能的关键区域,严重影响了生活质量。"共同通讯作者、索尔克研究所教授兼索尔克国际委员会遗传学讲席教授、霍华德·休斯医学研究所研究员Joseph Ecker博士说。"通过绘制随着动物衰老,单个脑细胞类型的表观基因组如何变化,我们现在有了一个框架来理解衰老如何在分子水平上重塑大脑。这一资源应有助于研究人员精确定位促成神经退行性疾病的机制。"
我们对衰老的大脑了解多少?
随着年龄增长,会出现四个分子标志:慢性炎症、线粒体功能障碍、基因组不稳定性和表观遗传变化。最近的发现已将表观基因组确定为生理性衰老的主要驱动因素。而一种称为甲基化的表观遗传变化类型与神经元功能、行为和疾病有关。
如果科学家能够将甲基化变化与不良的年龄相关结果联系起来,他们就可以开始设计逆转这些变化并恢复健康的解决方案。但生成有用的甲基化数据并不像取样几个脑细胞并得出概括性结论那么简单。大脑有许多不同的区域和细胞类型,必须逐一考虑才能全面了解情况。
"大脑是相互关联的,不同的区域控制着不同的功能,并且在细胞类型水平上以不同的速度衰老。"共同通讯作者、索尔克研究所研究教授Margarita Behrens博士说。"我们可以看到大脑在帕金森病等疾病中的相互关联程度,一组神经元的死亡会螺旋式地导致整个回路功能障碍,然后出现我们在患者身上看到的震颤和认知影响。因此,对衰老进行细胞类型特异性理解的重要性将带来更精细的知识,从而扩大治疗的可能性。"
什么是表观遗传图谱?
对脑细胞进行整体分析会丢失细胞类型特异性,这使得单细胞分析成为一种强大的工具。因此,索尔克研究所的研究人员着手创建迄今为止最全面的单细胞、多组学脑成像数据集。
除了甲基化,他们还调查了另一种称为染色质构象的基因组调控机制——基因组的3D形状。他们还使用尖端空间转录组学技术,在绘制基因表达图谱的同时,保留采样脑组织内的空间背景。
"这项工作之所以创新,首先在于其空间维度。"第一作者、Ecker实验室的研究生Qiurui Zeng解释道。"空间分辨率揭示了哪些区域和局部微环境最容易受到衰老影响,细胞类型组成如何随时间在不同脑区之间变化,以及邻近细胞可能如何影响彼此的衰老轨迹。空间数据集的规模——近90万个空间转录组细胞,对于一项纵向衰老研究而言本身就是前所未有的。"
使用衰老小鼠模型,团队收集了132,551个单脑细胞的甲基化数据以及72,666个脑细胞的甲基化-染色质构象联合数据。总共代表了36种主要细胞类型。
该数据集已于2025年12月在AWS和GEO上完整发布。在AWS上托管这个包含近90万个空间解析细胞的庞大数据集,既确保了可访问性,也保证了即时性。通常,如此海量的数据需要强大的计算能力才能访问,但云托管打破了这些基础设施障碍。
"AWS开放数据计划承担了存储成本,并将此数据集与艾伦脑图谱、西雅图阿尔茨海默病脑细胞图谱等其他主要神经科学资源放在一起,使其成为可公开访问的脑数据互联生态系统的一部分。"Zeng补充道。"从事衰老、神经退行性疾病和空间基因组学研究的科学家可以立即利用这一资源,从而大大加快发现速度,远超单个实验室所能取得的成就。"
表观遗传图谱能教给我们什么?
首先,甲基化数据揭示,与年龄相关的甲基化变化在非神经元细胞中更为显著。团队发现,随着细胞衰老,转座元件会失去DNA甲基化,这表明通常沉默的基因组元件在衰老的大脑中变得更加活跃。
转座元件是构成人类基因组约一半的重复DNA序列,它们的表达可能导致功能障碍和与年龄相关的衰退。这一发现与表观遗传变化可能导致衰老相关细胞功能障碍的观点一致。
染色质构象数据揭示了衰老过程中的进一步变化。值得注意的是,研究人员能够识别出一种新的脑衰老生物标志物:拓扑关联结构域边界处的强度增加以及相关CTCF结合位点的可及性增加。
基因组中包含的大量信息是使用拓扑相关结构域(TADs)组织的,TADs只是一些协同工作的较小的DNA片段。CTCF是一种蛋白质,它结合到TADs两端的边界上,协助它们的组织。然后是时候整合空间转录组学的见解了。将近90万个细胞被用来追踪不同脑区和细胞类型衰老之间的差异。
"同一种细胞类型因其位置不同而衰老方式也不同。例如,大脑后部的非神经元细胞比前部的非神经元细胞显示出更多的炎症。"Zeng说。"这些数据确实强调了即使是同一细胞类型在衰老过程中的变异性,强调了在解开衰老复杂性时细胞和脑区水平特异性的重要性。"
这个图谱将如何帮助科学家和患者?
团队已经从数据集中获得了令人印象深刻的见解。例如,他们开发了深度学习方法,利用未来的多组学表观遗传数据来预测基因表达,从而为未来开发虚拟大脑衰老模型奠定了基础。更多激动人心的见解即将出现。
该图谱现已在线提供,供任何人使用。通过让所有人都能访问这类资源,科学家们希望借助全球合作的力量加速他们的发现。(生物谷Bioon.com)
参考文献:
Qiurui Zeng et al, Cell-type-specific transposon demethylation and TAD remodeling in aging mouse brain, Cell (2026). DOI: 10.1016/j.cell.2026.02.015.
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


