线粒体 RNA“越狱”引爆炎症!Nat Commun:梅奥诊所破解“僵尸细胞”驱动脂肪肝的关键密码
来源:生物谷原创 2025-12-17 11:29
梅奥诊所的研究人员揭示了衰老的"僵尸细胞(zombie cells)"如何触发有害炎症,从而加速一种严重且日益常见的脂肪肝疾病——代谢功能障碍相关脂肪性肝炎(MASH)。
随着全球肥胖率持续攀升,代谢功能障碍相关脂肪性肝炎(MASH)已成为日益严峻的公共健康威胁,不仅是肝纤维化、肝癌的主要诱因,更逐渐成为肝移植的首要原因之一。这种疾病的核心特征是肝脏持续炎症与瘢痕形成,若得不到有效干预,往往会向终末期肝病进展。
近日,梅奥诊所的研究团队在《Nature Communications》上发表突破性研究,首次揭示了衰老 "僵尸细胞"(senescent cells)驱动 MASH 的关键机制——线粒体 RNA(mtRNA)的胞质泄漏,为这类难治性肝病提供了全新治疗靶点。

所谓 "僵尸细胞",是指那些因衰老、DNA 损伤或化疗等刺激而进入不可逆生长停滞状态的细胞。它们虽不再分裂,却会持续分泌大量促炎因子、趋化因子和基质降解蛋白,形成衰老相关分泌表型(SASP),如同 "僵尸" 般不断释放毒性信号,损害周围健康组织。年轻时,免疫系统能及时清除这些细胞,但随着年龄增长或代谢紊乱,它们会在肝脏等组织中大量堆积,成为慢性炎症和组织损伤的 "隐形推手"。
此前研究多聚焦于直接清除 "僵尸细胞",而梅奥诊所的团队则另辟蹊径,深入探究了这些细胞如何发出有害信号,为精准干预提供了新视角。
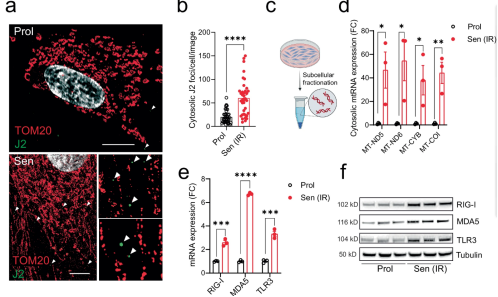
研究团队发现,"僵尸细胞" 的核心破坏力源于线粒体的 "内部叛变":正常情况下被禁锢在线粒体内的双链线粒体 RNA(mtdsRNA)会发生泄漏,逃入细胞质中。与核 RNA 不同,mtdsRNA 缺乏关键的核苷修饰,结构上与病毒 RNA 相似,极易被细胞的天然免疫传感器识别为 "危险信号"。
具体而言,这些逃逸的 mtdsRNA 会特异性结合细胞质中的 RNA 传感器RIG-I和MDA5,触发这两种蛋白的寡聚化,进而诱导线粒体抗病毒信号蛋白(MAVS)形成功能性聚集体——这一过程是激活下游炎症通路的关键步骤。最终,通过激活 NF-κB 和 IRF3 等转录因子,引发强烈的 SASP 反应,持续招募免疫细胞浸润肝脏,加剧炎症和纤维化。
而这场 "RNA 越狱" 的幕后推手,是两种名为 BAX 和 BAK 的促凋亡蛋白。研究证实,BAX 和 BAK 会在衰老细胞的部分线粒体膜上形成微小孔道(即微小线粒体外膜通透性,miMOMP),正是这些孔道为 mtdsRNA 的泄漏提供了物理通道。有趣的是,BAX 在这一过程中扮演了更关键的角色——单独抑制 BAX 就能显著降低 IL-6、IL-8 等核心 SASP 因子的表达,而抑制 BAK 的效果则微乎其微。
进一步的转录组分析显示,BAX/BAK 缺失与 MAVS 沉默会共同下调 32 个 SASP 相关基因,其中 30 个均为 NF-κB 的靶基因,表明线粒体应激信号最终会通过 NF-κB 通路收敛,放大炎症效应。
为验证这一机制的体内相关性,研究团队构建了 MASH 小鼠模型:给小鼠喂食高果糖、高脂肪、高胆固醇(FFC)饮食 24 周,成功诱导出肝脏衰老、炎症和纤维化表型。随后,通过基因编辑或 AAV 病毒介导的肝细胞特异性敲除,抑制 BAX/BAK 或 MAVS 的功能,结果令人振奋:小鼠肝脏中的 RNA 传感器(RIG-I、MDA5、TLR3)表达显著降低,纤维化标志物(TIMP1、Col1a1)和促炎因子(CCL2、CXCL10)水平下降,CD68 + 巨噬细胞浸润减少,肝脏组织功能得到明显改善。更重要的是,这种干预并未影响细胞衰老本身的生长停滞特性,避免了干扰衰老细胞的肿瘤抑制功能,安全性更具优势。
值得关注的是,这项研究还揭示了线粒体核酸信号的复杂性:除了已知的线粒体 DNA(mtDNA)泄漏激活 cGAS-STING 通路,mtdsRNA 的 "越狱" 构成了另一平行的炎症驱动轴。这两种核酸信号既会协同放大 SASP 效应,又各自调控不同的炎症基因模块,形成多层次的促炎网络。此外,研究团队还发现,抑制线粒体 RNA 聚合酶(POLRMT)阻止 mtdsRNA 合成,同样能有效抑制 SASP,这为开发小分子药物提供了新的思路。
"随着年龄增长,僵尸细胞会在体内不断积累,成为多种年龄相关疾病的共同推手。" 该研究的资深作者 João Passos 博士表示,"我们的发现表明,无需清除僵尸细胞,只需阻断其有害信号的释放,就能平息失控的炎症,延缓 MASH 等疾病的进展。这种靶向机制的策略,有望同时惠及多种与衰老相关的炎症性疾病。"
目前,研究团队正进一步开发技术,以实现对体内 "僵尸细胞" 的空间定位与精准干预。这项研究不仅为 MASH 提供了全新的治疗靶点(如 BAX/BAK、MAVS、POLRMT),更刷新了我们对衰老细胞致病机制的认知——线粒体 RNA 的胞质泄漏是连接细胞衰老与慢性炎症的关键桥梁。
未来,针对这一通路的药物研发,或将为 MASH 患者带来避免肝移植、阻断疾病进展的新希望,也为其他年龄相关炎症疾病(如心血管病、神经退行性疾病)的治疗提供宝贵借鉴。(生物谷Bioon.com)
参考文献:
Stella Victorelli et al, Mitochondrial RNA cytosolic leakage drives the SASP, Nature Communications (2025). DOI: 10.1038/s41467-025-66159-z.
版权声明
本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->





