Structure:修饰的tau蛋白在保留其生物学功能的同时阻止神经退行性疾病中的病理性聚集
来源:生物谷原创 2026-01-06 10:26
由德克萨斯大学西南医学中心研究人员领导团队开发的一种tau蛋白设计版本,在保持其生物学功能的同时,能够抵抗聚集——这是与称为tau蛋白病的神经退行性疾病相关的一种病理特征。

发表在《Structure》期刊上的这些发现,可能为包括阿尔茨海默病、额颞叶痴呆、慢性创伤性脑病(CTE)和进行性核上性麻痹在内的疾病带来新的治疗方法。
研究负责人、德克萨斯大学西南医学中心阿尔茨海默病和神经退行性疾病中心及生物化学与生物物理学系副教授Lukasz Joachimiak博士表示:"这是朝着创造一种原则上可以替代致病(引起疾病)蛋白质,同时仍保留其正常功能的分子迈出的第一步。"
理解tau蛋白的作用与病理
tau蛋白在细胞中起着至关重要的作用,它调节微管的组装和稳定性,而微管是作为指导囊泡、细胞器和其他成分通过细胞质的"高速公路"的蛋白质组件。tau蛋白通过其蛋白质的一部分结合到微管上,该部分中有一段氨基酸重复三次或四次。这些版本的tau蛋白分别被称为3R或4R。
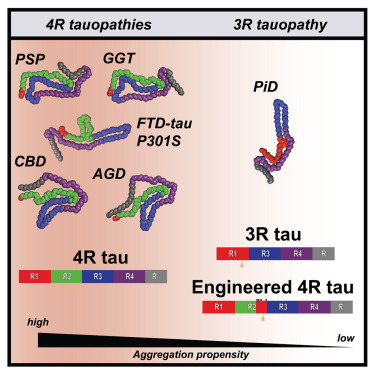
在tau蛋白病中,tau蛋白粘在一起或聚集,形成线状团块,从而在大脑中产生沉积物。Joachimiak博士解释说,先前的研究表明,绝大多数tau蛋白病是由4R形式的tau蛋白聚集引起的。但为什么会发生这种情况,以及是否有可能修改tau蛋白以防止聚集而不破坏其与微管的结合——一直未知。
设计抗聚集的tau蛋白
为了回答这些问题,来自Joachimiak实验室的研究人员及其同事构建了由4R重复序列和所谓的VQIVYK基序(负责形成团块的蛋白质部分)组成的tau蛋白片段,并改变了这些部分之间的几个氨基酸以模拟3R中发现的氨基酸。尽管未进行氨基酸替换的片段在试管中很容易聚集,但经过设计的片段则不会。
更仔细的观察揭示了原因:在设计片段的重复序列和VQIVYK基序之间的部分形成了一个刚性曲线,使其呈发夹形状,从而阻止它们与其他片段上的VQIVYK基序接触并形成团块。进一步的实验证实,这种设计策略在更大的tau蛋白片段和细胞中也有效,改变后的蛋白质能阻止与天然4R tau蛋白的聚集。
对未来疗法的意义
Joachimiak博士表示,重要的是,改变这些氨基酸并不影响tau蛋白与微管结合的能力,这表明改变后的蛋白质仍然可以执行其生物学功能。他说:"工程化的tau变异体保留了微管结合能力这一事实表明,在减少致病性聚集的同时保留生理功能是可能的。"
Joachimiak博士补充说,他的团队未来的研究将测试用这种设计版本替换天然tau蛋白是否能在动物模型中阻止tau蛋白病,这是为神经退行性疾病制定新治疗方法的一步。
他表示:"许多研究已经检验了tau蛋白亚型、聚集机制以及诸如与额颞叶痴呆相关的突变。但是,很少有研究像我们这项研究一样,对tau蛋白变异体进行理性设计以减少聚集,同时保留其功能。"(生物谷Bioon.com)
参考文献:
Sofia Bali et al, Amyloid-motif-dependent tau self-assembly is modulated by isoform sequence context, Structure (2025). DOI: 10.1016/j.str.2025.11.009.
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


