Science:工程醛脱氢酶可形成酰胺键
来源:生物谷原创 2026-03-06 09:54
这项研究很好地展示了如何通过酶工程对蛋白质分子进行巧妙调整,从而通过生物催化合成推动药物制造。
一种在现代医学中反复出现的单一化学结构,是将羰基连接到氮原子上的酰胺键。它们如此普遍,以至于2023年零售额排名前200的小分子药物中,有117种至少含有一个酰胺键。现在,研究人员发现了一种巧妙的新方法,可以重新设计天然酶,从醛和胺等简单化学品构建酰胺。
研究团队选择了一个自然中丰富的酶家族,即醛脱氢酶(aldehyde dehydrogenase),特别是对羟基苯甲醛脱氢酶,它能有效地将醛转化为酸。团队通过两种主要方式改造其酶的内部口袋,将其转变为一种新型催化剂,称为氧化酰胺酶:使其具有疏水性以防止形成不需要的酸,并使其变大以容纳更大、更多样化的化学部分,从而使它们能够结合在一起。

根据发表在《科学》杂志上的结果,该团队能够通过在一个容器中进行的、两步酶级联反应,直接从市售的醇中获得酰胺。这种方法可以为生产五种主要药物分子开辟更绿色的新方法,其中包括伊马替尼的关键成分,伊马替尼是用于治疗慢性髓性白血病和胃肠道间质肿瘤的基本药物。
通往药物分子骨架的捷径
酰胺键出现在许多用于治疗癌症、心脏病和血液疾病的知名药物中。尽管它们很重要,但这些键的典型形成方式远非理想。大多数传统的酰胺键制造方法依赖高活性化学品、高温或有毒金属,这会产生大量废物,并使药物制造的可持续性降低。
改用基于酶的方法使过程环保,但也有其自身的局限性。例如,脂肪酶,一种常用于将酯转化为酰胺的酶,仅对窄范围的底物有活性。其他酶,如连接酶,则需要非常高的能量输入才能正常运作。
该团队通过利用蛋白质工程的力量,将天然酶转化为高效的合成工具,克服了传统化学的限制。
为了实现这一目标,研究人员重新设计了PHBDD的内部口袋。他们移除了酶中亲水的部分,即两个关键位置R166和E259,并用疏水的甲硫氨酸和亮氨酸替换它们。这种改变改变了反应方向,导致酶使用胺而不是水,并形成酰胺键而不是不需要的酸。
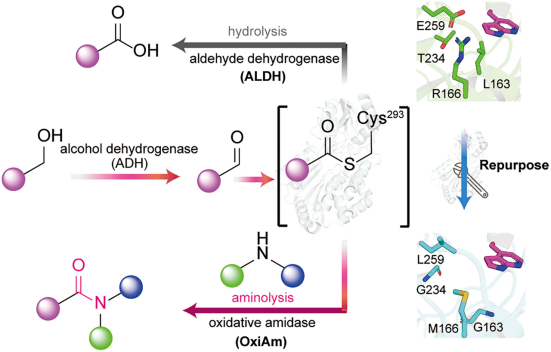
像PHBDD这样的ALDH的另一个问题是,许多重要的药物构建模块太大,无法进入其活性位点。经过几次尝试,研究人员发现,通过突变一个特定点可以扩大通道,将入口通道从6.1 Å拓宽到8.1 Å。
研究人员将他们的新型OxiAm酶与醇脱氢酶配对,创建了一个一锅两步法过程,仅使用空气中的氧气驱动反应,将普通醇直接转化为酰胺。然后,他们用这种方法测试了五种重要药物前体的生产:Vadadustat、Imatinib、Lazabemide、Saruparib和Vorinostat。
这项研究很好地展示了如何通过酶工程对蛋白质分子进行巧妙调整,从而通过生物催化合成推动药物制造。
研究人员认为,这种策略为合成结构多样的酰胺提供了一个绿色且多功能的平台,其应用不仅限于医药领域。(生物谷Bioon.com)
参考文献:
Lei Gao et al, Engineered aldehyde dehydrogenases for amide bond formation, Science (2026). DOI: 10.1126/science.adw3365.
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


