Cell子刊:聂广军/周合江团队开发通用型LYTAC平台,用于肿瘤免疫治疗
来源:生物世界 2024-02-07 09:41
该研究提供了一种模块化和简单的遗传策略用于溶酶体靶向降解,以及用于体内肿瘤靶向的递送平台,为使用TfR-LYTAC系统靶向和降解细胞外蛋白铺平了道路。
云南农业大学周合江助理研究员、国家纳米科学中心聂广军研究员等在 Cell 子刊 Cell Chemical Biology 上发表了题为:Anti-tumor immunotherapy using engineered bacterial outer membrane vesicles fused to lysosome-targeting chimeras mediated by transferrin receptor 的研究论文。
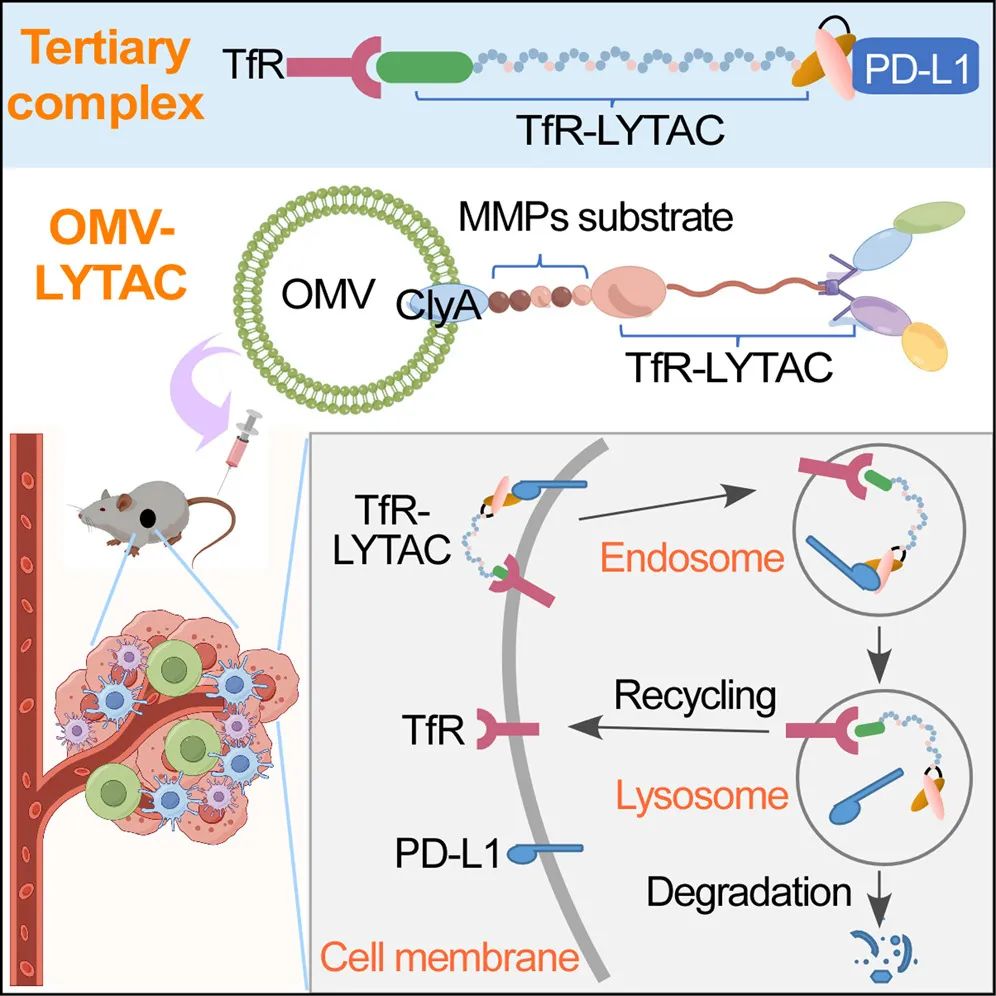
该研究开发了转铁蛋白受体(TfR)介导的溶酶体靶向降解嵌合体(TfR-LYTAC),并将其与细菌外膜囊泡(OMV)表面连接,开发了一个递送平台——OMV-LYTAC。
将LYTAC对PD-1/PD-L1通路的抑制和细菌OMV的免疫激活作用相结合,能够显著抑制了体内的肿瘤生长。

该研究设计了一种基因工程转铁蛋白受体(TfR)介导的溶酶体靶向降解嵌合体(TfR-LYTAC),它可以通过TfR介导的内吞作用有效地内化,并在培养细胞中靶向PD-L1进行溶酶体降解,但由于短半衰期和肿瘤靶向性不佳,在体内无法实现。研究团队通过将TfR-LYTAC融合到细菌外膜囊泡(OMV)表面,开发了一个递送平台——OMV-LYTAC。
经过工程改造的OMV-LYTAC,将LYTAC对PD-1/PD-L1通路的抑制和细菌OMV的免疫激活作用相结合,显著抑制了体内的肿瘤生长。
该研究提供了一种模块化和简单的遗传策略用于溶酶体靶向降解,以及用于体内肿瘤靶向的递送平台,为使用TfR-LYTAC系统靶向和降解细胞外蛋白铺平了道路。
近年来,蛋白质靶向降解领域得到了爆发式增长。溶酶体靶向降解嵌合体(LYTAC)代表了其中一种新方法,通过溶酶体途径诱导细胞外蛋白和膜蛋白的降解。但这种策略面临着复杂的化学合成和有效递送方面的重大挑战。
周合江、聂广军团队开发了基因编码的模块化LYTAC平台,能够通过回收转铁蛋白受体(TfR)和靶向蛋白的招募来降解膜相关蛋白。TfR的持续自我更新能力支持蛋白质稳态,确保TfR在介导目标蛋白降解中的长效性。理论上,这种TfR-LYTAC介导的降解系统可以应用于各种膜蛋白和细胞外蛋白,只需更换靶向蛋白的配体即可。因此,这种降解平台是通用且多功能的。
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


