《自然·纳米技术》:突破!科学家开发新型口服胰岛素制剂,有效控糖,且不会导致低血糖,预计明年开展临床试验
来源:奇点糕 2024-02-06 09:43
这项研究提供了一种新型口服胰岛素纳米制剂,在小鼠、大鼠和狒狒中显示出剂量依赖性地降低血糖,并且没有出现低血糖等不良事件。
目前,全球范围内有4.25亿糖尿病患者,其中有约7500万人需要使用胰岛素[1,2],对于这部分患者来说,需要将注射/输注胰岛素、生活方式干预和持续血糖监测相结合,严格控制血糖水平,以降低急性不良事件(高血糖和低血糖)的发生率和心血管疾病,及肾、神经和视网膜病变等长期合并症。
注射/输注的方式为患者带来了很多生活、工作和人际交往中的不便,低血糖不良事件也显著增加了患者的心血管疾病和死亡风险[3]、降低了健康相关生活质量和生产力[4,5]。
口服胰岛素或许是解决方案之一,因为它能够模拟胰岛素的内源性释放,并且口服的形式更容易为患者所接受。不过,此前的口服胰岛素临床试验未能确立降低低血糖发生率的优势[6]。
近日,澳大利亚悉尼大学的研究团队在《自然·纳米技术》杂志上发表了最新研究成果[7],他们使用纳米载体装载胰岛素制成口服胰岛素纳米制剂,不溶于酸性环境,不会被消化酶分解,能够安全到达肝脏,制剂对葡萄糖苷酶敏感,在血糖水平高时,葡萄糖苷酶活跃,纳米外壳被分解,释放胰岛素。
在糖尿病小鼠和大鼠中,该制剂成功使血糖产生剂量依赖性降低,并且没有出现低血糖和体重增加,在健康的狒狒中也复刻了这一结果,几种动物模型中均未观察到生化或血液学不良事件。研究人员预计临床试验将于2025年启动[8]。

研究使用的纳米载体是覆盖着壳聚糖/葡萄糖聚合物(CS/GS)的硫化银量子点(又称为纳米晶,粒径介于1-10nm之间),与单独的胰岛素和量子点相比,胰岛素与硫化银量子点结合在一起后,在低pH环境中的溶解度降低,在pH 3.5-6.5之间具有不溶性。
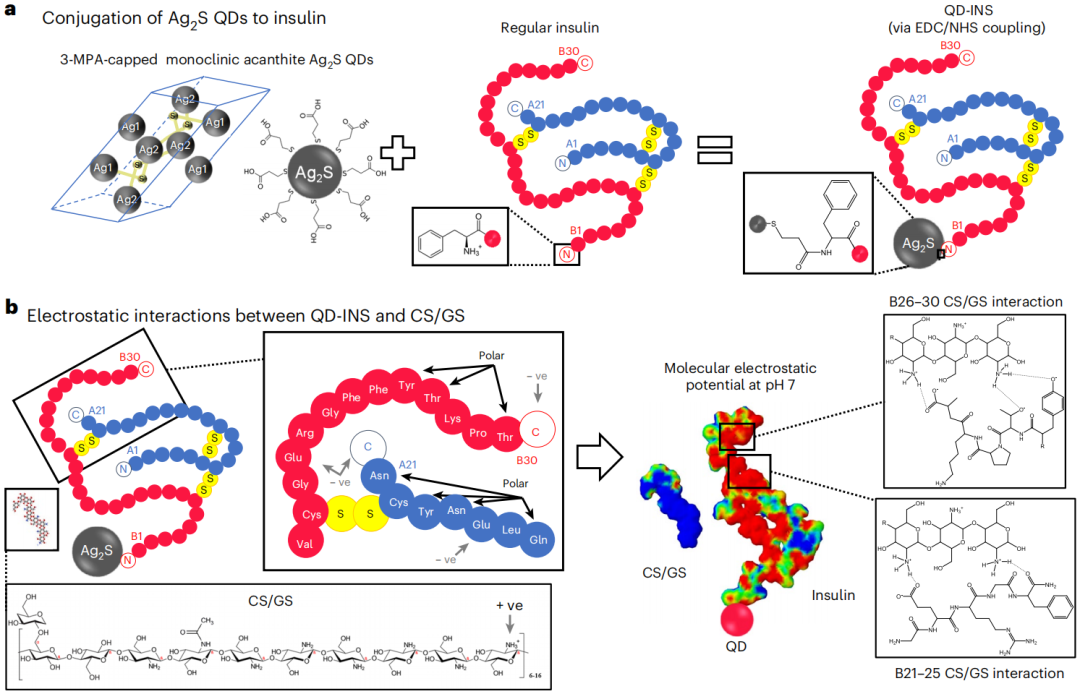
硫化银量子点和CS/GS结合示意
CS/GS对水解酶高度敏感,尤其是β-葡萄糖苷酶,酶解后释放的胰岛素主要为单体形式(87.5%),少量为二聚体(11.5%)和三聚体(<1.0%)。
这些特点帮助这种纳米制剂在口服后不会在胃中被胃酸和消化酶分解,能够顺利到达肝脏,血糖水平高时,葡萄糖苷酶活跃度也高,CS/GS被分解,释放胰岛素,血糖水平低时,胰岛素无法释放,据此,研究人员认为他们的纳米制剂能够在降血糖的同时减少低血糖发生。
带着这些理论,研究人员首先在健康小鼠中进行了实验。他们分别给两组小鼠皮下注射胰岛素(2 IU/kg)和口服胰岛素纳米制剂(20 IU/kg),二者有相似的口服葡萄糖耐量试验结果。
口服胰岛素纳米制剂的生物利用度为4%,给药后半小时,注射胰岛素在血液、肝脏和肌肉/脂肪中的分布分别为40%、40%和20%,口服胰岛素纳米制剂则为20%的肝脏和60%的肠道。
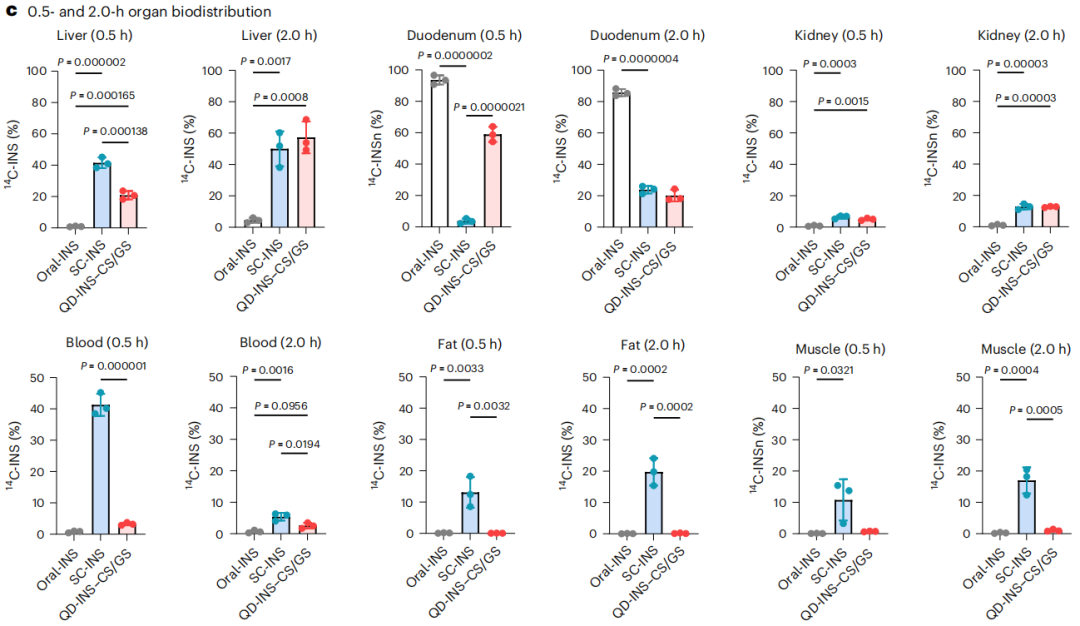
给药0.5小时和2小时后,直接口服胰岛素(灰)、注射胰岛素(蓝)和口服胰岛素纳米制剂(红)在不同器官和组织的分布
5 IU/kg的高剂量皮下注射胰岛素可引起小鼠低血糖,而口服胰岛素纳米制剂300 IU/kg时也不会出现低血糖。禁食小鼠的实验显示,口服胰岛素纳米制剂诱导低血糖所需的最小剂量为500 IU/kg,半数致死剂量为1800 IU/kg,即使长时间(7天)接受100或300 IU/kg的高剂量,也没有出现生化或脂质参数变化、炎症细胞浸润或组织坏死。
在自身免疫或链脲佐菌素(STZ)诱导的两种1型糖尿病小鼠,和STZ诱导的严重1型糖尿病大鼠中,口服胰岛素纳米制剂均诱导了剂量依赖性的血糖下降,没有生化或脂质参数的变化。
为了更加贴近临床,研究人员还在健康的狒狒中进行了实验。口服5和10 IU/kg的胰岛素纳米制剂分别使狒狒的血糖降低了10%和13%,在15-30分钟内可观察到效果。实验后的生化、脂质和血液学参数没有发生偏离标准范围外的变化,也没有出现包括低血糖在内的任何不良事件。
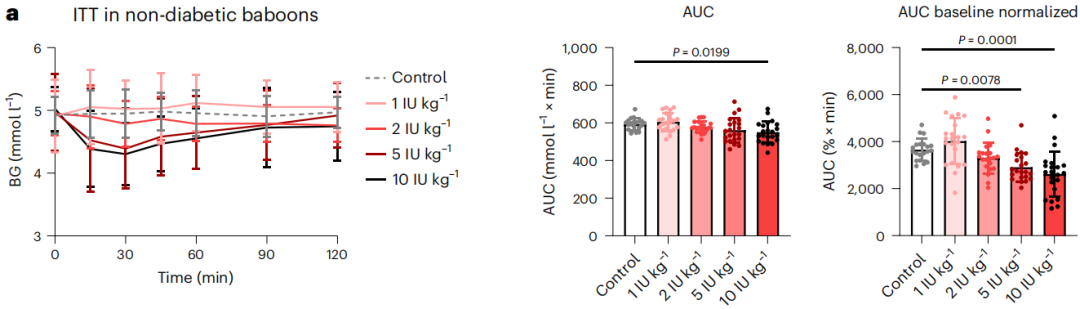
口服不同剂量的胰岛素纳米制剂后,狒狒的血糖下降情况
总的来说,这项研究提供了一种新型口服胰岛素纳米制剂,在小鼠、大鼠和狒狒中显示出剂量依赖性地降低血糖,并且没有出现低血糖等不良事件。除了胰岛素外,他们还希望能将此类纳米技术应用于其他肝脏或特定器官靶向性的药物口服运输,如利拉鲁肽等。
参考文献:
[1] Forouhi N G, Wareham N J. Epidemiology of diabetes[J]. Medicine, 2019, 47(1): 22-27.
[2] DiMeglio L A, Evans-Molina C, Oram R A. Type 1 diabetes[J]. The Lancet, 2018, 391(10138): 2449-2462.
[3] Amiel S A, Aschner P, Childs B, et al. Hypoglycaemia, cardiovascular disease, and mortality in diabetes: epidemiology, pathogenesis, and management[J]. The lancet Diabetes & endocrinology, 2019, 7(5): 385-396.
[4] Pawaskar M, Iglay K, Witt E A, et al. Impact of the severity of hypoglycemia on health-Related quality of life, productivity, resource use, and costs among US patients with type 2 diabetes[J]. Journal of Diabetes and its Complications, 2018, 32(5): 451-457.
[5] Núñez M, Díaz S, Dilla T, et al. Epidemiology, quality of life, and costs associated with hypoglycemia in patients with diabetes in Spain: a systematic literature review[J]. Diabetes Therapy, 2019, 10: 375-392.
[6] Eldor R, Arbit E, Corcos A, et al. Glucose-reducing effect of the ORMD-0801 oral insulin preparation in patients with uncontrolled type 1 diabetes: a pilot study[J]. PloS one, 2013, 8(4): e59524.
[7] Hunt N J, Lockwood G P, Heffernan S J, et al. Oral nanotherapeutic formulation of insulin with reduced episodes of hypoglycaemia[J]. Nature Nanotechnology, 2024: 1-11.
[8] https://www.eurekalert.org/news-releases/1031797
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


