JITC:南京医科大学团队发布肝癌新辅助临床研究成果
来源: 奇点糕 2022-07-12 10:10
据统计,2020年,全球范围内肝癌发病率排在所有恶性肿瘤的第7位,但肝癌相关死亡率却排在第2位,死亡率排名远超发病率,提示肝癌的治疗任重而道远[1]。
据统计,2020年,全球范围内肝癌发病率排在所有恶性肿瘤的第7位,但肝癌相关死亡率却排在第2位,死亡率排名远超发病率,提示肝癌的治疗任重而道远[1]。
肝细胞肝癌(HCC)是肝癌的主要类型,手术切除是重要的治疗手段之一。大约40%的HCC患者在诊断时即为局部晚期(根据中国肝癌分期标准为IIb/IIIa期),按照欧洲和美国肝癌协会标准,这一部分患者已经丧失手术切除机会。
但在中国,对于局部晚期HCC患者,如果符合一定条件可以接受手术切除治疗[2, 3]。不幸的是,大约55%的接受手术切除+术后辅助治疗的HCC患者,在术后中位22个月的时候肿瘤复发。
新辅助治疗可提高多种恶性肿瘤的手术切除率,可能给原本不能切除的恶性肿瘤带来手术的机会,这已成为医学界共识,但在肝癌围手术期系统性治疗(辅助治疗/新辅助治疗)方面,目前很少有相关研究报道。
临床前研究发现,免疫治疗联合抗血管治疗具有协同效应。IMbrave150研究发现阿替利珠单抗联合贝伐珠单抗与索拉非尼单药相比,可以改善不可切除HCC患者无进展生存时间(PFS)和总生存时间(OS)[4]。KEYNOTE-524研究发现帕博利珠单抗联合仑伐替尼在不可切除HCC患者中,可达到46%的客观缓解率(ORR)[5]。
虽然免疫治疗联合抗血管治疗在不可切除HCC患者中获得了一定疗效,但在可切除肝癌方面,目前仅有少数研究报道。比如纳武利尤单抗联合cabozantinib用于局部晚期可切除HCC新辅助治疗,切缘阴性率达80%,主要病理缓解率(MPR)为42%。卡瑞利珠单抗目前已批准用于HCC治疗,阿帕替尼在肝癌中也具有一定的疗效。RESCUE研究发现,两者联合在晚期HCC中达到了34.4%的ORR和5.7个月的中位PFS[6]。
为进一步研究卡瑞利珠单抗联合阿帕替尼在可切除HCC中的的疗效和安全性,南京医科大学第一附属医院夏永祥、王学浩、王平和浦立勇等领衔的研究团队,开展了一项开放标签、单臂、Ⅱ期临床研究[7]。
他们发现,卡瑞利珠单抗联合阿帕替尼在可切除HCC新辅助治疗中,展示出颇有前景的疗效和可控的安全性。研究还发现树突状细胞浸润可作为预测卡瑞利珠单抗联合阿帕替尼新辅助治疗疗效和患者复发的生物标志物,循环肿瘤DNA可作为预测病理缓解及复发的生物标志物。对部分多病灶HCC患者,不同病灶对治疗的敏感性存在差异。异常的糖代谢与不同病灶对于治疗的敏感性相关。
研究者认为小剂量新辅助治疗结合术后辅助治疗对抑制肝癌复发有一定作用,低强度的新辅助治疗后患者病灶病理反应率较低,联合术后辅助治疗对于改善该低病理反应非常必要。这一研究成果发表在著名期刊Journal for ImmunoTherapy of Cancer上。

论文首页截图
在2019年12月至2022年6月期间,这个研究共招募了20名可切除HCC患者。最终只有18名患者入组研究,他们的平均年龄54.7岁,大部分为男性。根据巴塞罗那临床肝癌分期(BCLC),5名(27.8%)患者为B期,13名(72.2%)患者为C期。
这18名患者接受了3个周期的卡瑞利珠单抗+阿帕替尼新辅助治疗,完成治疗后46天,17名患者接受手术治疗,1名患者因肿瘤进展未进行手术。术后4周内,13名患者接受卡瑞利珠单抗+阿帕替尼辅助治疗,其余4名患者未接受辅助治疗(1名患者为肝细胞-胆管细胞混合型肝癌,2名患者未达到R0切除,1名患者因其他原因未接受辅助治疗)。
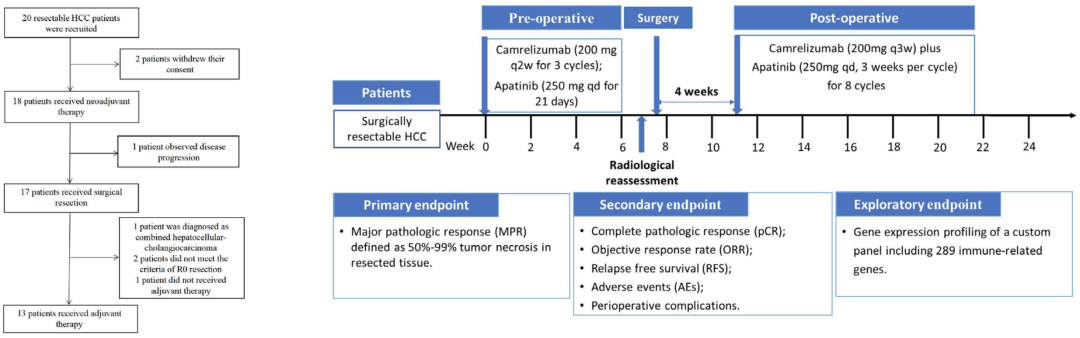
研究流程图及研究终点
研究的主要终点为MPR(定义为肿瘤切除后病理切片显示肿瘤坏死部分达到90%–99%),次要终点为pCR(定义为肿瘤切除后病理切片显示无任何肿瘤残留)。
先来看疗效,18名完成新辅助治疗的患者中,根据RECIST1.1标准,有3名(16.7%)患者达到客观缓解,根据mRECIST1.1标准,有6名(33.3%)患者达到客观缓解。在17名接受手术治疗的患者中,3名(16.7%)患者达到MPR,1名(5.9%)患者达到pCR。在基线甲胎蛋白(AFP)升高的8名患者中,2名患者接受新辅助治疗后,AFP水平显著下降。
安全性方面,18名接受新辅助治疗的患者被纳入安全分析集,16名(88.9%)患者出现了至少一次治疗相关不良事件(TRAE),最常见的TRAE依次为发热,高血压、乳酸脱氢酶水平升高和腹痛。3名(16.7%)患者出现了3级及以上TRAE,最常见的依次为皮疹、高血压、药物性肝损伤、中性粒细胞缺乏症。
13名完成全部治疗的患者接受了随访,结果显示1年的RFS率为53.85%,pCR患者RFS率高于non-pCR患者,但未达统计学显著性差异,单病灶患者RFS率高于多病灶患者,可能因为样本量较小,P值也未达到统计学显著性差异标准。值得一提的是,8名单病灶HCC患者中仅有2名患者出现复发,而其他研究中,未接受新辅助治疗的可切除肝癌患者复发率远高于该研究。
根据患者手术切除标本中肿瘤细胞坏死比例,将患者分为有反应组(R组,定义为肿瘤细胞坏死比例≥50%),和无反应组(NR组,定义为肿瘤细胞坏死比例<50%)。通过对治疗前肿瘤组织中289个免疫相关基因的转录数据分析,研究人员发现,R组与NR组相比,CCL13,MLANA,TNFSF9,IDO1,CD70,IL12RB2,CD19和IL4基因转录水平升高,而HILA-DQ1和GUSB基因的转录水平降低。
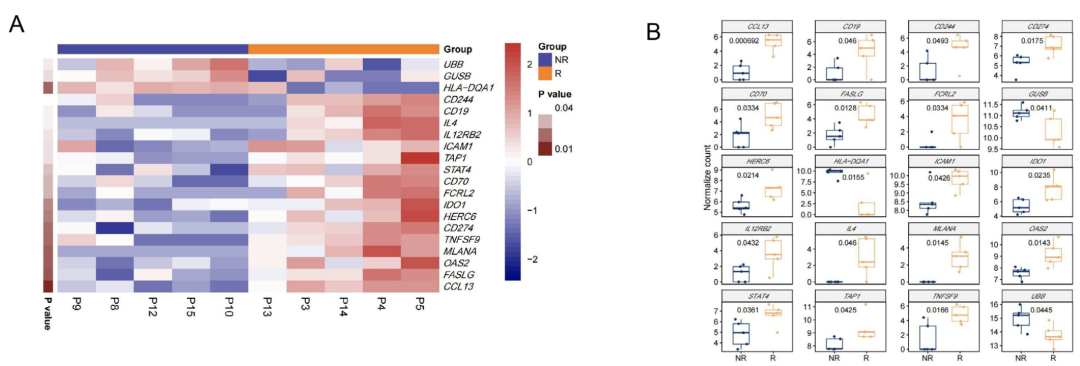
免疫相关基因转录水平和新辅助治疗疗效的关系
随后,研究人员分析了肿瘤微环境免疫细胞浸润分数,他们发现,R组免疫细胞浸润得分更高,特别是树突状细胞得分显著高于NR组,提示树突状细胞浸润水平可作为HCC新辅助治疗疗效生物标志物。
此外,研究人员还发现R0切除患者较R1切除患者,ctDNA阳性率明显降低。ctDNA阳性患者RFS较ctDNA阴性的患者显著缩短。患者接受辅助治疗后,ctDNA显著下降患者RFS长于ctDNA没有明显下降患者。
根据不同病灶对新辅助治疗的反应,研究人员还将肿瘤分为R病灶和NR病灶(R病灶定义为肿瘤细胞坏死比例≥50%的肿瘤病灶。NR病灶定义为肿瘤细胞坏死比例<50%的肿瘤病灶)。通过对R病灶和NR病灶蛋白组学进行分析,他们发现NR病灶中,PCBD1,TPI1,C1QA,FLAD1蛋白表达显著升高,而R病灶中,FASN,TCP1,PKM蛋白表达显著升高。通过KEGG通路富集分析发现,这些表达改变的蛋白显著富集到“糖酵解”和“甘露糖代谢”通路。

R病灶和NR病灶蛋白组学差异
最后,研究者认为本研究为小样本Ⅱ期临床研究,存在一定的局限性,且研究的随访时间仅1年,研究中治疗的选择需要依据临床经验进行调整和改进。基于患者标本的RNA水平、DNA水平、蛋白水平等数据,初步探索了新辅助治疗耐药的原因,但是目前研究尚较表浅,需要更深入研究探索其机制。
总的来说,卡瑞利珠单抗联合阿帕替尼在可切除HCC新辅助治疗中,展示出颇有前景的疗效,且安全性可控。
参考文献:
1, Sung H, Ferlay J, Siegel RL, et al. Global cancer statistics 2020: GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries. CA Cancer J Clin 2021;71:209–49.
2, Marrero JA, Kulik LM, Sirlin CB, et al. Diagnosis, staging, and management of hepatocellular carcinoma: 2018 practice guidance by the American association for the study of liver diseases. Hepatology 2018;68:723–50.
3, Zhou J, Sun H-C, Wang Z, et al. Guidelines for diagnosis and treatment of primary liver cancer in China (2017 edition). Liver Cancer 2018;7:235–60.
4, Qin S, Ren Z, Feng Y-H, et al. Atezolizumab plus bevacizumab versus sorafenib in the Chinese subpopulation with unresectable hepatocellular carcinoma: phase 3 randomized, open-label IMbrave150 study. Liver Cancer 2021;10:296–308.
5, Finn RS, Ikeda M, Zhu AX, et al. Phase Ib study of Lenvatinib plus pembrolizumab in patients with unresectable hepatocellular carcinoma. J Clin Oncol 2020;38:2960–70.
6, Xu J, Shen J, Gu S, et al. Camrelizumab in combination with apatinib in patients with advanced hepatocellular carcinoma (RESCUE): a nonrandomized, open-label, phase II trial. Clin Cancer Res 2021;27:1003–11.
7, Xia Y, Tang W, Qian X, et al.Efficacy and safety of camrelizumab plus apatinib during the perioperative period in resectable hepatocellular carcinoma: a single-arm, open label, phase II clinical trialJournal for ImmunoTherapy of Cancer 2022;10:e004656. doi: 10.1136/jitc-2022-004656.
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


