Science:深度对比学习使全基因组虚拟筛选成为可能
来源:生物谷原创 2026-01-27 11:45
DrugCLIP 是一种超高速虚拟筛选方法,研究者们通过计算机基准评估和湿实验室实验对其进行了严格验证。
人类可成药基因组中仍有相当一部分未被小分子药物靶向。随着AlphaFold等蛋白质结构预测技术的发展,全基因组范围的药物发现已成为一个更可实现的目标。然而,目前使用的虚拟筛选工具远不能满足这一需求。现有方法,无论是经典的分子对接还是深度学习方法,计算成本都过高,无法覆盖全基因组范围的靶点。为了解决这个问题,他们们的目标是开发一种有效的全基因组虚拟筛选方法,能够快速识别人体基因组中每个可成药靶点的小分子配体。

在一项新的研究中,他们国研究人员开发了DrugCLIP,这是一个用于快速、准确虚拟筛选的对比学习框架。DrugCLIP将蛋白质口袋和小分子编码到一个共享的潜空间中,并使用大规模合成数据和实验确定的蛋白质-配体复合物结构进行训练。然后,可以像现代搜索引擎一样,利用密集检索技术,用蛋白质靶点快速查询大型化合物库。为了促进其对AlphaFold预测结构的适用性,他们们开发了GenPack,一个生成式口袋优化模块,可以提高口袋检测的精度。他们使用基准数据集和湿实验室实验验证了DrugCLIP。为了进一步展示其潜力,他们们进行了一项全基因组虚拟筛选活动,并将所有结果公开。
在DUD-E和LIT-PCBA这两个广泛使用的虚拟筛选基准数据集上,DrugCLIP在速度和准确性方面均优于传统分子对接和最先进的深度学习基线。它还表现出跨化学支架和蛋白质家族的强大泛化能力,以及对结构扰动的鲁棒性。
在实验验证中,DrugCLIP为5-羟色胺2A受体(5HT2AR)和去甲肾上腺素转运蛋白这两个精神疾病的关键靶点鉴定出了高效力的配体。两个5HT2AR激动剂的半数有效浓度值低于100 nM,两个NET抑制剂的结构通过冷冻电镜得到了验证。
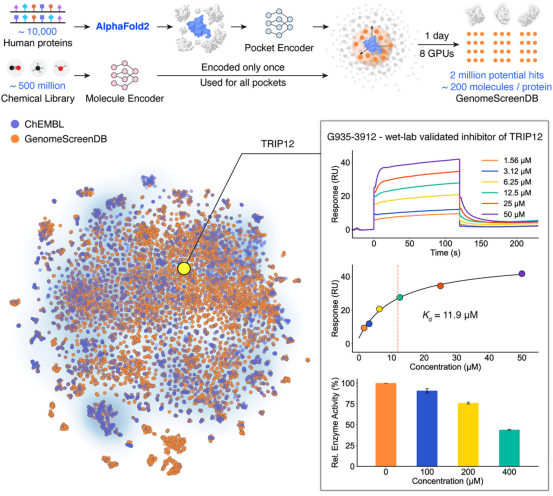
当与GenPack结合时,DrugCLIP在具有挑战性的apo结构和AlphaFold预测结构上的表现显著优于分子对接和诱导契合对接。DrugCLIP和GenPack成功为研究较少的靶点甲状腺激素受体相互作用蛋白12 鉴定出了小分子抑制剂,该靶点目前没有已报道的holo结构或配体。该模型在表面等离子共振实验中的命中率达到17.5%,其中两个抑制剂被进一步证实具有酶抑制活性。
最后,他们们将DrugCLIP应用于针对约10,000个人类蛋白质与5亿种化合物的全基因组虚拟筛选,仅使用八个图形处理单元,在24小时内完成了对超过10万亿个蛋白质-配体对的评分。这次筛选产生了超过200万个候选分子,覆盖了约20,000个口袋,代表了大约一半的人类基因组。所有筛选数据均已公开,以支持药物发现领域的广泛应用。
综上所述,DrugCLIP 是一种超高速虚拟筛选方法,他们通过计算机基准评估和湿实验室实验对其进行了严格验证。其速度使得能够进行覆盖人类可成药蛋白质组的万亿级筛选,提供了一个开放获取的资源,为下一代药物发现(特别是针对了解较少的靶点)奠定了基础。(生物谷Bioon.com)
参考文献:
Yinjun Jia et al, Deep contrastive learning enables genome-wide virtual screening, Science (2026). DOI: 10.1126/science.ads9530.
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


