肠道干细胞研究进展(第4期)
来源:生物谷原创 2026-01-30 09:38
从分子的角度来看,肠道是一个嘈杂的地方,各种人类细胞和微生物细胞彼此之间相互沟通,从而维持一种稳健而又健康的细胞群落。这个细胞群落的关键是肠道干细胞(intestinal stem cell),它们产生多种细胞类型,从而有助于保持肠道功能正常。肠道干细胞位于肠黏膜隐窝基底部,即基底隐窝是肠道干细胞的细胞库。正常情况下,位于隐窝基底部的肠道干细胞不断向隐窝顶部(肠腔方向)迁移,整个迁移过程大约3至5天,在迁移过程中肠道干细胞分化形成不同的肠粘膜细胞。
针对肠道干细胞研究近期取得的进展,小编进行了一番盘点,以飨读者。
1.Adv Mater:定制的无异种聚合物表面促进肠道干细胞的动态迁移
doi: 10.1002/adma.202513371
来源于患者自身细胞的肠道干细胞(Intestinal Stem Cell, ISC)因其低排斥风险,作为治疗难治性肠道疾病的新替代方案备受关注。然而,传统的培养方法依赖动物源性成分(异种成分),由此引发的安全性和监管问题限制了其临床应用。
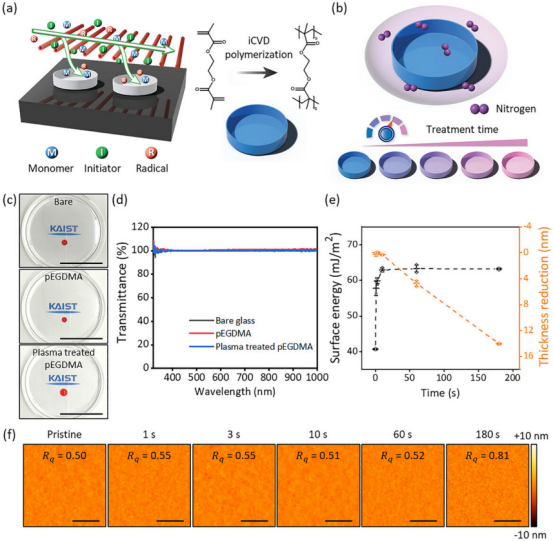
由KAIST化学与生物分子工程系的Sung Gap Im教授、韩国标准科学研究院纳米生物测量组的Tae Geol Lee博士以及韩国生命工学研究院干细胞融合研究中心的Mi-Young Son博士共同领导的研究团队,开发了一种基于聚合物的培养平台,该平台在无异种成分的环境中显著改善了ISC的迁移和再生能力。该研究成果发表在《Advanced Materials》上。
为了克服干细胞疗法临床应用中的障碍——例如使用小鼠成纤维细胞或基质胶等物质时存在病毒传播给患者的风险——该联合研究团队开发了PLUS。这种基于聚合物的培养表面技术无需任何动物源性材料即可有效运作。
PLUS是一种通过气相沉积方法涂覆的合成聚合物表面。通过精确控制表面能和化学成分,它显著增强了ISC的粘附和大量培养效率。值得注意的是,即使在室温下储存三年后,它仍能保持完全相同的培养性能,确保了干细胞疗法的工业可扩展性和储存便利性。
通过蛋白质组学分析,研究团队发现,在PLUS环境下培养的ISC中,与细胞骨架重组相关的蛋白质表达显著增加。具体来说,团队确认了细胞骨架结合蛋白和肌动蛋白结合蛋白表达的增加,导致了细胞内结构的稳定重组。这为干细胞在基质上更快、更积极地移动提供了动力源。
2.EMBO Mol Med:罕见基因突变有望揭示肠道干细胞的再生奥秘
DOI:10.1038/s44321-025-00295-3
在医学领域,罕见病的研究一直是科学探索的前沿热点,目前全球大约有7000多种罕见病,影响着全球约3.5亿人的健康;其中,一种名为透明纤维瘤综合征(HFS,Hyaline Fibromatosis Syndrome)的罕见遗传性疾病,因其在婴儿期可能导致致命性腹泻而备受关注,HFS是由毛细血管生成基因2(CMG2)的功能丧失型突变所引起,但CMG2在肠道中的具体作用一直未被充分研究。
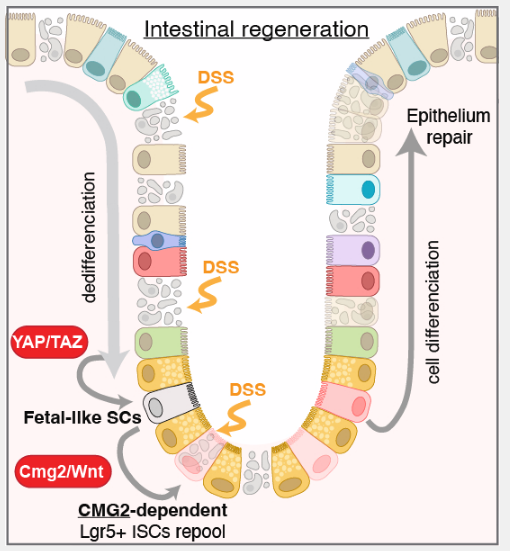
日前,一篇发表在国际杂志EMBO Molecular Medicine上题为“Injury-induced intestinal stem cell renewal requires capillary morphogenesis gene 2”的研究报告中,来自瑞士洛桑联邦理工学院等机构的科学家们通过对小鼠模型进行研究,揭示了CMG2在肠道干细胞再生中的关键作用,为理解HFS的致病机制和开发新疗法提供了重要线索。
文章中,研究人员通过构建CMG2基因敲除(knockout)小鼠模型模拟了HFS患者的肠道环境,结果发现,CMG2在肠道损伤后的再生过程中发挥着至关重要的作用,在正常情况下,CMG2基因敲除小鼠的肠道形态和功能与正常小鼠无异;然而,当研究人员通过化学诱导剂引发结肠炎后,CMG2基因敲除小鼠的肠道则无法正常再生,从而就会导致肠道干细胞池无法得到补充,这一发现不仅解释了HFS患者中严重的肠道症状,还为理解肠道干细胞的再生机制提供了新的视角。
研究人员表示,CMG2基因敲除小鼠在经历肠道损伤后,无法像正常小鼠那样恢复肠道功能,这就表明,CMG2在肠道干细胞再生过程中起着不可或缺的作用。进一步研究后,研究人员揭示了CMG2通过调节Wnt信号通路中的β-catenin蛋白的核转位来控制干细胞的再生。在CMG2基因敲除小鼠中,β-catenin无法进入细胞核激活干细胞相关基因,从而就会导致干细胞再生受阻。
3.Nature:肠道干细胞的“能量密码”,揭秘α-酮戊二酸如何决定细胞命运
doi:10.1038/s41586-025-09097-6
在生物医学研究领域,细胞代谢与干细胞命运的联系正逐渐成为前沿热点。过去,我们常常认为细胞的命运是由基因和信号通路决定的,而代谢过程只是为细胞活动提供能量。然而,越来越多的研究表明,代谢产物本身也可能直接调控细胞的命运。
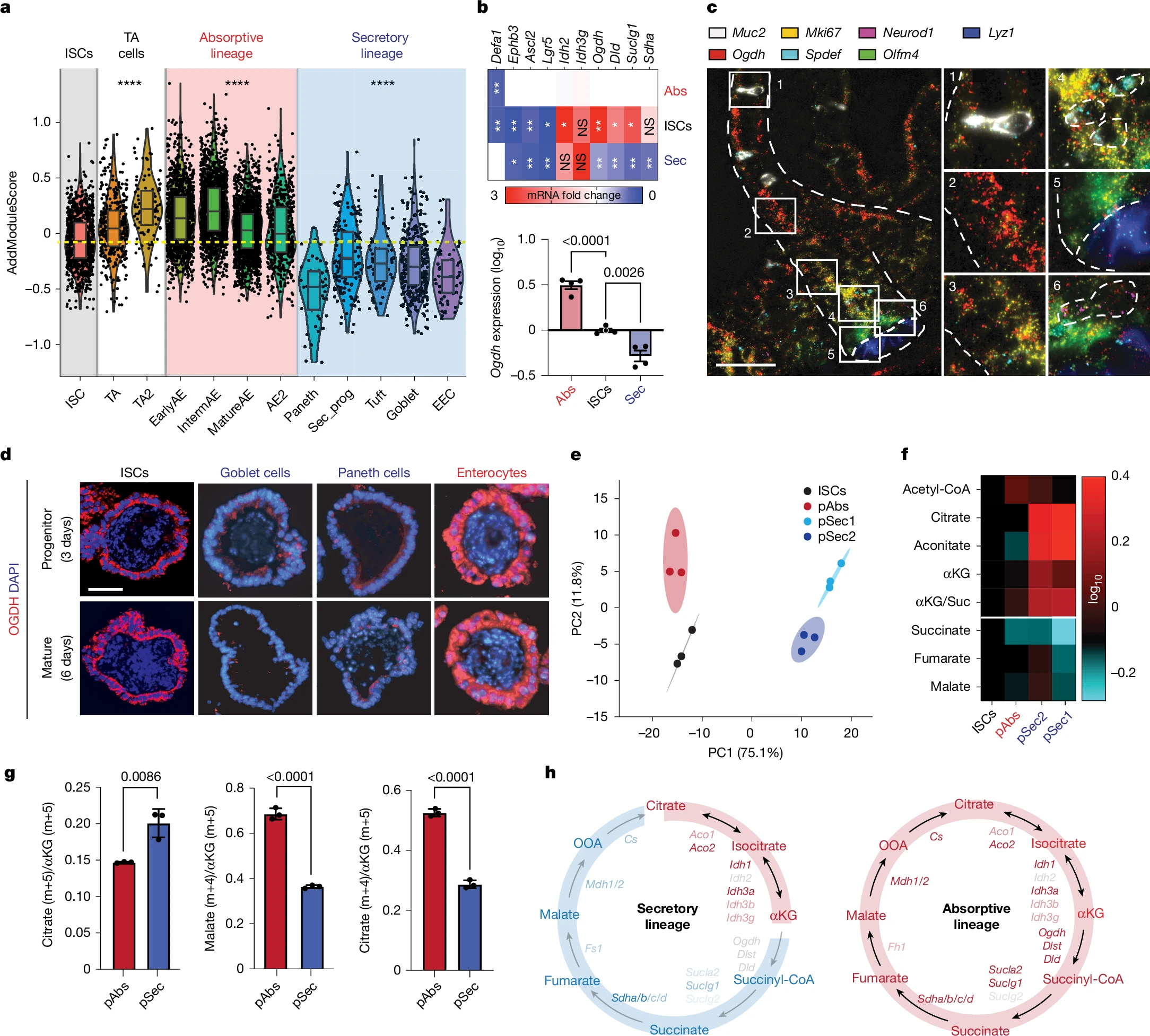
近日,一篇发表在国际杂志Nature上题为“Metabolic adaptations direct cell fate during tissue regeneration”的研究报告中,来自纪念斯隆-凯特琳癌症中心等机构的科学家们通过研究揭示了α-酮戊二酸或能通过调控肠道干细胞的命运从而影响肠道的再生和修复。
研究者表示,作为一种关键的代谢产物,α-酮戊二酸(α-KG)能决定肠道干细胞分化为吸收性细胞还是分泌性细胞,这一发现不仅改变了科学家们对细胞代谢的传统认识,还为治疗肠道疾病提供了新的思路。研究者指出,作为细胞的能量工厂,线粒体负责通过分解蛋白质、脂肪和碳水化合物来生成携带能量的ATP分子,然而,随着研究的深入,科学家们逐渐意识到,线粒体在细胞功能和命运调控中扮演着更为复杂的角色;特别是,线粒体中的代谢产物,如α-酮戊二酸(α-KG),在细胞分化过程中可能具有重要的信号传导功能。这项研究正是基于这一背景探索了α-KG如何影响肠道干细胞的命运。
研究人员首先观察了人类和小鼠肠道细胞中三羧酸循环(TCA cycle)酶的表达差异,他们发现,吸收性细胞中2-氧代戊二酸脱氢酶(OGDH)的表达水平较高,而分泌性细胞中该酶的表达较低。OGDH负责将α-KG转化为琥珀酰辅酶A(succinyl-CoA)。通过遗传和药理学方法,研究者们进一步证实了OGDH的差异表达如何通过代谢途径影响肠道干细胞的命运。
4.为何说吸烟是“隐形杀手”?eLife揭秘尼古丁驱动肠道干细胞癌变新机制,DBZ或带来治疗新曙光
doi:10.7554/eLife.95267
在日常生活中,吸烟的危害如影随形,时刻威胁着人们的健康。那袅袅升起的烟雾中,隐藏着诸多致病因子,而尼古丁作为香烟的关键成分,更是备受瞩目。你是否想过,它在进入人体后,会在我们的肠道深处悄然引发怎样的“蝴蝶效应”呢?近期Elife的一项重磅研究Nicotine enhances the stemness and tumorigenicity in intestinal stem cells via Hippo-YAP/TAZ and Notch signal pathway聚焦尼古丁对肠道干细胞的影响,为肠道肿瘤的防治开辟了新的视角。

该研究以小鼠为实验模型,采用了体内外相结合的研究方法。在体内实验中,让小鼠长期饮用含200 μg/ml尼古丁的水,模拟吸烟状态。结果显示,尼古丁处理后,小鼠小肠绒毛长度缩短,但隐窝大小基本不变,同时肠道内分化细胞数量减少。进一步检测发现,小肠和大肠中Ki67阳性细胞显著增多,这表明细胞增殖活性增强。增殖性Olfm4阳性肠道干细胞在小肠中的数量也明显上升,且在特定基因标记的小鼠模型中,Lgr5+结肠干细胞数量增加,而Paneth细胞数量无明显改变。
体外实验则对小鼠肠道隐窝进行培养研究。当在培养体系中添加不同浓度尼古丁时,100 nM、1 µM、10 µM的尼古丁均能促进小肠隐窝形成类器官,1 µM尼古丁对结肠隐窝类器官形成也有积极作用。在将ISCs和Paneth细胞共同培养并添加诱导剂的实验里,来自尼古丁处理小鼠的ISCs形成的类器官集落数量远超对照组,且单独培养ISCs并添加尼古丁时同样能刺激类器官形成,而Paneth细胞在尼古丁处理与否的情况下,其功能无显著差异。
5.Science:揭示PIEZO离子通道依赖的机械传感对肠道干细胞的命运决定和维持至关重要
doi:10.1126/science.adj7615
在一项新的研究中,来自多伦多病童医院和居里研究所的研究人员揭示了肠道干细胞如何感知环境并做出反应,对炎症性肠病和结直肠癌具有重要意义。相关研究结果发表在2024年11月29日的Science期刊上,论文标题为“PIEZO-dependent mechanosensing is essential for intestinal stem cell fate decision and maintenance”。
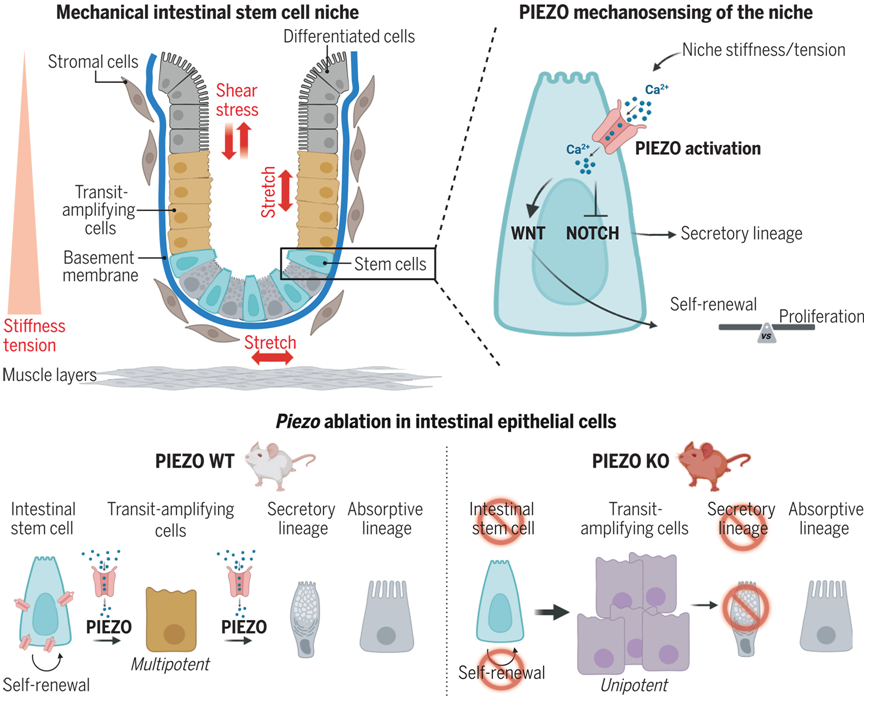
肠道干细胞在化学信号和物理力量的作用下,不断适应环境,以维持器官和组织的健康。如果肠道干细胞不能发挥预期功能,就会导致一系列健康问题,包括炎症性肠病(IBD)和结直肠癌。
迄今为止,肠道干细胞如何感知周围的物理力量仍不清楚,但由多伦多病童医院前博士后研究员Meryem Baghdadi博士、Tae-Hee Kim博士和居里研究所的Danijela Vignjevic博士领导的一个研究团队在这项新的研究中发现揭示,肠道干细胞的生存依赖于两个离子通道,即PIEZO1和PIEZO2。
Kim解释说,“肠道干细胞周围环境的物理特性对我们的健康至关重要。有了这些知识,我们就能探索促进胃肠道再生的方法,不仅能预防,还能修复受损的肠道干细胞。”
6.Science子刊:揭示Daam1在调节肠道干细胞分化为潘氏细胞中起着关键作用
doi:10.1126/sciadv.adh9673
干细胞可以分化为新的细胞来取代死亡和受损的细胞。但在特定情况下,干细胞如何决定成为哪种类型的细胞?在一项新的研究中,来自奥地利科学院分子生物技术研究所和韩国基础科学研究院等研究机构的研究人员利用肠道类器官(intestinal organoids),发现了一个称为Daam1的新基因,它在肠道分泌细胞的发育过程中起着至关重要的作用。这一发现为癌症研究开辟了新的视角。相关研究结果发表在2023年11月24日的Science Advances期刊上,论文标题为“Intestinal Paneth cell differentiation relies on asymmetric regulation of Wnt signaling by Daam1/2”。
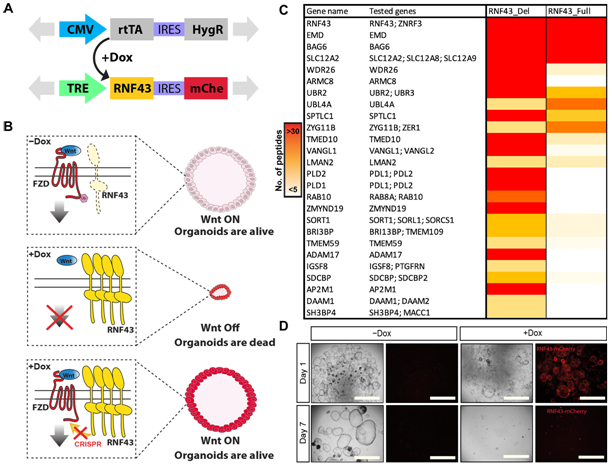
我们的身体在某些方面就像汽车一样,需要定期检查和修理才能保持正常运转。就我们的身体而言,任何受损或死亡的细胞都需要被替换,以保持器官的功能。这种替换要归功于组织驻留的成体干细胞。
胚胎干细胞可以在体内形成任何细胞类型,与之相比,成体干细胞只会形成其所属组织中的细胞类型。但是,组织特异性干细胞如何知道要产生哪种细胞类型呢?这些作者决定利用肠道干细胞研究这个问题。
论文共同第一作者、奥地利科学院分子生物技术研究所Bon-Kyoung Koo实验室博士后研究员Gabriele Colozza解释说,“在我们的肠道中,细胞暴露在极端条件下。”机械磨损、消化酶和不同的pH值都会影响肠道细胞。反过来,肠粘膜中的干细胞会通过分化形成新的肠道细胞。
“受损细胞必须被替换,但干细胞自我更新和分化成其他细胞类型之间存在着微妙的平衡:干细胞不受控制地增殖可能会导致肿瘤的形成;另一方面,如果过多的干细胞发生分化,组织中的干细胞就会枯竭,最终无法自我更新。”
这种平衡通过信号传导通路和反馈回路进行微妙调整,从而使细胞能够相互沟通。其中一种重要的信号传导通路叫做Wnt。Wnt通路因其在胚胎发育中的作用而闻名,如果不加以控制,过度活跃的Wnt通路会导致细胞过度分裂并形成肿瘤。
7.Science:确定ZNF800是肠道干细胞分化为肠内分泌细胞的主抑制因子
doi:10.1126/science.adi2246
人类肠道的不同细胞类型是由肠道干细胞通过分化过程发育而成的。在一项新的研究中,来自荷兰胡布勒支研究所、马克西玛公主儿科肿瘤中心和马斯特里赫特大学的研究人员利用肠道类器官(gut organoids)对1800种人类转录因子进行了系统性CRISPR筛选,发现ZNF800是特定肠道细胞类型---肠内分泌细胞(enteroendocrine cell)---分化的关键调节因子。这一发现可能会对我们了解胃肠道疾病、胃肠道内分泌失调以及胰腺发育和糖尿病产生影响。相关研究结果发表在2023年10月27日的Science期刊上,论文标题为“Unbiased transcription factor CRISPR screen identifies ZNF800 as master repressor of enteroendocrine differentiation”。

人类肠道中含有多种细胞类型,每种细胞类型都有特定的功能。这些细胞类型都来自肠道干细胞。肠道干细胞尚未发生特化,但有潜力成为功能上特化的肠道细胞。
肠道的重要细胞类型包括负责吸收营养的肠上皮细胞(enterocyte)、产生粘液的杯状细胞(goblet cell)、分泌抗菌肽的潘氏细胞(Paneth cell)以及产生多种激素的肠内分泌细胞。肠内分泌细胞分泌的激素能调节消化过程,如营养物吸收、食欲和葡萄糖代谢。
在这项新的研究中,这些作者研究了肠道干细胞如何通过一种称为分化的过程变成肠内分泌细胞。为此,他们使用了肠道类器官:实验室培育的微型器官,可模拟实际肠道的结构和功能。
这些作者利用CRISPR对人类转录因子的全部序列(包括1800个基因)进行了系统筛选,以找到参与肠道干细胞分化成肠内分泌细胞的转录因子。
Lin说,“通过筛选所有可能的‘交通信号灯’,我们确定了在控制细胞命运决定中起关键作用的特定转录因子。其中的一些转录因子像绿灯一样,促进基因的激活,从而引导细胞走向特定的命运,而另一些转录因子则像红灯一样,抑制某些基因的表达,使细胞走上不同的道路。”
这些作者发现,ZNF800是决定肠道中肠内分泌细胞和其他细胞类型之间平衡的关键转录因子。Lin解释说,“ZNF800的存在对肠内分泌细胞的产生起到了红灯的作用:当我们关闭ZNF800红灯时,我们看到肠道类器官中的肠内分泌细胞显著增加了10倍。与此同时,诸如杯状细胞和潘氏细胞之类的其他肠道细胞类型受到抑制。”
8.JEM:我国科学家揭示氟马西尼有望让肠道干细胞免受放化疗的毒副作用
doi:10.1084/jem.20220541
在一项新的研究中,来自中国山东大学、中国医学科学院北京协和医学院、中山大学和四川大学的研究人员发现,抑制一种名为GABAA受体的蛋白可以保护肠道干细胞免受化疗和放疗的毒性影响。他们指出作为一种美国食品药品管理局(FDA)批准的抗镇静剂,靶向作用于GABAA受体的氟马西尼(flumazenil)可减轻许多癌症治疗所引起的一些常见的胃肠道副作用,如腹泻和呕吐。
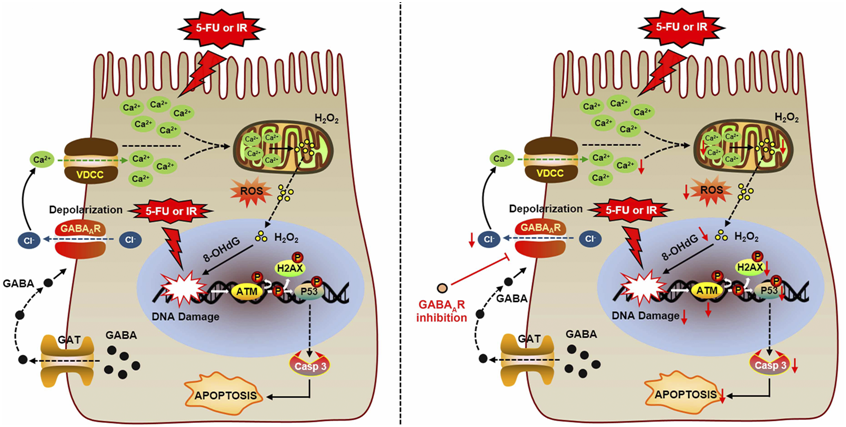
相关研究结果于2022年9月20日发表在Journal of Experimental Medicine期刊上,论文标题为“Inhibition of GABAA receptors in intestinal stem cells prevents chemoradiotherapy-induced intestinal toxicity”。论文通讯作者为山东大学临床医学院的陈达威(Dawei Chen)博士和山东大学齐鲁医学院的李景新(Jingxin Li)教授。
由于肠道干细胞必须不断地增殖和替换肠道壁内的细胞,因此它们对化疗和放疗高度敏感。这些治疗方法损害了肠道干细胞的DNA,并导致它们死亡,从而导致肠道损伤和多种痛苦的胃肠道症状。这些毒副作用,在治疗结束后会持续很长时间,限制了癌症患者的化疗药物或放疗剂量,并使他们的生活质量恶化。
这些作者发现,在接受放疗或化疗药物治疗的小鼠的肠道干细胞中,一种名为GABRA1的蛋白水平增加了。GABRA1是GABAA受体的一个组成部分,GABAA受体以它在神经系统中的作用而闻名,在那里它与神经递质γ-氨基丁酸(GABA)结合。但是GABA和GABAA受体也存在于整个身体的其他组织中。
他们发现,抑制GABAA受体可以保护小鼠免受化疗或放疗的毒副作用,减少DNA损伤量,增加肠道干细胞的存活率。这使得这些小鼠能够维持正常的肠道内壁,并在致命剂量的放疗或化疗药物治疗后存活。
这些作者发现抑制GABAA受体可以通过限制放化疗(chemoradiotherapy)中自由基的形成来保护肠干细胞免受DNA损伤。然而,至关重要的是,他们确定抑制GABAA受体并不能阻止放疗或化疗药物杀死癌细胞。(生物谷Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


