鼻腔类器官拆解感冒轻重密码!耶鲁研究:干扰素反应是胜负关键,失衡则触发炎症风暴
来源:生物谷原创 2026-01-27 13:30
来自耶鲁大学医学院等机构的科学家们通过研究提出了一个颠覆性的见解:真正决定你感冒轻重与否的,可能不是你接触的病毒有多“毒”,而是你鼻子里的细胞如何“应战”。

鼻病毒是普通感冒最常见的元凶,成年人平均每年会遭遇 2-4 次感冒,儿童则可能高达 6-8 次。对大多数人来说,这只是个烦人的小插曲,流几天鼻涕、打几个喷嚏就过去了。然而,对于吸烟者、哮喘患者等高危人群,鼻病毒感染却可能导致严重的呼吸道窘迫,甚至诱发哮喘急性发作。为什么同一种病毒在不同人身上会导致差异如此巨大的结果?
长期以来,科学家们一直在寻找答案。传统观点往往聚焦于病毒本身的特性,但近日,一篇发表在国际杂志《Cell Press Blue》上的研究报告中,来自耶鲁大学医学院等机构的科学家们提出了一个颠覆性的见解:真正决定你感冒轻重与否的,可能不是你接触的病毒有多 “毒”,而是你鼻子里的细胞如何 “应战”。
文章中,研究人员利用实验室培育的人鼻腔类器官模型,结合单细胞测序技术,首次在微观层面实时观测了鼻腔细胞与鼻病毒交锋的全过程,揭示了决定感染结局的关键分子机制——干扰素反应的强弱平衡,直接主导了是轻微感冒还是严重炎症的不同走向。

鼻病毒是普通感冒最常见的病因,也是高危人群呼吸窘迫的主要原因,但导致广泛感染结局的分子机制长期未被完全阐明。要深入探究人体对鼻病毒的防御机制,传统研究方法存在明显局限:常用的单一细胞系无法模拟真实鼻腔中基底细胞、分泌细胞、纤毛细胞等多种细胞类型协同作战的复杂环境,而鼻病毒通常只感染人类,动物模型难以复刻人体真实反应。
为此,研究人员开创性地在实验室里培育出了 “人鼻腔上皮类器官”——他们将人类鼻腔干细胞在空气 - 液体界面的模拟体内环境中培养 28 天,最终得到了一个包含多种功能细胞的微型组织模型,不仅有产生黏液的分泌细胞和具有清扫功能的纤毛细胞,还能精准重现人体鼻腔的生理结构和免疫反应。这个栩栩如生的 “迷你鼻子” 成为了完美的实验平台,研究人员得以同时观察成千上万个细胞的协同反应,并通过干扰特定的细胞感应通路,测试防御机制的动态变化。
研究人员揭示了一套精密的防御体系:当鼻病毒入侵时,鼻腔上皮细胞能迅速通过模式识别受体感知病毒 RNA,启动核心防御机制——干扰素反应。干扰素是一类信号蛋白,堪称免疫系统的 “警报器” 和 “动员令”:感染病毒的细胞会分泌以 III 型干扰素为主的信号分子,它不仅能在被感染的细胞内部启动抗病毒程序,诱导干扰素刺激基因(ISG)表达,制造不利于病毒复制的环境,还能 “通知” 邻近的未感染细胞提前进入戒备状态。
研究人员发现,在完整的人鼻腔上皮中,鼻病毒主要诱导的就是这种高效的干扰素反应,正是这个迅速启动的防御网络,能成功将病毒感染限制在不到 2% 的细胞中,有效遏制病毒扩散。即便没有免疫细胞参与,快速启动的干扰素反应就足以控制鼻病毒感染,凸显了其作为 “第一道防线” 的关键作用。
然而,当研究人员在实验中人为抑制干扰素反应(通过阻断 TBK1 激酶抑制 IRF3 激活)时,战局急转直下。病毒复制彻底失控,感染范围从不足 2% 飙升至 30% 以上,不仅感染原本主要受攻击的纤毛细胞,还扩散到基底细胞和分泌细胞。
更严重的是,病毒失控复制触发了一个更具破坏性的次级反应——以核因子 κB(NF-κB)和 NLRP1 炎性小体通路为核心的促炎反应被过度激活。鼻病毒的 3C 蛋白酶会直接切割并激活 NLRP1 炎性小体,导致白细胞介素-1β 等炎性因子大量释放,而白细胞介素-1β 又会通过受体形成正反馈,进一步放大炎症反应和黏液过度分泌,形成 “炎症风暴”,这正是鼻塞、咳嗽、呼吸困难等严重症状的核心成因。值得注意的是,NF-κB 不仅是促炎反应的关键开关,还是干扰素反应的必要共调节因子,其功能失衡会同时加剧病毒复制和炎症损伤。
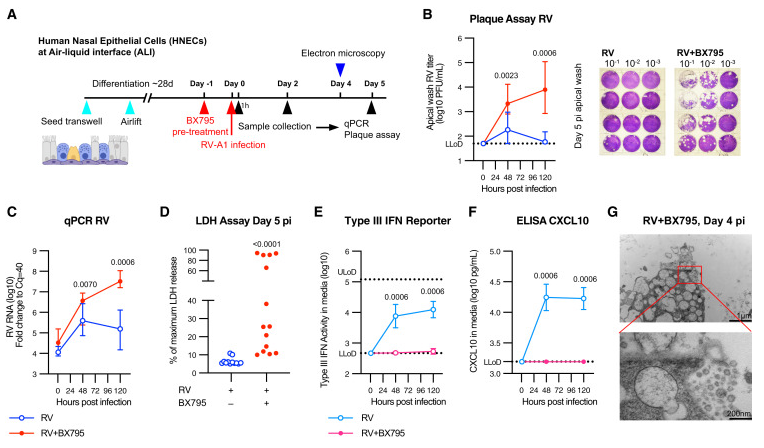
干扰素应答限制鼻病毒在分化型人鼻上皮中的复制
这一发现为理解感冒症状的个体差异提供了全新视角:症状的严重程度并非直接由病毒载量决定,而是由宿主免疫反应的平衡性主导。在健康个体中,迅速且适度的干扰素反应能有效控制病毒,炎症反应温和,症状轻微;而在某些高危人群中(如呼吸道屏障功能受损者),或当干扰素反应因遗传、环境因素(如空气污染、过敏原)或合并感染被延迟或削弱时,病毒得以复制扩散,进而触发过度的促炎和黏液分泌反应,导致症状恶化。研究还通过 CRISPR 敲除 NLRP1 基因的类器官实验证实,阻断 NLRP1 通路能显著减少白细胞介素-1β 释放和中性粒细胞趋化因子分泌,进一步验证了这一机制的关键作用。
这项研究不仅增进了我们对普通感冒这一常见病的科学理解,更重要的是为开发新的治疗策略指明了方向。既然过度的炎症反应是导致症状恶化的关键,未来药物开发的思路或许可以从传统的 “抗病毒” 转向 “调节免疫”。例如,针对 NLRP1 炎性小体、白细胞介素-1 受体或鼻病毒 3C 蛋白酶开发抑制剂,或在感染早期增强局部 III 型干扰素反应,可能有助于减轻高危人群的严重症状,避免哮喘急性发作等并发症。此前在临床试验中效果有限的 3C 蛋白酶抑制剂鲁平曲韦,也可能通过阻断 NLRP1 激活,重新成为治疗病毒诱导呼吸道炎症的候选药物。
当然,研究人员也指出,人体内的真实情况更为复杂:鼻腔类器官模型虽然先进,但仍缺少免疫细胞、肠道菌群等其他参与防御的因素,且完全抑制干扰素反应属于极端情况,体内通常是部分减弱。下一步,研究人员将会探索免疫细胞、环境污染物、气道菌群等因素如何共同调节机体对鼻病毒的反应,让研究结果更贴近临床实际。(生物谷Bioon.com)
参考文献:
Bao Wang,Julien A.R. Amat,Valia T. Mihaylova,et al. Rhinovirus triggers distinct host responses through differential engagement of epithelial innate immune signaling. Cell Press Blue. doi: 10.1016/j.cpblue.2025.100001.
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


