体内诱导CAR-T细胞:有望突破当前CAR-T细胞治疗的障碍
来源:生物世界 2023-04-07 13:41
体内诱导CAR-T细胞有望取代当前的CAR-T细胞疗法,成为治疗癌症的标准免疫细胞疗法。
嵌合抗原受体T细胞疗法(CAR-T)在治疗恶性血液病方面取得了令人瞩目的成功,但目前自体CAR-T细胞疗法的全身毒性和复杂的制造过程阻碍了其更广泛的应用。通用型CAR-T细胞已经被开发出来,通过从健康人身上分离和编辑异基因T细胞来简化生产过程,但异基因CAR-T细胞最近遇到了安全问题,部分临床试验被FDA叫停。因此,迫切需要寻找新的方法来克服目前CAR-T细胞疗法的障碍。
在小鼠模型中,由装载CAR基因和基因编辑工具的纳米载体诱导的体内CAR-T细胞显示出了治疗白血病的效果以及更低的全身毒性。自体T细胞的原位编程避免了异体T细胞的安全问题,并且纳米载体的制造更易实现标准化。因此,体内诱导的CAR-T细胞有望克服目前CAR-T细胞治疗的诸多局限性。
近日,华中科技大学同济医学院附属协和医院吴小艳等人在 Frontiers in Oncology 期刊发表了题为:In-Vivo Induced CAR-T Cell for the Potential Breakthrough to Overcome the Barriers of Current CAR-T Cell Therapy (体内诱导CAR-T细胞有望突破当前CAR-T细胞治疗的障碍)的综述论文。
该论文综述了CAR结构、基因编辑工具和基因递送技术在免疫治疗中的应用,以及免疫细胞治疗的未来趋势,有助于设计和开发新的体内原位诱导CAR-T细胞。

嵌合抗原受体T细胞疗法(CAR-T)是一种新型细胞免疫治疗技术,它将合成受体结合到T细胞中,用同源靶向配体识别和杀死肿瘤细胞。自美国FDA首次批准CD19靶向的CAR-T细胞疗法以来,CAR-T细胞疗法在B细胞淋巴瘤患者中表现出了前所未有的治疗效果。然而,随着CAR-T细胞治疗的显著成就,细胞因子释放综合征(CRS)、神经毒性等许多全身毒性作用也被频繁报道。
此外,CAR-T细胞复杂的制造过程限制了这种治疗方法作为标准临床治疗的广泛应用。因此,迫切需要开发一种新型CAR-T细胞范式来克服这些障碍,并让这种治疗方法使更多的患者受益。
为了简化CAR-T细胞的复杂制造过程,来自健康人的通用异基因CAR-T细胞已在临床试验中进行了测试。通用CAR-T细胞可以是现成的,然后像普通药物一样注入患者体内,而不需要等待从患者体内分离出自体T细胞。然而,去年Cellectis公司的通CAR-T疗法UCARTCS1A临床试验期间的死亡案例引发了人们对异基因CAR-T细胞安全性的担忧。出于安全考虑,FDA最近还停止了来自Allogene公司的通用CAR-T细胞的临床试验。因此,我们需要新的策略来克服相关毒性,并简化当前CAR-T细胞疗法的制造过程。
由装载CAR基因的纳米载体和基因编辑工具诱导的体内CAR-T细胞对白血病显示出良好的效果。原位编程自体CAR-T细胞可以增强对肿瘤细胞的靶向杀伤,降低细胞因子释放综合征(CRS)和神经毒性等全身毒性。此外,纳米载体可以很容易地以标准化的方法制造。体内诱导的CAR-T细胞为克服目前CAR-T细胞治疗的障碍提供了一种潜在的解决方案。
本文综述了CAR结构设计、基因编辑工具、基因递送系统以及免疫细胞治疗的未来趋势。
CAR结构和进化
嵌合抗原受体(CAR)的结构具有模块化设计,包括抗原结合域、铰链、跨膜域和细胞内信号域(图1A)。抗原结合域通常是由单克隆抗体衍生的单链可变片段(scFv)分子,可与恶性癌细胞表面的抗原结合,跨膜结构域负责将CAR锚定在T细胞膜上。细胞内信号域通常包含T细胞受体CD3ζ链衍生的T细胞激活域,以及共刺激域,通常由含有CD28或4-1BB区域的基于酪氨酸的免疫受体激活基序组成(也称为CD137和TNFRSF9)。CAR结构的每个组成部分的变化能够微调最终CAR-T细胞产品的功能和抗肿瘤活性。
各种CAR结构被设计用来提高CAR-T细胞治疗的安全性和有效性。一旦设计的CAR基因被整合到T细胞中,T细胞表面的scFv会特异性地识别肿瘤相关抗原,并将CAR-T细胞与肿瘤细胞结合。在此之后,CAR-T细胞的细胞内信号域被激活,导致CAR-T细胞增殖并分泌杀死肿瘤细胞的细胞因子。
自2011年宾夕法尼亚大学Carl June和费城儿童医院David Porter首次将CAR-T细胞应用于临床治疗以来,CAR结构已经历经了五代发展(图1B)。第一代CAR含有细胞内刺激区和细胞外单链抗体,由于缺乏共刺激分子,这一代CAR-T细胞不能持续增殖。第二代CAR增加了一种共刺激分子,如CD28,或4-1BB(CD137),以增强CAR-T细胞的增殖和降低毒性。Yescarta™和Kymriah™这两款最早获批上市的CAR-T细胞疗法是分别含有CD28和4-1BB的第二代CAR-T细胞。第三代CAR包括两个共刺激分子,如CD27、CD28、肿瘤坏死因子超家族4(OX40,也称为CD134)、4-1BB(CD137)或CD244。第四代CAR被称为TRUCKs,它结合了CAR-T细胞的直接抗肿瘤能力和递送的细胞因子的免疫调节功能。TRUCKs已经进入早期临床试验,使用一系列细胞因子,包括IL-7、IL-12、IL-15、IL-18、IL-23及其组合。第五代则集成了一个额外的膜受体,以抗原依赖的方式控制CAR-T细胞的激活。
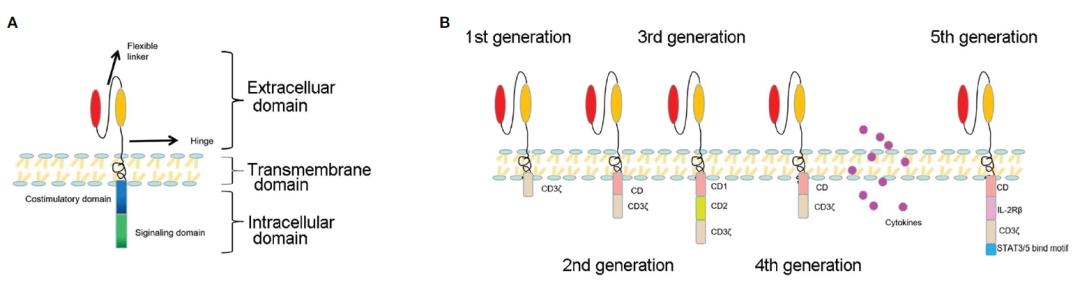
图1A:CAR的基本结构;图1B:五代CAR的发展
除了在CAR结构中添加新的功能分子外,许多研究为新的CAR结构选择了替代的肿瘤靶向位点。CD30在霍奇金淋巴瘤恶性细胞上表达非常强,而在健康淋巴细胞和造血干/祖细胞(HSPC)上表达较弱。CD30 CAR-T细胞疗法在CD30+恶性肿瘤的治疗中表现出优异的效果,而健康活化淋巴细胞和HSPC则不受影响。CD20是一种33-37-kDa的非糖基化跨膜磷酸化蛋白,有助于B细胞的发育和分化,CD20在晚期pre-B细胞和成熟B细胞中高表达,但在热休克细胞表面不表达。CD20 CAR-T细胞疗法在b细胞非霍奇金淋巴瘤的治疗中已显示出前景,目前正被考虑用于复发或难治性CD20阳性慢性淋巴细胞白血病患者。Lym-1靶向人B细胞淋巴瘤表面的人白细胞抗原D-相关抗原(HLA-DRs)的构象表位。Lym-1与恶性B细胞的结合亲和力高于正常B细胞,Lym-1 CAR-T细胞对B细胞淋巴瘤表现出强大的抗肿瘤作用。一些替代的靶向位点与CD19结合形成双靶点CAR-T细胞。例如,将CD37和CD19结合到一个CAR中,生成能够单独或同时识别CD19和CD37的双特异性CAR-T细胞。CD79b也是CD19的一个补充靶向位点。CD19和CD79双特异性CAR-T细胞阻止了B细胞淋巴瘤从CD19 CAR-T细胞逃逸。一些替代的靶向位点具有联合靶向功能,作用于肿瘤细胞和肿瘤微环境。例如,CD123在霍奇金淋巴瘤细胞和肿瘤相关巨噬细胞中都有表达,因此抗CD123的CAR-T细胞可以共同靶向这两种细胞并同时杀死它们。CAR结构在不断进化,以提高目前CAR-T细胞疗法的疗效。
当前CAR-T细胞疗法的障碍
从2017年到2021年,FDA已经批准了5款CAR-T细胞治疗产品上市,如表下表所示。

FDA批准的5款CAR-T细胞治疗产品
Kymriah™(Tisagenlecleucel)是首个被FDA批准用于某些类型B细胞淋巴瘤成人患者的CAR-T细胞疗法。三种已获批的CAR-T细胞产品Yescarta™(Axicabtagene ciloleucel)、TecartusE™(Brexucabtagene autoleucel)和Breyanzi®(Lisocabtagene maraleucel)也被批准用于B细胞淋巴瘤的治疗。第五种CAR-T细胞产品Abecma®(Idecabtagene vicleucel)用于多发性骨髓瘤治疗。
除了已获批准的5种CAR-T细胞产品外,还有大量的CAR-T细胞正在临床试验中进行研究,但目前的CAR-T疗法存在一些障碍,如相关毒性、免疫抑制肿瘤微环境和复杂的制造工艺,这些障碍阻碍了CAR-T疗法的更广泛应用。
目前CAR-T治疗相关的主要毒性包括细胞因子释放综合征(CRS,也称为细胞因子风暴)、免疫效应细胞相关神经毒性综合征(ICANS)和非肿瘤靶向毒性。CRS是由CAR-T细胞治疗后产生大量炎症细胞因子引起的,如IL-6、IL-10、IL-2和TNFα。CRS常引起发热、低血压、缺氧、器官功能障碍,甚至危及生命的不良反应。严重或危及生命的CRS发生率可达25%。ICANS是与CAR-T细胞治疗相关的另一种常见毒性,其特征是神经异常和后遗症,通常在CAR-T细胞治疗后1周内发生。ICANS引起的常见不良反应包括中毒性脑病伴失语、思维混乱和找词困难
非肿瘤靶向毒性是由于靶向蛋白在正常和恶性细胞上均有表达,例如,在恶性B细胞患者给予CD19 CAR-T细胞时,由于CD19 CAR-T细胞根除CD19+B细胞祖细胞,非肿瘤靶向效应将导致B细胞再生障碍性发育,并导致低γ球蛋白血症。
免疫抑制肿瘤微环境(MVT)抑制CAR-T细胞的活化,加速T细胞耗竭,免疫抑制MVT的不利因素包括缺氧、多种免疫抑制细胞、共抑制受体的持续表达。缺氧的定义是肿瘤MVT中缺氧。肿瘤MVT中的免疫抑制细胞包括调节性T细胞(Tregs)、肿瘤相关巨噬细胞(TAMs)和髓源性抑制细胞(MDSCs)。
目前CAR-T细胞的制造过程是一项非常复杂的工作,包括T细胞的收集、基因修饰和扩增,以及输注回患者体内,这些多步骤的技术和物流运输充满了风险。此外,长期和个性化的制造过程对建立标准操作程序提出了巨大的挑战。目前CAR-T细胞的制造过程昂贵且技术密集,这使得许多需要这种新疗法的癌症患者难以获取。
CAR-T细胞治疗中的基因编辑工具
CAR-T细胞治疗中常用的基因编辑工具包括ZFN、TALEN和CRISPR-Cas9技术。ZFN是第一代广泛应用的基因编辑工具,可以实现有效、特异的基因编辑,但优化目标蛋白分子耗时较长。TALEN作为第二代基因编辑工具,比ZFN更经济,但仍需要较长的时间来优化系统。而CRISPR-Cas9技术因其简单、高效和特异性成为最受欢迎的基因编辑工具。
以CRISPR-Cas9为代表的基因编辑技术的发展,使得CAR-T细胞的精确基因编辑能够通过去除T细胞的PD-1来生成抗耗竭T细胞。CRISPR-Cas9也被用于敲除正常细胞中的内源性抗原,如CD33和CD7,以减少重定向T细胞的非肿瘤靶向毒性。
目前,CRISPR-Cas9系统已用于至少21种靶抗原的CAR-T临床试验,其中CD19和BCMA这两个靶点占据了近一半。为了更广泛地使用CRISPR-Cas9系统来编辑CAR-T细胞,必须开发有效的递送方法。
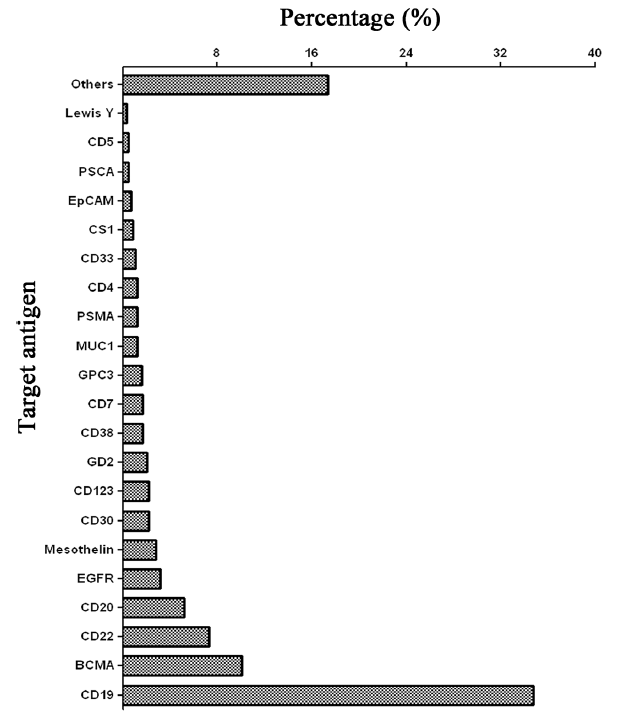
使用CRISPR-Cas9基因编辑技术的CAR-T细胞治疗的靶向抗原,数据截至2021年6月,仅统计在在美国注册的临床试验
基因递送系统
目前已有多个不同递送系统被用于递送基因治疗产品,包括递送基因编辑工具和CAR基因。例如各种病毒载体和非病毒载体。
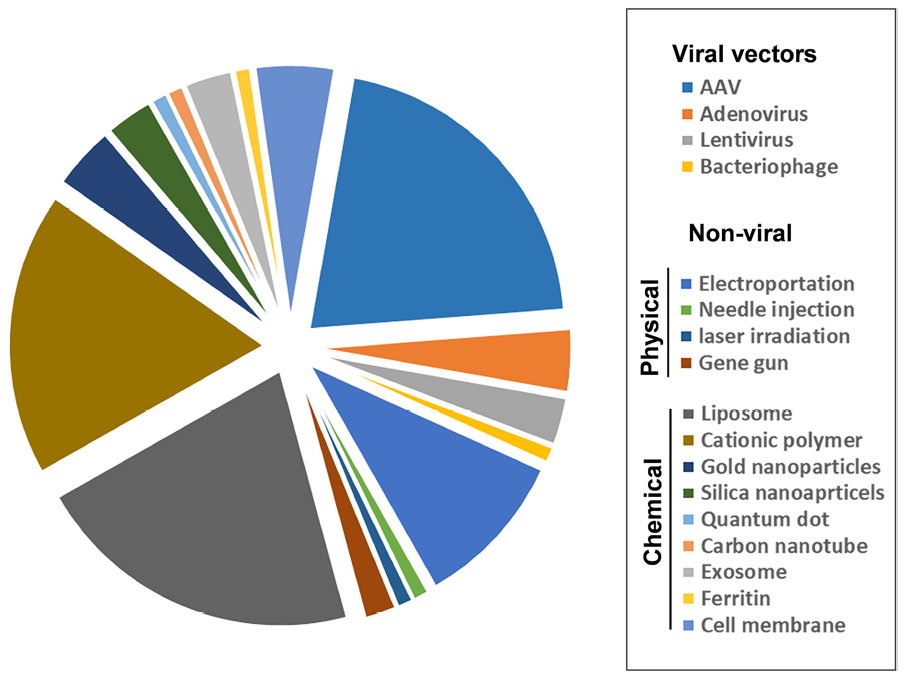
用于基因递送的病毒载体和非病毒载体的分类及占比情况
病毒载体具有最高的转染效率,被广泛应用于基因递送,但其存在免疫原性和细胞毒性等问题。腺相关病毒(AAV)比其他病毒载体(例如慢病毒和腺病毒)具有较低的毒性风险,然而,AAV载体比其他病毒载体的装载尺寸更小,只能递送不足5kb的DNA片段。
除了病毒载体外,还有非病毒递送系统,非病毒传递系统可以分为物理技术和化学技术两大类。物理技术包括电穿孔、针注射、激光辐照和基因枪。电穿孔是应用最广泛的基因递送方法之一,它利用电脉冲诱导细胞膜上的孔隙形成和基因的瞬时渗透性。物理技术由于免疫原性较低,成为一种有吸引力的基因递送方法,但这种方法不能靶向内脏器官。用于基因递送的化学技术主要包括阳离子脂质或基于聚合物的纳米颗粒、金纳米颗粒、二氧化硅纳米颗粒、碳纳米管、外泌体、铁蛋白、细胞质膜等等。
基于脂质的纳米颗粒是最具吸引力的非病毒基因递送载体之一,这些载体已经几种配方被批准用于临床。特别是脂质纳米颗粒(LNP)被成功用于递送mRNA新冠疫苗。LNP也被用于递送CRISPR-Cas9系统,在临床试验中实现了有效的基因编辑和治疗效果。基于聚合物的纳米颗粒是另一种适合基因递送系统,带正电的聚合物可以与破坏细胞膜并使内体逃逸的基因形成稳定的多聚体。基于聚合物的纳米颗粒的局限性在于其正电荷表面与血液循环中的负电荷细胞膜和蛋白质相互作用导致的毒性和免疫原性。
外泌体是天然分泌的纳米尺寸的细胞外囊泡,由于其天然的生物相容性和最小的免疫清除,正被广泛研究作为基因递送载体。但是将外泌体作为基因递送载体,还要克服生产、分离和提纯方面的困难,目前还面临着诸多挑战。来自血小板、红细胞的细胞质膜是用于基因递送的仿生载体,具有天然的生物相容性和靶向性,但其转染效率有待提高。其他化学纳米载体都具有一些自己的特性,决定了它们对基因递送的影响。一些已经显示出治疗多种疾病的潜在效果,但最佳的给药系统仍未实现临床应用。
体内CAR-T细胞诱导
目前CAR-T细胞的制造过程需要专门的设备和大量的技术积累,而且是劳动密集型和耗时的,限制了这项技术在全球范围内的广泛应用,并推高了CAR-T细胞疗法的价格,使许多患者无法负担。
为了简化生产过程,来自异体健康人的通用型CAR-T细胞已在临床试验中进行了测试,但是,由于对异体CAR-T细胞的安全性担忧,FDA最近暂停了来自异体基因的通用型CAR-T细胞的临床试验。因此,迫切需要开发一种安全、简单的CAR-T细胞生产工艺。
通过纳米颗粒在体内对CAR-T细胞进行编程是简化和标准化体外CAR-T细胞复杂制造过程的一种优雅而新颖的方法。此外,CAR-T细胞的原位诱导可有效降低细胞因子释放综合征(CRS)、免疫效应细胞相关神经毒性综合征(ICANS)等全身毒性。
早在2017年和2020年,美国Fred Hutchinson癌症研究中心的 Matthias Stephan 教授就曾先后在 Nature Nanotechnology 和 Nature Communications 期刊发表论文【2、3】。通过纳米载体递送CAR-DNA或CAR-mRNA实现体内诱导CAR-T细胞。在这两项工作中,纳米递送系统的核心由阳离子聚合物聚(β-氨基酯)构成,并与靶向CD19的第二代CAR结构组装。纳米递送系统的外部由聚谷氨酸(PGA)与抗CD3抗体缀合而成。携带CD19特异性CAR基因的聚合物纳米颗粒在体内快速和特异性编辑T细胞,并带来了与传统实验室制造的CAR-T细胞相当的抗肿瘤效果,而不会引起全身毒性。
Christian Buchholz 等人首次报道了用第二代抗CD19-CAR基因包裹的慢病毒在免疫缺陷NOD-scid-IL2Rc null(NSG)小鼠中原位诱导CAR-T细胞,并显示出抗肿瘤活性。在他们的研究中,意外检测到CAR阳性的NK和NKT细胞,这可能是由于慢病毒载体的非特异性造成的。
为了克服病毒载体的非特异性,Samuel K Lai等人开发了一种双特异性结合剂,将慢病毒载体重定向到T细胞,用于CAR-T细胞的体内特异性工程。他们观察到由慢病毒改造的体内CAR-T细胞具有抗肿瘤活性,但表达CAR的T细胞数量相对较少。他们认为这证明了一个有价值的、未经证实的理论,即与离体CAR-T细胞相比,体内CAR-T细胞具有更好的性能和自我更新能力。
在病毒载体中,腺相关病毒(AAV)的毒性风险较低,2021年3月,南京大学医学院吴喜林等人在 Blood Cancer Journal 期刊发表论文【4】,报道了AAV编码第三代CAR基因可以充分重编程免疫效应细胞产生体内CAR-T细胞。在这项工作中,他们证明了AAV在体内诱导CAR-T细胞的概念,但他们也表示了对携带CAR基因的AAV的非特异性的担忧。除了病毒载体的非特异性外,病毒载体的另一个普遍担忧的安全问题是其可能导致基因在染色体中的随机插入。
精确快速的基因编辑工具如CRISPR已被广泛用于生成体外CAR-T细胞。利用CRISPR进行体内基因编辑的研究很多,但目前还没有应用CRISPR生成体内CAR-T细胞的报道。结合基因编辑工具和CAR基因的未来应用将加速体内CAR-T细胞的临床应用。
纳米载体递送设计的CAR-结构和基因编辑工具可以诱导具有多种功能的CAR-T细胞在体内形成,以克服当前CAR-T细胞的障碍,如相关毒性作用、免疫抑制微环境和复杂的制造过程。
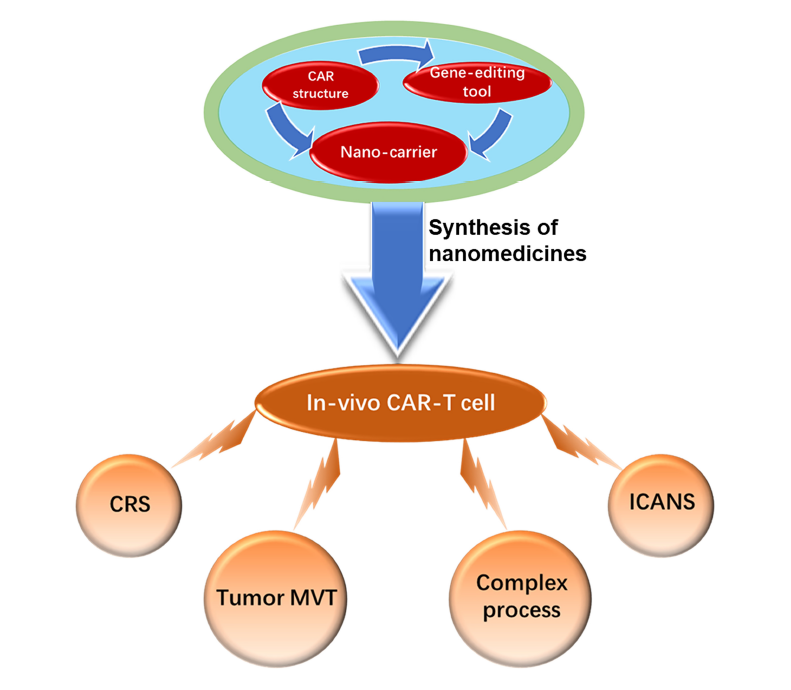
全身毒性作用可以通过肿瘤原位编辑和T细胞的扩增来降低。在CAR结构中加入特殊的细胞因子基因,使CAR-T细胞能够分泌细胞因子,改善免疫抑制微环境,使其适合T细胞的生存和增殖。将CAR结构的基因编辑工具加载到纳米颗粒中,可以敲除免疫检查点基因,从而逆转T细胞耗竭。更重要的是,该方法解决了体外CAR-T细胞制造工艺标准化和规模化的难题。最终,通过纳米递送载体可以方便地生产、储存和作为常规药物的CAR-T细胞治疗产品。
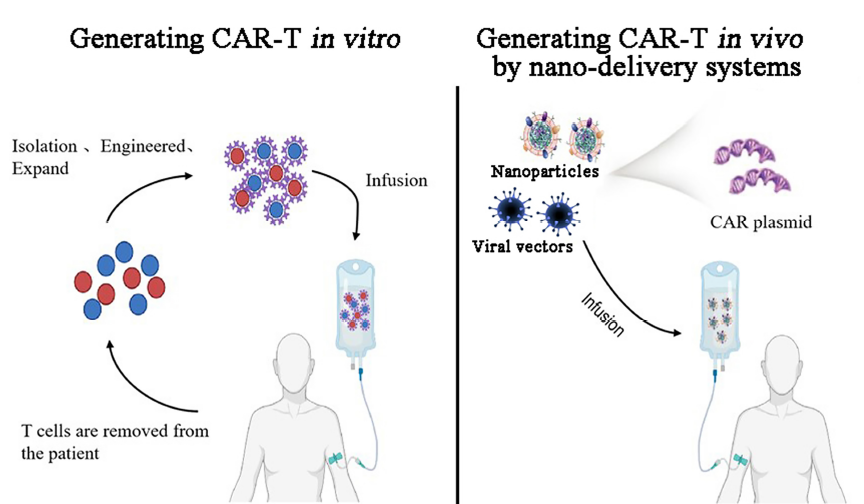
体外生成CAR-T与基于纳米递送系统的体内生成CAR-T的比较
上述这些研究只是体内原位诱导CAR-T细胞的开始,要想实现临床应用,还需要更多的努力来监测T细胞在体内的编辑和扩增状态。
结论与展望
在过去的十年中,CAR-T细胞治疗取得了巨大成就,已有五种CAR-T细胞产品已获得FDA批准上市。然而,目前的CAR-T细胞疗法也有一些需要克服的障碍,如CRS和ICANS的毒性以及昂贵和复杂的生产制造程序。通过装载CAR基因的纳米颗粒和基因编辑工具在体内诱导CAR-T细胞,已经显示出克服当前CAR-T细胞疗法障碍的潜在突破。
尽管很少有研究报道纳米颗粒诱导的体内CAR-T细胞,但可靠的临床前数据预测了通过纳米递送方法进行细胞治疗的未来前景。体内诱导CAR-T细胞治疗领域仍处于起步阶段,将这种方法转化为临床实践同样面临许多挑战。系统总结用于体内诱导CAR-T细胞的纳米递送系统可以指导纳米颗粒及其负载物的设计,以优化其功效。
综上所述,体内诱导CAR-T细胞有望取代当前的CAR-T细胞疗法,成为治疗癌症的标准免疫细胞疗法。
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


