2021年12月10日Science期刊精华
来源:本站原创 2021-12-16 23:53
2021年12月16日讯/生物谷BIOON/---本周又有一期新的Science期刊(2021年12月10日)发布,它有哪些精彩研究呢?让小编一一道来。1.Science:真核生物的核孔是机械敏感性的doi:10.1126/science.abd9776真核生物的细胞核容纳并保护遗传信息。它被核膜所包围,而且核膜将核质与细胞质分开。核膜的双膜系统与细胞骨架和
2021年12月16日讯/生物谷BIOON/---本周又有一期新的Science期刊(2021年12月10日)发布,它有哪些精彩研究呢?让小编一一道来。
1.Science:真核生物的核孔是机械敏感性的
doi:10.1126/science.abd9776
真核生物的细胞核容纳并保护遗传信息。它被核膜所包围,而且核膜将核质与细胞质分开。核膜的双膜系统与细胞骨架和染色质在物理上连接在一起。它能感知机械刺激并发出信号。核孔复合物(nuclear pore complex, NPC)介导核质互换。它们将内核膜和外核膜融合在一起,形成一个水性的中央通道。它们复杂的圆柱形结构由大约30个核孔蛋白组成。这种核孔蛋白支架以高度动态的方式呈现膜融合拓扑结构。NPC直径的变化已有报道,但其生理情况和分子细节仍是未知的。
为了研究体内NPC构象的动态变化,在一项新的研究中,德国研究人员对裂殖酵母细胞中的NPC进行了结构分析。他们使用低温电子断层成像和随后的子断层扫描图平均化(subtomogram averaging)来定量确定暴露于不同应激刺激下的细胞中的NPC直径。他们发现在指数生长的细胞中,NPC支架扩张,然而在能量耗尽和高渗冲击(hyperosmotic shock)的条件下,它们会收缩。将综合结构模型结合在一起的结构分析显示,NPC支架在收缩过程中经历了大规模的运动和弯曲。因此,这个中央通道的体积减少到约二分之一。核质扩散明显减少。NPC支架上的核孔蛋白没有任何已知的使它们能够施加力量的运动活性。因此,观察到的NPC直径的动态变化很可能是在核膜内侧向施加的力量的结果。在能量耗尽和高渗冲击的条件下,细胞体积和核体积减少,以致于核收缩导致核膜过剩。因此,他们推测NPC支架对机械敏感。他们还推测,核膜张力的降低会导致NPC收缩到一种构象基态。相关研究结果发表在2021年12月10日的Science期刊上,论文标题为“Nuclear pores dilate and constrict in cellulo”。
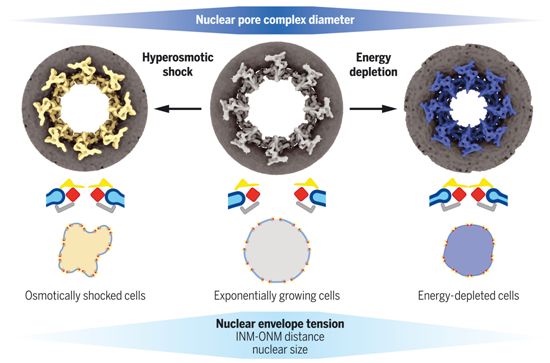
NPC在细胞能量耗尽和高渗冲击的条件下会收缩。图片来自Science, 2021, doi:10.1126/science.abd9776。
2.Science:重大进展!揭示白内障形成的病理机制,有望开发出新的疗法
doi:10.1126/science.abk0410
随着年龄的增长,衰老在各种退化性疾病的发病中发挥着重要作用,包括白内障的缓慢发展。白内障是一种晶状体混浊,困扰着全世界数百万人的视力。形成眼球晶状体的透明细胞在一生中不断分裂,但在老年人中,这种细胞分裂过程的效率较低,而且衰老的细胞会引发透明度的下降。尽管发病机制在很大程度上还不清楚,但具有早发白内障遗传倾向的患者可以帮助确定分子机制。
缺乏脂质激酶PI3K-C2α会导致鱼类、小鼠和人类的白内障提前发生。这表明PI3K-C2α参与维持一种进化上保守的保护晶状体免受透明度下降影响的机制。在这一发现的基础上,来自意大利都灵大学等研究机构的研究人员在一项新的研究中,从该激酶参与有丝分裂以及正确的细胞分裂可避免衰老和白内障最终产生的概念出发,想要确定PI3K-C2α在晶状体中的作用。相关研究结果发表在2021年12月10日的Science期刊上,论文标题为“PI(3,4)P2-mediated cytokinetic abscission prevents early senescence and cataract formation”。
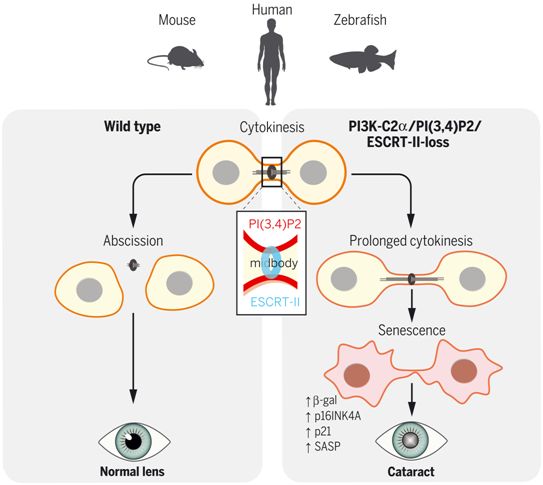
图片来自Science, 2021, doi: 10.1126/science.abk0410。
在中心颗粒体,ESCRT I(endosomal sorting complexes required for transport I)复合物触发了ESCRT II蛋白聚合体的去核,随后触发膜切割ESCRT III装置的去核。作为ESCRT II复合物中的一种关键成分,VPS36锚定在局部预形成的PI(3,4)P2上,从而适当地让ESCRT II蛋白聚合体在中心颗粒体上保持稳定。这是在鱼类、小鼠和人类中发现的,这表明这一过程在整个脊椎动物进化过程中一直是保守的。
如果没有PI3K-C2α及其脂质产物PI(3,4)P2,ESCRT装置就会失去效率,细胞分裂就会延迟。延长的细胞分裂引发了p16INK4A的表达和转录程序的激活,从而导致衰老,这很可能避免了细胞分裂后再融合和四倍体化的基因组不稳定性。然而,细胞分裂演变为一种有弹性的细胞过程,在各种ESCRT复合体的组装中,冗余的途径很常见。例如,ESCRT III组装的另一种绕过了对ESCR II聚合体的需要的途径依赖于连接蛋白ALIX的功能。在晶状体中,ALIX表达不良,特别需要PI3K-C2α、PI(3,4)P2和VPS36途径来保护晶状体细胞免受细胞分裂延迟、衰老以及最终的白内障形成。
3.Science:我国科学家揭示小鼠和人类大脑发育的相似性和差异
doi:10.1126/science.abj6641
GABA能中间神经元(GABAergic interneuron)是中枢神经系统中产生主要抑制性化学信使---γ-氨基丁酸(GABA)---的神经元。在一项新的研究中,来自中国科学院生物物理研究所、北京师范大学、清华大学、首都医科大学和英国伦敦大学国王学院的研究人员发现GABA能中间神经元早期发育背后的一些过程在人类和小鼠之间是一致的。这是对人类中间神经元(interneuron)---介于神经中枢之间的神经元---发育的首次彻底调查,并阐明了人类和小鼠大脑发育的重要相似性和差异。相关研究结果发表在2021年12月10日的Science期刊上,论文标题为“Mouse and human share conserved transcriptional programs for interneuron development”。
这些作者使用单细胞RNA测序来描述神经节隆起(ganglionic eminences)中细胞多样性的出现,其中神经节隆起是GABA能中间神经元的起源区域。在此过程中,他们发现了小鼠和人类大脑早期发育过程的显著一致性。这种单细胞RNA测序使得这些作者能够构建人类发育的中期妊娠早期(相当于妊娠期的第9-18周)的基因表达的时空图谱。
作为大脑中最大和最发达的部分,端脑(telencephalon)的组织和细胞结构在哺乳动物之间是广泛保守的,尽管它的大小和复杂性在啮齿动物和灵长类动物之间有很大的差异。以前的分析已表明,构成大脑皮层的细胞在小鼠和人类之间相对相似。然而,在小鼠和人类的成年大脑中,特定类型的中间神经元的相对比例、组织分布和基因表达模式存在广泛差异。
这些作者指出,这项研究阐明了人类GABA能中间神经元的出现,并确定了人类和啮齿动物的大脑发育之间的相同点和差异。重要的是,这项研究使人们对神经发育障碍的理解达到了新的水平。许多神经发育障碍都有重叠的遗传学和表型,纹状体和皮层GABA能神经元的变化已经在自闭症和精神分裂症中得到了有力的证明。
4.Science:利用人工智能成功预测蛋白相互作用
doi:10.1126/science.abm4805
在一项新的研究中,来自美国德克萨斯大学西南医学中心和华盛顿大学等研究机构的研究人员利用人工智能(AI)和进化分析构建出真核生物蛋白相互作用的三维模型。他们首次鉴定出100多种可能的蛋白复合物,并为700多种以前未被描述的蛋白复合物提供了结构模型。对成对或成组的蛋白如何结合在一起执行细胞过程的深入了解可能会带来大量新的药物靶标。相关研究结果于2021年11月11日在线发表在Science期刊上,论文标题为“Computed structures of core eukaryotic protein complexes”。论文通讯作者为德克萨斯大学西南医学中心的Qian Cong博士和华盛顿大学的David Baker博士。论文第一作者为华盛顿大学的Ian R. Humphreys、Minkyung Baek和Aditya Krishnakumar以及德克萨斯大学西南医学中心的Jimin Pei。
直到最近,构建相互作用组的一个主要障碍是许多蛋白质结构的不确定性,这是科学家们半个世纪以来一直试图解决的问题。2020年和2021年,一家名为DeepMind的公司和Baker博士的实验室独立发布了两项名为AlphaFold(AF)和RoseTTAFold(RF)的人工智能技术,这两种技术根据产生蛋白的基因序列使用不同的策略来预测蛋白结构。
在这项新的研究中,Cong博士、Baker博士和他们的同事通门过对许多酵母蛋白复合物进行建模,扩展了这些人工智能结构预测工具。酵母是一种常见的基础生物学研究的模型生物。为了找到可能相互作用的蛋白,他们首先在相关真菌的基因组中寻找以相互关联的方式获得突变的基因。然后,他们使用这两种人工智能技术来确定这些蛋白是否可以在三维结构中配合在一起。
他们的研究确定了1505种可能的蛋白复合物。其中的699种已在结构上得到表证,验证了他们方法的实用性。然而,只有有限的实验数据支持700种预测的相互作用,另外106种从未被描述过。
为了更好地了解这些较差表证或未知的蛋白复合物,Cong团队、Baker团队与世界各地已经在研究这些或类似蛋白的同事们合作。通过这项新研究中构建的三维模型与合作者提供的信息相结合,他们能够获得对参与维持和处理遗传信息、细胞构造和运输系统、新陈代谢、DNA修复和其他领域的蛋白复合物的新见解。他们还根据新发现的与其他特征明确的蛋白的相互作用,确定了以前功能未知的蛋白的作用。
5.Science:新研究表明mRNA-1273疫苗加强注射会增加猴子的中和抗体反应和保护作用
doi:10.1126/science.abl8912
在一项新的研究中,来自美国国家卫生研究院等研究机构的研究人员在恒河猴接种初始疫苗系列(primary vaccine series)大约六个月后,给它们加强注射mRNA-1273 COVID-19疫苗,可显著提高针对所有已知SARS-CoV-2变体的中和抗体水平。相关研究结果于2021年10月21日在线发表在Science期刊上,论文标题为“Protection against SARS-CoV-2 beta variant in mRNA-1273 vaccine–boosted nonhuman primates”。
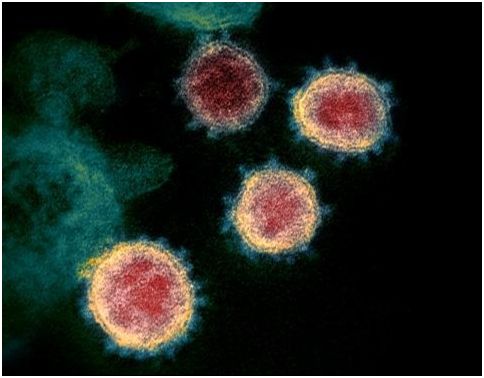
SARS-CoV-2(之前称为2019-nCoV)的透射电镜图,图片来自NIAID RML。
这项研究是在六个月前进行的,当时SARS-CoV-2的Beta变体是一个主要问题。这些作者把重点放在Beta变体上,因为根据这些作者的说法,它一直显示出最大的抗中和抗体能力,这可能是通过降低疫苗的有效性来实现的。这些作者指出,虽然SARS-CoV-2的Delta变体已经成为美国的主要病毒变体,但由于它的高传播性,它只有中等的抗中和能力。
这些作者写道,在人身上,mRNA-1273疫苗加强注射可能会提高上、下呼吸道免受包括Delta变体在内的任何流通中的SARS-CoV-2变体感染的时间和效力。他们指出,这对于维持对严重疾病的保护并可能限制轻度感染和病毒传播尤为重要。他们的结果支持对老年人、已有基础疾病的人、高风险暴露的人以及对初始疫苗接种反应不佳的人进行疫苗加强注射。
6.Science:揭示SARS-CoV-2的Delta变体传染性为何如此之强
doi:10.1126/science.abl9463
SARS-CoV-2的Delta变体已经席卷了整个地球,在短短几个月内成为主导变体。在一项新的研究中,来自美国波士顿儿童医院的研究人员解释了为何Delta变体如此容易传播并如此迅速地感染人们。它还为开发下一代COVID-19疫苗和治疗方法提出了一种更有针对性的策略。相关研究结果于2021年10月26日在线发表在Science期刊上,论文标题为“Membrane fusion and immune evasion by the spike protein of SARS-CoV-2 Delta variant”。
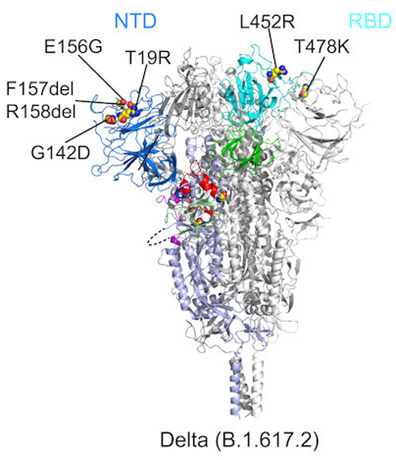
这张带状图显示了在与靶细胞融合之前Delta变体刺突蛋白的结构,突出显示了NTD突变E156G、T19R、F157del、R158del和G142D,以及RBD突变L452R和T478k。图片来自Science, 2021, doi:10.1126/science.abl9463。
Chen及其同事们使用两种基于细胞的检测方法,证实Delta变体的刺突蛋白特别擅长于膜融合。这使得模拟的Delta变体能够比其他五种SARS-CoV-2变体更快更有效地感染人类细胞。特别是当人类细胞中ACE2受体的数量相对较少时,Delta变体的优势更加明显。
Chen解释说,“膜融合需要大量的能量,并且需要一种催化剂。在不同的SARS-CoV-2变体中,Delta变体在催化膜融合的能力方面表现突出。这解释了为什么Delta变体的传播速度要快得多,为什么你在较短的接触后就能感染它,以及为什么它能感染更多的细胞并在体内产生如此高的病毒载量。”
7.Science:探究植物叶子发育
doi:10.1126/science.abf9407
禾本科植物(grasses)的长而窄的叶片看起来与通常较短、较平的双子叶植物(eudicot plant)的叶片相当不同。Richardson等人将发育遗传学和计算模型结合起来,揭示出这两种因进化而被广泛分开的叶子,其共同点比预期的要多。类似的模式化基因在原始区(primordial zone)中的表达对于双子叶植物的叶子来说只限于楔形区域,而在禾本科植物的叶子中则扩展到同心圆区域,这推动了禾本科植物叶子特征性的圆柱形环状鞘的发育。边缘区(marginal zone)中的基因表达的增加或去除有助于产生双子叶植物特征性的更宽叶片。
8.Science:探究热带森林恢复
doi:10.1126/science.abh3629
尽管整个热带地区的森林砍伐十分猖獗,但森林在废弃的土地上有很强的重新生长能力。这些“次生”森林可能会在生物多样性保护、减缓气候变化和景观恢复方面发挥越来越重要的作用。Poorter等人分析了美洲和西非77个次生林地点的森林属性(与土壤、植物功能、结构和多样性有关)的恢复模式。他们发现,不同森林属性的恢复速度不同,土壤在不到十年的时间内恢复,而物种多样性和生物量的恢复则略多于一个世纪。这些作者讨论了如何将这些发现应用于促进森林恢复的努力中。(生物谷 Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


