肝纤维化:细胞外小泡介导的窦周间隙细胞间通讯
来源:本站原创 2021-11-29 13:13
肝脏复杂的功能活动是精心安排的,这要归功于所有肝实质细胞和非肝实质细胞群体之间结构良好的串扰。肝内不同细胞类型释放的胞外小泡(EV)旁分泌相互作用是重要的细胞间通讯工具
肝脏复杂的功能活动是精心安排的,这要归功于所有肝实质细胞和非肝实质细胞群体之间结构良好的串扰。肝内不同细胞类型释放的胞外小泡(EV)旁分泌相互作用是重要的细胞间通讯工具。在正常肝脏中,静止的肝星状细胞(HSCs)释放的EV调节细胞的再生、存活、细胞分化、细胞迁移和免疫反应。慢性肝损伤后,HSC被激活,获得肌成纤维细胞(MFBs)样表型,并异常分泌细胞外基质蛋白,形成纤维瘢痕。
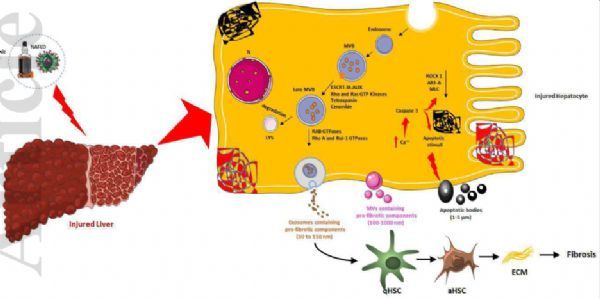
为了维持受损肝脏的病理状态,激活的HSCs分泌含有促纤维化成分的特异性EV,这些EV与肝细胞、静止期HSCs、肝窦内皮细胞(LSECs)和肝窦周围和窦状隙中的Kupffer细胞相互作用。活化的HSCs分泌富含miR-192、血小板衍生生长因子受体和凋亡信号调节激酶1的EV,通过雷帕霉素和Rho相关蛋白激酶1信号轴的机制靶点激活静止的HSCs,称为“水平转移过程”。 同时,损伤肝细胞来源的促炎β(miR-19a和-192)和富含转化生长因子-miRNA的外切体将分别激活枯否细胞和造血干细胞上的Toll样受体-9和-3,从而获得纤维化表型。
图片来源: https://pubmed.ncbi.nlm.nih.gov/34773651/
每年全球约有120万人死于肝病,占全球总死亡人数的3.5%。急性肝损伤通常是可逆的,而慢性肝损伤通常会导致肝脏炎症、脂肪性肝病、肝纤维化、肝硬化和肝细胞癌(HCC)。慢性肝损伤和持续的炎症过程刺激纤维化,导致肝硬化、HCC和随后的肝功能衰竭。
目前,全球有15亿人受到任何形式的慢性肝病(CLD)的影响。肝纤维化被认为是肝脏结构恶化的会合点。近年来,由于肝炎、非酒精性脂肪性肝炎(NASH)、慢性酒精摄入、代谢综合征等原因,肝硬化的发病及其相关死亡率显著增加。
肝细胞来源的外切体调节邻近肝细胞和非实质细胞(如肝星状细胞(HSCs)、肝窦内皮细胞(LSECs)、库普弗细胞(Kupffer Cell)或浸润性免疫细胞)的再生和修复。肝星状细胞、肝星状上皮细胞和胆管细胞也分泌外泌体,在肝损伤时调节肝脏重塑。
然而,在慢性肝损伤后,肝细胞分泌含有几个促纤维化信号分子的外泌体,进而激活其他肝细胞在窦周间隙传播一系列促纤维化信号。此外,越来越多的证据也证实,肝病及其进展往往与来源于或转移到肝星状细胞和存在于窦周隙中的其他细胞的胞外小泡有关。
因此,这篇综述的重点是造血干细胞来源的细胞外囊泡在肝纤维化过程中的作用及其与窦周环境中细胞群的相互作用。
损伤肝细胞合成的胞外小泡的生物发生和类型
图片来源: https://pubmed.ncbi.nlm.nih.gov/34773651/
一些证据表明qHSC来源的EV具有抗纤维化作用,而AHSC来源的EV含有多种促纤维化蛋白、脂质和核酸,如mRNA、miRNA和lncRNA。在损伤肝脏的窦周间隙,AHSC通过多种细胞间和细胞内通讯途径,以多种类型的肝细胞为靶点,包括肝细胞、qHSCs、LSECs和Kupffer细胞。同时,来自不同细胞来源的EV激活qHSCs以获得类似MFBs的表型。
然而,在正常肝脏的窦周间隙,qHSC释放的EV是稳态细胞间和细胞内通讯的重要介质。到目前为止,我们对这一过程的理解还处于初级阶段。因此,未来的研究有必要深入了解EVS的发生、命运、释放和分子功能的调控机制,以便有效地解决它们的治疗用途或在进一步的临床应用中进行分析。(生物谷 Bioon.com)
参考文献
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。