irf3结合的lncRNA-ISIR可增强病毒感染和自身炎症中干扰素的产生
来源:本站原创 2021-11-25 17:45
干扰素调节因子3 (IRF3)是启动许多免疫反应的重要转导因子。
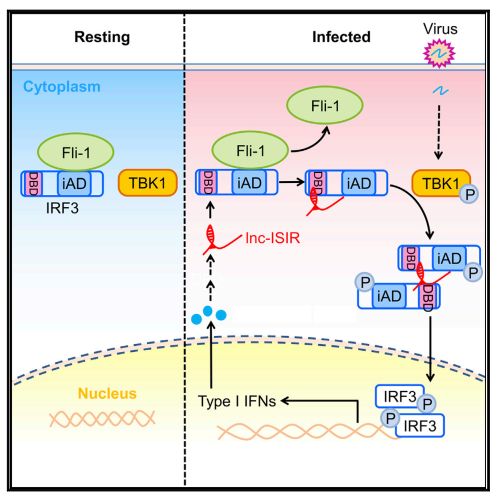
干扰素调节因子3 (IRF3)是启动许多免疫反应的重要转导因子。在这里,作者发现lncRNA-ISIR直接结合IRF3,促进其磷酸化、二聚和核易位,并增强靶基因的产生。体内lncRNA-ISIR缺陷导致IFN产生减少,病毒复制失控,死亡率增加。人类同源物AK131315也与IRF3结合并促进其激活。更重要的是,AK131315在狼疮患者中的表达与I型干扰素(IFN-I)水平和狼疮严重程度呈正相关。
机制上,在静息细胞中,IRF3与抑制蛋白Flightless-1 (Flightless-1)结合,使其保持不活动状态。在感染后,ifn -i诱导的lncRNA-ISIR在细胞质的dna结合区域与IRF3结合,并从IRF3上去除fli1 s的关联,从而促进IRF3的激活。该研究结果表明,ifn -i诱导的lncRNA-ISIR反馈通过消除免疫应答中抑制的Fli-1来增强IRF3的激活,揭示了一种lncrna介导的转录因子(TF)激活调节方法。
图片来源:https://doi.org/10.1016/j.celrep.2021.109926
精心设计的先天免疫反应,尤其是 I 型干扰素 (IFN-I) 的适当诱导,在宿主防御多种感染(尤其是病毒感染)以及许多自身免疫性疾病的发病机制中起着至关重要的作用。入侵病毒的核酸组分可被宿主保守模式识别受体(PRRs)识别,包括维甲酸诱导基因I (RIG-I)、环型GMP-AMP合成酶(cGAS)、异质核蛋白A2/B1 (hnRNPA2B1)和toll样受体(TLRs)。
然后通过rig -i -线粒体抗病毒信号蛋白(MAVS)、cgas干扰素基因刺激因子(STING)和TLR3-TIR结构域包含的适配器诱导b干扰素(TRIF)等信号适配器激活免疫信号级联,募集并激活tank结合激酶1 (TBK1),然后磷酸化转录因子(TF) IRF3。在磷酸化后,IRF3形成同源二聚体,随后转移到细胞核,与其他转录因子(如IRF7)合作,诱导ifn,主要是IFN-I和大量ifn刺激基因(ISGs),保护宿主免受病毒感染。在大多数细胞类型中,IRF3是构成性表达的,激活后会刺激IRF7的表达,而IRF7只在浆细胞样树突状细胞(pDCs)和巨噬细胞中构成性表达。
IRF3作为一种重要的转录因子,在免疫应答中产生IFN-I是必不可少的。IRF3功能障碍可引起免疫系统紊乱,包括炎症自身免疫性疾病、淋巴系统疾病、慢性感染性疾病等。到目前为止,已经揭示了多种不同水平的调节机制来调节IRF3的功能。有报道称,适配器MAVS、STING和TRIF的pLxIS基序磷酸化导致IRF3招募,从而使IRF3被TBK1磷酸化。
接下来,IRF3二聚并与GREBBP形成复合物,转运到细胞核。此外,IRF3可以被RACK1-PP2A复合物去磷酸化,然后在细胞质中恢复静息状态。虽然已经报道了许多IRF3相关蛋白,但抑制结合蛋白和IRF3 RNA结合调节IRF3激活仍然需要充分了解。
越来越多的长非编码rna (long noncoding RNAs, lncrna)被报道用于确定免疫发育和调节免疫应答,如在CD8 T细胞建立中lncRNA-Snhg1,在树突状细胞成熟中lnc-DC,以及在癌症免疫逃避中NKILA。lncrna可能以不同的方式发挥其生物学功能。
irf3结合的lncRNA-ISIR可增强病毒感染和自身炎症中干扰素的产生
图片来源:https://doi.org/10.1016/j.celrep.2021.109926
考虑到IRF3上的dna结合域(DBD)的核酸结合潜力,作者假设可能存在与IRF3相互作用的lncRNA,参与调控抗病毒免疫应答。通过甲醛交联RNA免疫沉淀(FA-CLIP)和RNA测序,作者发现了一种未被描述的irf3结合的lncRNA,即lncRNA- isir,它是在病毒感染时诱导产生的,来源于基因间非编码基因。IRF3以单体形式与肌动蛋白重塑蛋白Fli-1结合,在未受刺激的细胞中保持沉默。
激活后,lncRNA-ISIR被IFN-I诱导,与IRF3结合,阻断其与抑制蛋白Fli-1的联系,促进IRF3磷酸化、二聚体化和核易位,从而增强体内外IRF3启动的免疫应答。该工作揭示了一种更有效的lncRNA作用模式,即直接与免疫应答TF结合并调节其活性。(生物谷 Bioon.com)
参考文献
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。




