PNAS:揭示蛋白E-NTPD8抑制结肠炎恶化机制
来源:本站原创 2021-09-21 13:04
在一项新的研究中,来自日本大阪大学的研究人员发现了一种分子机制:通过调节肠道中一种影响某些免疫细胞并促进炎症反应的微生物代谢物---三磷酸腺苷(ATP)---的水平来抑制结肠炎的恶化。
2021年9月21日讯/生物谷BIOON/---肠道微生物生态系统包括不同种类的细菌。这些细菌可以产生生物活性代谢物,直接影响宿主的免疫系统。微生物代谢物的不平衡与包括溃疡性结肠炎在内的慢性疾病的发病机制有关。在一项新的研究中,来自日本大阪大学的研究人员发现了一种分子机制:通过调节肠道中一种影响某些免疫细胞并促进炎症反应的微生物代谢物---三磷酸腺苷(ATP)---的水平来抑制结肠炎的恶化。相关研究结果发表在PNAS期刊上,论文标题为“The ATP-hydrolyzing ectoenzyme E-NTPD8 attenuates colitis through modulation of P2X4 receptor-dependent metabolism in myeloid cells”。
由于肠道细菌分泌的ATP---称为腔内ATP(luminal ATP)---会影响宿主的免疫系统,因此要严格控制腔内ATP的数量以防止肠道炎症。然而,调节结肠腔内ATP水平的具体机制并不完全清楚。在这项新的研究中,这些作者调查了一种称为E-NTPD8(ectonucleoside triphosphate diphosphohydrolase 8)的ATP水解酶在结肠中的作用。
属于E-NTPD家族的酶可以将ATP分子分解为二磷酸腺苷或单磷酸腺苷(这被称为ATP水解),以阻止不适当的免疫反应。这些作者进行了细胞培养实验,发现E-NTPD8可以水解加入细胞培养基中的ATP。为了研究这种活性在体内的特定影响,他们利用缺乏E-NTPD8蛋白编码基因的小鼠构建出一种模型系统。
论文资深作者、大阪大学的Kiyoshi Takeda说,“在这些基因敲除小鼠中,E-NTPD8在结肠上皮细胞中的表达被完全移除,而野生型小鼠在这些细胞中高水平地表达这种蛋白。这些基因敲除小鼠的结肠中的腔内ATP水平也高得多。”
此外,在化学诱导结肠炎后,这些作者观察到E-NTPD8基因敲除小鼠的症状更严重。这些小鼠的结肠中Th17细胞和中性粒细胞(两种不同类型的免疫细胞)的数量也更多。用一种特定的抗体治疗这些小鼠以剔除中性粒细胞,明显改善了严重的结肠炎症状,而剔除其他类型的免疫细胞则没有这种效果。
论文资深作者、大阪大学的Hisako Kayama说,“进一步的机理实验向我们表明,ATP和一种叫做P2X4R的受体之间的相互作用起着至关重要的作用。与正常小鼠相比,同时缺乏E-NTPD8和P2X4R的小鼠有明显的疾病改善,以及具有减少的中性粒细胞数量。”
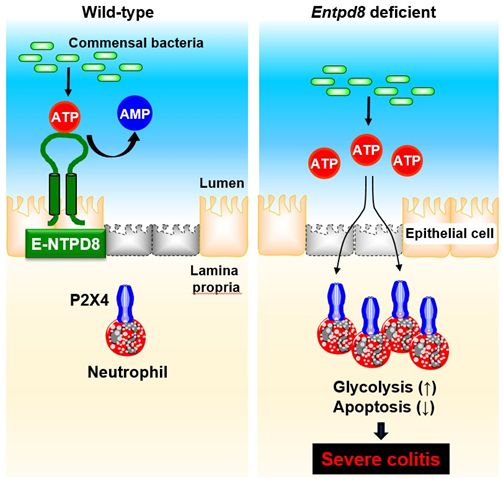
结肠上皮细胞中的E-NTPD8通过水解共生细菌产生的腔内ATP来维持肠道稳态(左)。由于缺乏E-NTPD8而引起的腔内ATP水平升高可调节中性粒细胞生理,如通过P2X4介导的糖酵解促进延长生存时间。这随后会加重结肠炎的症状(右图)。图片来自PNAS, 2021, doi:10.1073/pnas.2100594118。
这些作者确定腔内ATP可以通过P2X4R促进一种称为糖酵解的过程,这延长了中性粒细胞的生存。这最终导致了中性粒细胞在结肠内堆积而引起的炎症增加。
Kayama解释说,“我们的数据表明,控制腔内ATP-P2X4R信号传递和E-NTPD8的表达水平可能能够转化为针对人类溃疡性结肠炎的治疗干预。”
炎症性肠病,如溃疡性结肠炎和克罗恩病,对全世界数百万人的生活产生了负面影响。这些作者提供的有影响的数据为开发治疗这些疾病的新疗法提供了一个有希望的方向。
Kayama说,“这项研究确定了一种减少结肠中中性粒细胞数量和预防严重结肠炎的机制。我们希望我们的研究成果将导致对溃疡性结肠炎病因的阐明和新疗法的开发。我们要向所有的同事和提供样本的患者表示最深切的感谢。”(生物谷 Bioon.com)
参考资料:
Haruka Tani et al.
The ATP-hydrolyzing ectoenzyme E-NTPD8 attenuates colitis through modulation of P2X4 receptor-dependent metabolism in myeloid cells. PNAS, 2021, doi:10.1073/pnas.2100594118.
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


