Journal for ImmunoTherapy of Cancer:新型表达增强杂交IgGA Fc PD-L1抑制剂的溶瘤腺病毒可激活多种免疫效应群体,从而增强体外、体内和患者来源的肿瘤类器官的肿瘤杀伤
来源:生物谷 2021-08-23 14:11
研究者证明了交叉同种型Fc区使ICI能够在各种肿瘤细胞系中引发IgA和IgG同种型的效应机制,随后多种效应机制的激活进一步增强了肿瘤杀伤,并被证明优于PD-L1 IgG1抗体或Atezolizumab(目前已被FDA批准的ICI)。
免疫检查点抑制剂(ICI)疗法已被确立为多种肿瘤类型的有效治疗选择,所有临床批准的ICI都是主要作为拮抗剂的抗体,其主要作用机制是通过破坏免疫抑制轴来重建T细胞反应。然而,ICI要么有限,要么完全不能引发关键的抗体依赖性效应机制,例如与抗体相关的补体依赖性细胞毒性(CDC)或抗体依赖性细胞毒性/吞噬作用(ADCC/ADCP)。根据临床数据,激活效应机制是治疗性抗体实现肿瘤清除的必要条件,此外,ADCC和CDC等效应机制是增强针对细胞毒性T淋巴细胞相关蛋白4(CTLA-48)或程序性死亡受体1(PD-L1)的某些改良ICI的抗肿瘤反应的必要条件。因此,通过Fc片段配备或增强具有这种效应机制的ICI可能会提高疗效,从而提高临床反应率。
图片来源:http://dx.doi.org/10.1136/jitc-2021-003000
该研究开发了一种抗PD-L1的Fc融合肽,称为IgGA。由一个包含IgG1和IgA1恒定区的交叉杂交Fc区组成,连接到PD-1胞外域,携带有经甘氨酸衔接物增加其对PD-L1亲和力的突变。研究者证明了交叉同种型Fc区使ICI能够在各种肿瘤细胞系中引发IgA和IgG同种型的效应机制,随后多种效应机制的激活进一步增强了肿瘤杀伤,并被证明优于PD-L1 IgG1抗体或Atezolizumab(目前已被FDA批准的ICI)。
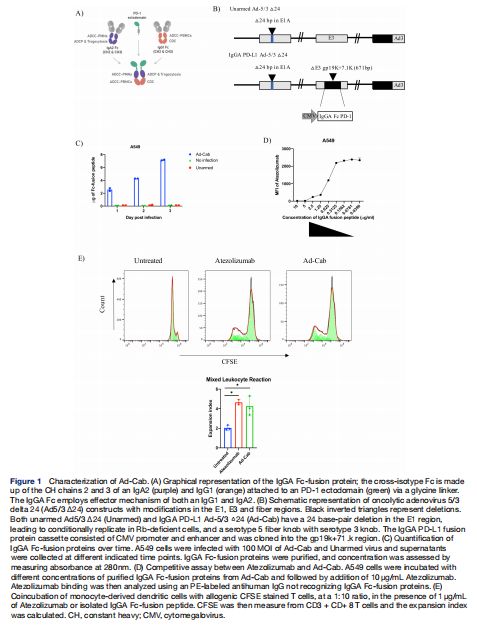
Ad-Cab的表征 图片来源:http://dx.doi.org/10.1136/jitc-2021-003000
研究者生成了一种溶瘤腺病毒Ad-Cab(腺病毒嵌合抗体),表达了一种嵌合IgG-IgA (IgGA) Fc,将其克隆到E3A基因的gp19K+7.1K区域。为了评估产生的Fc融合肽是否可以与PD-L1结合,研究者使用市售的抗PD-L1(Atezolizumab)进行了竞争测定,将A549细胞与浓度不断增加的Fc融合肽共同培养,从感染细胞的上清液中纯化,然后加入10 μg/mL的Atezolizumab,然后通过添加不能识别Fc融合肽的二级PE标记的抗人IgG来分析结合Atezolizumab与PD-L1的检测。
结果表明,当不添加Fc融合肽时,Atezolizumab能够与PD-L1结合,然而,随着Fc融合肽浓度的增加,Atezolizumab的结合显著降低。为了测试Fc融合肽激活CD8+ T细胞的能力,进行了同种异体混合白细胞反应,在该测定中,来自一个供体的单核细胞分化的树突细胞与来自另一个供体的分离的CFSE(羧基荧光素二乙酸酯,琥珀酰亚胺酯)染色的外周血单个核细胞(PBMC)混合,以模拟PD-L1/PD1相互作用的免疫抑制作用。使用或不使用Atezolizumab或纯化的IgGA Fc融合肽处理样品,以测试阻断PD-L1是否可以诱导T细胞扩增,当添加Atezolizumab和IgGA Fc融合肽时,观察到CD8+ T细胞明显扩增,在计算它们的扩增指数时,Atezolizumab和IgGA Fc融合肽均高于模拟物,证明了Ad-Cab可以分泌高水平的Fc融合肽,该肽能够PD-L1结合,在竞争中胜过Atezolizumab并激活CD8+T细胞。

激活免疫系统的多个分支 图片来源:http://dx.doi.org/10.1136/jitc-2021-003000
在测试表达和结合后,研究者检测了Fc融合肽激活抗体效应机制的能力,由于Fc需要IgG1 和IgA1的杂交体,CDC和ADCC用中性粒细胞(PMN)和PBMC在表达不同水平PD-L1的六种不同的人和鼠肿瘤细胞系上进行了测试。细胞首先用Ad-Cab或未武装的溶瘤腺病毒(Ad-5/3 Δ24)以两种不同的感染复数(MOI,10和100)感染2天,以限制人细胞系(MDA-MB-436和A549)的溶瘤作用,随后,当加入补体活性血清时,可以观察到 Ad-Cab 感染细胞的细胞裂解,在MOI为10时,细胞裂解正在发生,并且随着所有六种细胞系中的MOI增加到100,细胞裂解进一步增强。然后用两种不同的免疫群体测试ADCC检测:PBMC和PMN,与CDC相比,在MOI 10时,当添加PBMC或PMN时,用Ad-Cab感染的所有细胞系都可以观察到ADCC的最小诱导或没有诱导。最后,研究者测试Ad-Cab激活巨噬细胞和诱导ADCP的能力,引发ADCP的能力由来自用CFSE标记的肿瘤细胞系的巨噬细胞摄取CFSE来确定。在MOI 10 时,在任何条件下均未观察到CFSE摄取,但在MOI 100时,当添加Ad-Cab时,在所有细胞系中都可以观察到巨噬细胞对CFSE的摄取增加,这些数据表明分泌的Fc融合肽可以诱导IgG1和IgA的效应机制。
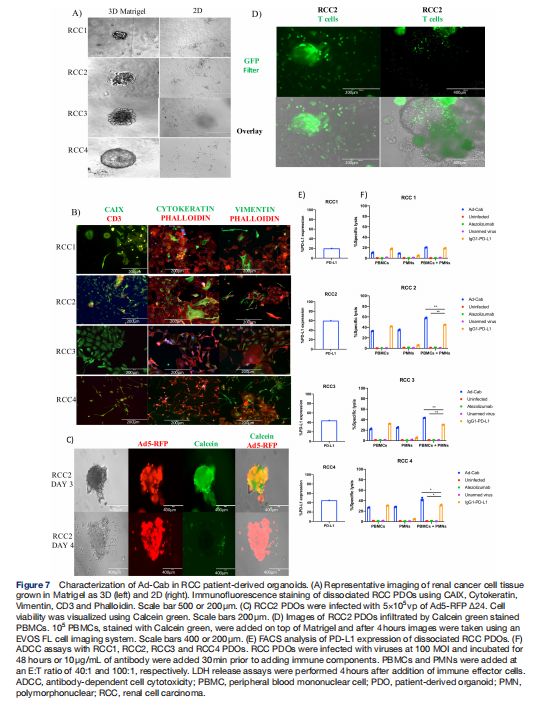
在RCC患者来源的类器官中表征Ad-Cab 图片来源:http://dx.doi.org/10.1136/jitc-2021-003000
为了进一步研究Ad-Cab的IgA部分贡献,研究者开发了一个使用肾癌患者来源的类器官,直接从患者肿瘤组织开发来的(RCC PDO)新型测试平台。在将RCC类器官优化为Ad Cab的功能测试平台后,研究者使用它们来执行PBMC和PMN的ADCC实验,RCC类器官首先被病毒感染或用抗体处理并孵育3天,从ADCC结果可以明显看出,当将PBMC添加到类器官时,Ad-Cab和IgG1 PD-L1抗体观察到相似水平的细胞毒性。与体外数据一致,当添加PMN作为效应细胞时,只能用Ad-Cab观察到细胞毒性,而不能用IgG1 PD-L1抗体观察到细胞毒性,当同时添加两个效应细胞群时,与单独添加每个群时相比,Ad-Cab增强了细胞杀伤。这可以通过以下事实来解释:当单独添加每个效应子群时,所有表达PD-L1的细胞都被杀死了。
Fc融合肽能够激活PBMC,通常由IgG1抗体激活,并参与一个被忽视但重要的群体PMN。 两种群体的这种共同参与显示出协同作用,在各种PD-L1表达细胞系和RCC PDO中增强了肿瘤杀伤,这样的临床前结果促使Ad-Cab进一步研究走向临床开发的道路。(生物谷 bioon)
参考文献
Firas Hamdan et al. Novel oncolytic adenovirus expressing enhanced cross-hybrid IgGA Fc PD-L1 inhibitor activates multiple immune effector populations leading to enhanced tumor killing in vitro, in vivo and with patient-derived tumor organoids. Journal for ImmunoTherapy of Cancer (2021 Aug 06) doi:http://dx.doi.org/10.1136/jitc-2021-003000
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。